
- DAZ.online
- DAZ / AZ
- DAZ 21/2019
- Schädliche Strahlung
Beratung
Schädliche Strahlung
Wenn Arzneistoffe photoallergische oder phototoxische Hautreaktionen begünstigen
Eine systematische Übersichtsarbeit aus dem vergangenen Jahr hat ergeben, dass die Evidenz für lichtbedingte Nebenwirkungen gering ist. Nach der Auswertung von 240 Studien mit 129 verschiedenen Wirkstoffen waren fast 90% der Untersuchungen hinsichtlich phototoxischer oder photoallergischer Reaktionen von geringer Aussagekraft. Die Autoren sehen die Ursache beispielsweise darin, dass lichtbedingte Hautreaktionen in Zusammenhang mit der Einnahme bestimmter Wirkstoffe zu selten berichtet und häufig fehldiagnostiziert werden. Erschwert wird die Dokumentation dieser Ereignisse auch durch die häufige Verwendung des ungenauen Begriffs Photosensitivität anstelle der exakten Termini Phototoxizität und Photoallergie [1].
Hypothesen zu phototoxischen Reaktionen
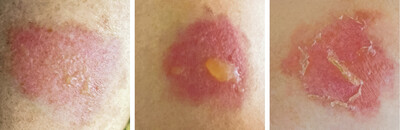
Zur Pathophysiologie phototoxischer Reaktionen gibt es verschiedene Hypothesen. Eine besagt, dass ein Wirkstoff infolge der Absorption von UV-Strahlung (bevorzugt UV-A) in einen energiereichen, aber kurzlebigen angeregten Zustand übergeht und mit Lipiden in Zellmembranen, mit Proteinen oder mit der DNA reagiert. Anschließend tritt das Molekül wieder in einen energieärmeren Zustand über. Häufig entstehen dabei auch reaktive Sauerstoffspezies (reactive oxygen species, ROS) wie Superoxid-Anionen, Hydroxylradikale und Singulett-Sauerstoff. Eine andere Hypothese geht davon aus, dass sich durch die UV-Strahlung stabile Photoprodukte und -addukte bilden, die an die DNA binden und dort Schäden hervorrufen. Phototoxische Reaktionen können innerhalb von Minuten oder Stunden nach der erstmaligen Applikation ablaufen. Die Symptome treten in den lichtexponierten Hautarealen auf und ähneln einem Sonnenbrand. Sie reichen von geröteter Haut bis zur Blasenbildung (siehe Abb. 1).
Photoallergische Reaktionen mit Verzögerung
Im Gegensatz dazu werden photoallergische Reaktionen durch das Immunsystem vermittelt. Voraussetzung ist die kovalente Bindung an ein endogenes Protein in Gegenwart von UV-Strahlung und die Bildung eines Photoantigens. Dieses wird anschließend den immunkompetenten Zellen in der Dermis präsentiert. Bei erneuter Exposition mit dem Arzneistoff kommt es zu einer T-Zell-vermittelten Typ-IV-Reaktion (Spättyp-Reaktion). Dabei werden proinflammatorische Zytokine freigesetzt, die in der Haut zu Entzündungen und Ekzembildung führen. Photoallergisch bedingte Reaktionen treten meistens mit einer Verzögerung von einem bis drei Tagen nach der Applikation auf. Sie können auch in Bereichen sichtbar werden, die nicht der Sonne ausgesetzt waren. Zu den Photoallergenen zählen einige Topika wie beispielsweise nichtsteroidale Antirheumatika (NSAR) (z. B. Ketoprofen, Piroxicam, Diclofenac), Benzocain (als Lokalanästhetikum) oder Chlorhexidin. Einige Wirkstoffe wie Thiazid-Diuretika können sowohl phototoxisch als auch photoallergen wirken [5].
Häufig verordnet – häufig berichtet
Die meisten Berichte verzeichnete der Review zu Amiodaron, Chlorpromazin, Doxycyclin, Hydrochlorothiazid (HCT), Vemurafenib und Voriconazol. Das bedeutet aber nicht, dass diese Wirkstoffe das gleiche Potenzial für phototoxische oder photoallergische Reaktionen besitzen. Beispielsweise wird das Potenzial unter Hydrochlorothiazid als relativ niedrig eingestuft. Die zahlreichen Berichte sind aller Wahrscheinlichkeit nach auf die häufige Verordnung dieses Wirkstoffs zurückzuführen. Im vergangenen Jahr geriet das Diuretikum, das auch Bestandteil zahlreicher Kombinationsarzneimittel ist, außerdem wegen eines möglicherweise erhöhten Hautkrebsrisikos in den Fokus. Ein Rote-Hand-Brief [2] hatte über zwei pharmakoepidemiologische Studien aus Dänemark informiert, die einen kumulativen dosisabhängigen Zusammenhang zwischen Hydrochlorothiazid und der Entwicklung der beiden Hautkrebsformen Basalzellkarzinom (Basaliom) und Plattenepithelkarzinom (Spinaliom) nahelegen. Man vermutet, dass bei ihrer Entstehung die phototoxische Wirkung von HCT eine Rolle spielen könnte.
Johanniskraut: Risiko geringer als vermutet?
In den Packungsbeilagen und Fachinformationen rezeptfreier und verschreibungspflichtiger Johanniskraut-Präparate lassen sich entweder keine Häufigkeitsangaben oder lediglich Verweise auf eine selten vorkommende erhöhte Empfindlichkeit der Haut gegenüber intensiver UV-Bestrahlung bei hellhäutigen Personen finden. Als Folge könnten auf Hautpartien, die starker Sonnenbestrahlung ausgesetzt waren, sonnenbrandähnliche Reaktionen (Rötungen) oder auch Missempfindungen wie Kribbeln, Schmerz- und Kälteempfindlichkeit oder Brennen auftreten. Photodermatosen, wie sie bei hellhäutigen Weidetieren nach dem Fressen großer Mengen Johanniskraut beobachtet wurden, scheinen beim Menschen äußerst selten zu sein. Als Ursache wird vermutet, dass die Hypericin-Gewebekonzentrationen, die nach oraler Anwendung therapeutischer Dosierungen von Johanniskraut-Extrakt erreicht werden können, zu gering sind, um solche Nebenwirkungen auslösen zu können [3].
Beratungstipps zur Prävention
Im Rote-Hand-Brief wurde empfohlen, Patienten unter Hydrochlorothiazid (Mono- und Kombinationspräparate) über das Risiko von weißem Hautkrebs zu informieren. Sie sollten dazu angehalten werden, ihre Haut regelmäßig auf neue Hautveränderungen sowie Veränderungen an bestehenden Läsionen zu untersuchen und verdächtige Beobachtungen zu melden. Außerdem wurde dazu geraten, die Exposition gegenüber Sonnenlicht und UV-Strahlen einzuschränken. Falls das nicht möglich sei, solle ein angemessener Schutz verwendet werden [2]. Die beiden letztgenannten Empfehlungen lassen sich auf alle Arzneistoffe übertragen, bei denen ein phototoxisches oder photoallergisches Potenzial bekannt ist. Insbesondere bei Neuverordnung eines Präparats sollten Patienten darauf hingewiesen werden. Als „angemessener Schutz“ gelten dabei:
- die Anwendung von Sonnenschutzmitteln mit Schutz vor UV-A- und UV-B-Strahlung,
- das Vermeiden von Sonnenexposition in der Zeit von 11 bis 15 Uhr,
- das Tragen von hautbedeckender Kleidung und gegebenenfalls einer Kopfbedeckung beim Aufenthalt in der Sonne,
- der Verzicht auf Solariumbesuche,
- falls relevant, das Bekleben von Fensterscheiben mit UV-undurchlässigen Folien,
- wenn möglich, die Einnahme des potenziell phototoxischen Medikaments auf den Abend verlegen [4].
Auf Sonnenschutzmitteln weist das Symbol „UV-A im Kreis“ darauf hin, dass die in der EU geforderte UV-A-/UV-B-Balance erfüllt wird. Das bedeutet, dass der UV-A-Schutz ein Drittel des UV-B-Schutzes beträgt.
Ist eine Lichtreaktion aufgetreten, können die betroffenen Hautpartien mit Cortison-haltigen Dermatika behandelt werden. Die beste Lösung wäre das Absetzen des Medikaments, sofern eine gut verträgliche Alternative zur Verfügung steht. Im Falle von Hydrochlorothiazid kommen Indapamid und Chlortalidon mit einem geringeren Risiko für phototoxische Reaktionen infrage (siehe Tabelle).
Wirkstoffgruppe |
Wirkstoff |
Präparat (Beispiele) |
Häufigkeit laut Fachinformation |
|---|---|---|---|
Antiarrhythmika |
Amiodaron |
Cordarex® Tabletten
|
sehr häufig |
Antibiotika | |||
Tetracycline |
Doxycyclin |
Doxycyclin AL Tabletten |
sehr häufig |
Minocyclin |
Minocyclin-ratiopharm® Kapseln
|
häufig |
|
Fluorchinolone |
Ciprofloxacin |
Ciprobay® Tabletten
|
selten |
Levofloxacin |
Tavanic® Tabletten
|
keine Angabe |
|
Antidiabetika |
Glibenclamid |
Glib-ratiopharm® S Tabletten
|
gelegentlich |
Antihypertensiva | |||
Calcium-Antagonisten |
Amlodipin |
Amlodigamma® Top Tabletten
|
sehr selten |
Diltiazem |
Dilzem® retard Tabletten
|
keine Angabe |
|
Nifedipin |
Adalat® Weichkapseln
|
selten |
|
ACE-Hemmer |
Enalapril |
Enalapril-ct Tabletten |
keine Angabe |
Quinapril |
Accupro® Filmtabletten
|
gelegentlich |
|
Ramipril |
Delix® Tabletten
|
sehr selten |
|
Antikonvulsiva |
Carbamazepin |
Tegretal® Tabletten
|
sehr selten |
Antimykotika |
Voriconazol |
Vfend® Filmtabletten
|
gelegentlich |
Diuretika |
Chlortalidon |
Hygroton® Tabletten
|
selten |
Furosemid |
Lasix® Tabletten
|
gelegentlich |
|
Hydrochlorothiazid |
Hct-ct Tabletten |
gelegentlich |
|
Indapamid |
Natrilix® Tabletten
|
keine Angabe |
|
Xipamid |
Xipagamma® Tabletten |
selten |
|
Immuntherapeutika |
Methotrexat |
Metex® Tabletten
|
gelegentlich |
nichtsteroidale Antirheumatika |
Celecoxib |
Celebrex® Kapseln
|
selten |
Dexibuprofen |
Deltaran® Tabletten
|
sehr selten |
|
Diclofenac |
Voltaren® Tabletten
|
sehr selten |
|
Naproxen |
Aleve® Tabletten
|
sehr selten |
|
Piroxicam |
Piroxicam Hexal® Tabletten
|
gelegentlich |
|
Protonenpumpen-inhibitoren |
Esomeprazol |
Nexium® Mups Tabletten |
selten |
Lansoprazol |
Agopton® Kapseln |
selten |
|
Omeprazol |
Antra Mups® Tabletten |
selten |
|
Pantoprazol |
Pantozol® Tabletten
|
keine Angabe |
|
Retinoide |
Acitretin |
Acicutan® Kapseln
|
gelegentlich |
Isotretinoin |
Aknenormin® Kapseln
|
selten |
|
Tumortherapeutika |
Dacarbazin |
Detimedac® Trockensubstanz
|
gelegentlich |
Epirubicin |
Epirubicin Hexal® Inj.-Lösung
|
keine Angabe |
|
Imatinib |
Glivec® Tabletten
|
häufig |
|
Vandetanib |
Caprelsa® Tabletten
|
sehr häufig |
|
Vemurafenib |
Zelboraf® Tabletten
|
sehr häufig |
|
Vinblastin |
Vinblastinsulfat Teva Inj.-Lösung |
keine Angabe |
|
Kategorien: sehr häufig (≥ 1/10); häufig (≥ 1/100 bis < 1/10); gelegentlich (≥ 1/1000 bis < 1/100); selten (≥ 1/10.000 bis < 1/1000); sehr selten (< 1/10.000) | |||
Überforderte Schutzmechanismen
Die menschliche Haut ist mit zahlreichen Schutzmechanismen ausgestattet. Beispielsweise sind Keratinozyten in der Lage, Enzyme wie die Superoxiddismutase, die Glutathionperoxidase und die Katalase zu exprimieren, um reaktive Sauerstoffspezies zu neutralisieren. Geschädigte DNA und Lipidmembranen können repariert, zerstörte Proteine entsorgt werden. Sind diese Mechanismen überfordert, kommt es zu Schädigungen. Außerdem hat man herausgefunden, dass Vitamin D3 die Keratinozyten vor lichtbedingten Schäden zu schützen vermag. Patienten mit niedrigen Vitamin-D3-Spiegeln könnten also empfänglicher sein. Insgesamt scheint es große interindividuelle Unterschiede bei der medikamentös bedingten Lichtempfindlichkeit zu geben [5].
Blick in die Zukunft
Aktuelle Forschungen eröffnen weitere Möglichkeiten, die Hautzellen vor UV-Schäden zu schützen. Ein interessanter Ansatz ist beispielsweise die Aktivierung des Transkriptionsfaktors Nrf2 (nuclear factor E2-related factor 2). Im Mausmodell ist es gelungen, die Tiere mithilfe eines Nrf2-Induktors vor UV-A-bedingten Schäden unter einer Azathioprin-Behandlung zu bewahren. Die Autoren stellen sich vor, dass zukünftig Nrf2-Induktoren als Wirkstoffpflaster auf der Haut vor Phototoxizität durch Azathioprin oder andere Wirkstoffe schützen könnten [5, 6]. |
Literatur
[1] Kim WB et al. Drug-induced phototoxicity: A systematic review. J Am Acad Dermatol 2018;79(6):1069-1075
[2] Hydrochlorothiazid – Risiko von nichtmelanozytärem Hautkrebs. Rote-Hand-Brief vom 17. Oktober 2018, www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RHB/2018/rhb-hydrochlorothiazid.html, Abruf am 24. April 2019
[3] Teuscher E, Melzig M, Lindequist U. Biogene Arzneimittel. Lehrbuch der Pharmazeutischen Biologie. Wissenschaftliche Verlagsgesellschaft Stuttgart, 7. Auflage 2012
[4] Vorsicht Sonne: Medikamente machen Haut lichtempfindlicher. Pressemitteilung der ABDA vom 26. Juli 2013, www.abda.de/pressemitteilung/artikel/vorsicht-sonne-medikamente-machen-haut-lichtempfindlicher, Abruf am 23. April 2019
[5] Khandpur S et al. Drug-induced photosensitivity: new insights into pathomechanisms and clinical variation through basic and applied science. Br J Dermatol 2017;176:902-909
[6] Kalra S et al. Highly potent activation of Nrf2 by topical tricyclic bis(cyano enone): implications for protection against UV radiation during thiopurine therapy. Cancer Prev Res (Phila) 2012;5:973-981























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.