
- DAZ.online
- DAZ / AZ
- DAZ 11/2019
- Berlin, Essen, Boston, ...
Arzneimittel und Therapie
Berlin, Essen, Boston, London, Düsseldorf ...
... und dazwischen noch China: Erfolge und Misserfolge in der Heilung der HIV-Infektion
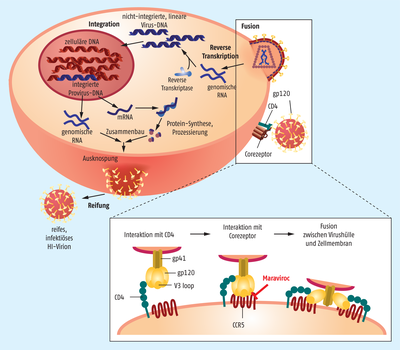
Infiziert das Humane Immundefizienz-Virus (HIV) 1 eine T-Helferzelle, benötigt es nicht nur das Oberflächenmolekül CD4, sondern zusätzlich einen Corezeptor – wahlweise CCR5 oder CXCR4 –, um in die Zelle einzudringen. Dies ist ein extrem wichtiger Schritt im „Leben“ von HIV, der bereits erfolgreich mit dem CCR5-Antagonisten Maraviroc (Celsentri®) unterbunden werden kann (s. Abbildung). Bevor das Arzneimittel eingesetzt wird, muss zwingend getestet werden, ob der zu behandelnde Patient tatsächlich mit sogenannten R5-HI-Viren, also CCR5-tropen Viren, infiziert ist.
CCR5 ist ein Rezeptor für kleine Signalmoleküle im Körper und wird neben T-Zellen auch auf verschiedenen anderen Immunzellen, wie natürlichen Killerzellen, Makrophagen und unreifen dendritischen Zellen vor allem nach Stimulation durch proinflammatorische Zytokine exprimiert [1]. Der Signalweiterleitung über CCR5 in die Zelle wird eine wichtige Rolle bei der Rekrutierung von Immunzellen in Entzündungsherde, aber auch für die Proliferation und Metastasierung von Tumorzellen zugeschrieben [2].
In der europäischen Bevölkerung kommt mit einer Frequenz von 10% eine Deletion von 32 Basenpaaren im CCR5-Gen (CCR5Δ32) vor, die dazu führt, dass das Rezeptormolekül nicht in die Zellmembran eingebaut wird und somit funktionslos ist. Dass diese Mutation in Europa so häufig vertreten ist, wird auf die Beulenpest- und Pocken-Epidemien im Mittelalter zurückgeführt. Offensichtlich verschaffte ein nicht funktionelles CCR5-Molekül bei diesen Erkrankungen einen Überlebensvorteil [3]. Während etwa 1% der Europäer homozygote Träger der CCR5Δ32-Mutation sind, tritt sie in der asiatischen Bevölkerung praktisch nicht auf.
Stammzelltransplantationen bei HIV-positiven Patienten
Für erste Schlagzeilen sorgte der als „Berliner Patient“ in die Medizingeschichte eingegangene Timothy Ray Brown. Zehn Jahre nach der HIV-Diagnose erkrankte er zusätzlich an einer akuten myeloischen Leukämie (AML), die sich als therapierefraktär herausstellte. Die letzte Option bestand in einer Knochenmarktransplantation, für die die behandelnden Ärzte einen Spender auswählten, der zusätzlich zur Gewebe-Kompatibilität auch homozygoter Träger der CCR5Δ32-Mutation war [4]. Nach zwei Runden starker Chemo- und Radiotherapie zur Zerstörung des eigenen Immunsystems und Transplantation von CCR5Δ32-Stammzellen gilt Timothy Ray Brown nach mittlerweile mehr als zehn Jahren ohne nachweisbare HI-Viren im Körper als geheilt.
Weniger erfolgreich verlief die Therapie beim sogenannten „Essener Patienten“, der infolge eines anaplastisch-großzelligen Lymphoms ebenfalls eine Knochenmarktransplantation erhielt. Auch in diesem Fall wurden wegen einer gleichzeitig vorliegenden HIV-Infektion homozygote CCR5Δ32-Stammzellen transplantiert. Allerdings wurde vor der Transplantation die antiretrovirale Therapie (ART) ausgesetzt. Recht schnell nach der Stammzelltherapie stieg die Anzahl der HI-Viren im Blut des Patienten wieder an. Diese Viren erwiesen sich jedoch als CXCR4-trope Varianten [5, 6]. Ein fataler Umstand, denn diese Viren, die CXCR4 als Corezeptor benutzen, wurden durch das Knochenmarktransplantat des CCR5Δ32-Spenders nicht am Eindringen in eine kompatible Zelle gehindert.
Zwei HIV-positive Patienten in Boston, die wegen eines Hodgkin- bzw. eines Non-Hodgkin-Lymphoms eine Knochenmarkspende von Spendern mit Wildtyp-CCR5-Gen erhielten, hatten zwar durch die Kombination aus antiretroviraler und konditionierender Chemotherapie eine kurzfristig erniedrigte Viruslast. Allerdings konnten sich Viren, die sich offensichtlich in tiefen Kompartimenten des Wirtsorganismus versteckt hatten, nach einem Auslassversuch der ART schnell wieder in den CCR5-positiven Blutzellen vermehren [7].
Jetzt kam erneut die Meldung eines wahrscheinlichen Heilungserfolgs mit dem sogenannten „Londoner Patienten“. Auch dieser Patient erhielt zur Therapie eines Hodgkin-Lymphoms eine allogene Stammzelltransplantation eines homozygoten CCR5Δ32-Spenders nach einer konditionierenden Chemotherapie. Die antiretrovirale Therapie wurde während der Krebsbehandlung fortgeführt und erst 16 Monate nach der Transplantation gestoppt. Zu diesem Zeitpunkt waren keine Viren nachweisbar, und dieser vermeintlich HIV-negative Zustand hält sich mittlerweile seit weiteren 18 Monaten ohne ART [8]. Sechs andere HIV-positive Leukämie-Patienten, bei denen nach einer CCR5Δ32-Stammzellspende keine Viren mehr nachweisbar waren – darunter auch der sogenannte „Düsseldorfer Patient“, werden derzeit an verschiedenen Standorten beobachtet. Es könnten also mittlerweile durchaus mehr als nur ein oder zwei HIV-Patienten von ihrer Virusinfektion geheilt sein [9].
Gentherapie als Hoffnungsträger?
Ende letzten Jahres sorgte die Geburt von Zwillingen in China für Aufregung. Die Kinder wurden durch In-vitro-Fertilisation gezeugt, und gleichzeitig wurde mithilfe der Genschere CRISPR/Cas9 die CCR5Δ32-Mutation in das Genom eingeführt. Ziel war, die Kinder über diese Mutation resistent gegen eine HIV-Infektion zu machen, die ihnen beispielsweise über ihren HIV-positiven Vater drohen könnte [10]. Damit sollte also über Gentherapie an der befruchteten Eizelle der Zustand erreicht werden, der bei ca. 1% der Europäer natürlicherweise vorliegt und wahrscheinlich einen Schutz vor einer HIV-Infektion darstellt. Das Problem der Kinder wird jedoch vermutlich sein, dass die Gentherapie unvollständig verlaufen ist und die Mutation nicht in allen Zellen auftritt. Somit könnten immer noch Immunzellen mit Wildtyp-CCR5-Molekülen vorliegen, die als Wirtszellen für HIV dienen.
Konsens herrscht zwischenzeitlich unter Wissenschaftlern, Ethikern und einem großen Teil der interessierten Bevölkerung, dass eine Keimbahn-Manipulation nicht der richtige Weg ist, HIV-Resistenz herzustellen. Das ist auch nicht erforderlich. Denn alternative Gentherapieansätze mithilfe der CRISPR/Cas9-Methode an einem allogenen oder autologen Transplantat könnten entwickelt werden, um die zu transplantierenden Zellen so zu modifizieren, dass sie keine funktionellen CCR5-Moleküle mehr exprimieren. Allerdings muss auch hier sichergestellt sein, dass beide CCR5-Allele inaktiviert sind. Das ist kein leichtes Unterfangen, so dass an einer sicheren, weitläufig verbreiteten Lösung noch intensiv gearbeitet werden muss [11].
Lehren aus den Heilungserfolgen
Selbst wenn die wenigen Heilungserfolge einer HIV-Infektion über eine passende Knochenmarkspende erzielt wurden, ist das Procedere zu aufwändig und gefährlich, als dass die allogene Stammzelltransplantation die Methode der Wahl zur Elimination von HIV werden könnte. Immerhin scheint eine so massive Konditionierung des Empfängers, wie sie beim Berliner Patienten mit Radio- und Chemotherapie durchgeführt wurde, nicht nötig zu sein. Förderlich für den Heilungserfolg und die Eradikation der HI-Viren ist offensichtlich eine Graft-versus-Host-Disease, also eine Reaktion der transplantierten Stammzellen gegen das Immunsystem des Empfängers [8]. Diese Abwehrreaktion ist eigentlich eine unerwünschte und sehr gefährliche Komplikation bei einer Transplantation. Läuft diese Reaktion jedoch unter kontrollierten Bedingungen ab, ist sie mit Sicherheit ein Teil der Lösung des eigentlichen Problems.
Bisher ist die Heilung einer HIV-Infektion über eine Stammzelltransplantation also einer recht kleinen Gruppe an Patienten vorbehalten und nach wie vor mit einigen Gefahren verbunden. Das internationale IciStem-Consortium beobachtet den Verlauf von insgesamt 39 HIV-Patienten, die wegen einer Krebserkrankung eine Stammzelltransplantation erhalten hatten. Bisher ist allerdings bereits eine signifikante Anzahl verstorben – entweder an der Stammzellspende selbst oder an der Krebserkrankung [12]. Es wird also noch einige Zeit dauern, bis eine Heilung der HIV-Infektion möglich ist, die ohne Knochenmarktransplantation auskommt. |
Quelle
[1] Ghorban K et al. Is the CCR5 Δ 32 mutation associated with immune system-related diseases? Inflammation 2013;36:633-642
[2] Aldinucci D, Casagrande N. Inhibition of the CCL5/CCR5 Axis against the Progression of Gastric Cancer. Int J Mol Sci 2018;19:pii:E1477
[3] Galvani AP, Slatkin M. Evaluating plague and smallpox as historical selective pressures for the CCR5-Delta 32 HIV-resistance allele. Proc Natl Acad Sci USA 2003;100:15276-15279
[4] Hütter G. et al. Long-term control of HIV by CCR5 Delta32/Delta32 stem-cell transplantation. N Engl J Med 2009;360:692-698
[5] Verheyen J et al. Rapid Rebound of a Preexisting CXCR4-tropic Human Immunodeficiency Virus Variant After Allogeneic Transplantation With CCR5 Δ32 Homozygous Stem Cells. Clin Infect Dis 2019;68:684-687
[6] Kordelas L et al. Shift of HIV tropism in stem-cell transplantation with CCR5 Delta32 mutation. N Engl J Med 2014;371:880-882
[7] Henrich TJ et al. Antiretroviral-free HIV-1 remission and viral rebound after allogeneic stem cell transplantation: report of 2 cases. Ann Intern Med 2014;161:319-327
[8] Gupta RK et al. HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem-cell transplantation. Nature 2019; doi:10.1038/s41586-019-1027-4
[9] Wilson C. A third person may have become HIV-free after a bone marrow transplant. NewScientist 2019;3220
[10] Zündorf I, Dingermann T. Aufregung um „CRISPR“-Babies. DAZ 2018;158:5028-5031
[11] Allen AG et al. Gene Editing of HIV-1 Co-receptors to Prevent and/or Cure Virus Infection. Front Microbiol 2018;9:2940
[12] Wilson C. Immune war with donor cells may wipe out HIV. NewScientist 2017;3124




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.