
- DAZ.online
- DAZ / AZ
- DAZ 2/2017
- Miniflux macht Makromolek...
Prisma
Miniflux macht Makromoleküle sichtbar
Fluoreszenzmikroskopie mit optimaler Trennschärfe
Bei der Fluoreszenzmikroskopie wird das zu untersuchende Objekt mit Fluoreszenzfarbstoffen markiert, die durch Licht bestimmter Wellenlängen angeregt werden, d. h. dass sie Photonen aufnehmen. Wenn sie die Photonen wieder abgeben, um in den Grundzustand zurückzukehren, senden sie das Fluoreszenzlicht aus. Die von Stefan Hell entwickelte STED-Mikroskopie (Stimulated Emission Depletion) kombiniert die Anregung im Fokus des Laserstrahls mit der Abregung (engl. depletion) in der Umgebung, sodass bei der rastermäßigen Abtastung des Objekts durch den Laserstrahl jeweils kleinste Flächen dargestellt werden und das sich aus diesen einzelnen Aufnahmen ergebende Gesamtbild erheblich schärfer erscheint. Den selben Effekt erzielt die u. a. von Eric Betzig entwickelte photoaktivierte Lokalisationsmikroskopie (PALM), bei der verschiedene photoaktivierbare fluoreszierende Proteine sukzessive durch Lichtblitze verschiedener Längenwelle angeregt werden; die angeregten Moleküle können weit voneinander entfernt liegen, und erst durch ein Computerprogramm entsteht ein Bild des Objekts. Beide Forscher haben zusammen mit William Moerner, der die Einzelmolekül-Fluoreszenzspektroskopie entwickelt hat, 2014 den Chemie-Nobelpreis erhalten.
Stefan Hell hat nun mit seinem Team am Max-Planck-Institut für biophysikalische Chemie das Mikroskop Miniflux vorgestellt, das die Prinzipien von STED und PALM kombiniert und nach dem minimalen Photonenfluss benannt ist. Die Auflösung liegt bei 1 nm, dem Zehnfachen des mittleren Atomradius (Ångström). Einzelne Proteine können als solche erkannt werden, wenn sie mindestens 6 nm voneinander entfernt sind. Zudem ermöglicht das Computerprogramm eine extrem schnelle zeitliche Auflösung, indem es neue Bilder in Bruchteilen von Millisekunden generiert, sodass eine Art Film entsteht.
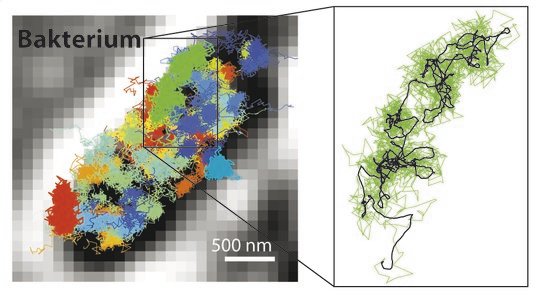
So ist es z. B. möglich, die Synthese von Proteinen in Bakterien in Echtzeit zu beobachten. Will man den Prozess genauer studieren, kann man den Film langsam abspielen oder wahlweise anhalten. Die Forscher hoffen, durch eine weitere Beschleunigung der Bildfolgen sogar die Faltung von Proteinen beobachten zu können. |
Quellen
Balzarotti F, et al. Nanometer resolution imaging and tracking of fluorescent molecules with minimal photon fluxes. Science; Epub 22.12.2016
Film Bewegungsmuster von 30S-Ribosomen in einer Bakterienzelle. Geben Sie dazu auf DAZ.online in die Suchfunktion den Webcode X2JR3 ein.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.