
- DAZ.online
- DAZ / AZ
- DAZ 41/2016
- Tödlicher Verschluss
Fortbildung
Tödlicher Verschluss
Leben retten mit Leitlinien-gerechter Thrombose-Therapie
Die venöse Thromboembolie mit den Symptomen tiefe Beinvenenthrombose (TVT) und Lungenembolie (LE) ist eine häufige Erkrankung. In den USA wird die Inzidenz für neu aufgetretene Beinvenenthrombosen mit ca. 100 pro 100.000 Personen pro Jahr angegeben. Auch wenn für Deutschland keine genauen Zahlen vorliegen, werden sie in einer vergleichbaren Größenordnung liegen. Die Zahl tödlich verlaufender Lungenembolien als Folge tiefer Beinvenenthrombosen liegt in der Bundesrepublik bei etwa 40.000 pro Jahr. Damit ist die letale Lungenembolie als Form der venösen Thromboembolie die dritthäufigste stationäre Todesursache in Deutschland.
Die zunehmende Alterung der Bevölkerung, aggressive Behandlungsverfahren und die Multimorbidität der oft älteren Patienten führen zu einer unverändert hohen Inzidenz venöser Thromboembolien bei Patienten.
Zahlreiche populationsbezogene Studien weisen eine enge Korrelation zwischen dem höheren Lebensalter und der Inzidenz venöser Thromboembolien nach. Das Risiko einer venösen Thromboembolie bei Patienten über 60 Jahren steigt exponenziell. Bei unter 40-Jährigen findet man bei 30 pro 100.000 Personen eine tiefe Thrombose, bei über 70-Jährigen bei 300 bis 500 Patienten pro 100.000 Personen.
Wie venöse Thrombosen entstehen
Die Virchow-Trias führt die pathogenetischen Mechanismen einer venösen Thrombose auf, wobei die einzelnen Mechanismen entsprechend der jeweiligen auslösenden Ursache oder Erkrankung eine unterschiedliche klinische Wertigkeit besitzen.
Virchow-Trias
Stase (Immobilität)
Venenwandschädigung
Übergerinnbarkeit (Hyperkoagulabilität)
Die venöse Stase ist durch die krankheitsbedingte Immobilität hervorgerufen, die den venösen Rückfluss durch Inaktivierung der Muskelvenenpumpe beeinträchtigt. Zusätzliche pathologische Befunde (externe Venenkompression durch Lymphknoten, Hämatome, Kompressionssyndrome, Tumore im kleinen Becken, Aszites u. a.) reduzieren den venösen Rückstrom. Aber auch eine klinisch manifeste Rechtsherzinsuffizienz führt über kardiale Ödeme und eine verminderte kardiale Pumpfunktion zur venösen Stase.
Direkte Venenwandschädigungen sind zum einen Endothelläsionen, ausgelöst durch internistische Erkrankungen mit Exprimierung von wandständigen Gerinnungsfaktoren, zum anderen oft Folge von invasiven diagnostischen und/oder therapeutischen Maßnahmen. Natürlich können auch Entzündungen, invasiv wachsende Tumoren, chirurgische Eingriffe und Bestrahlungen zu einer direkten Venenwandschädigung führen.
Die Übergerinnbarkeit oder Hyperkoagulabilität kann angeboren (z. B. Homocysteinämie) oder erworben (z. B. Leberinsuffizienz) sein. Bei einer Gerinnungsneigung können auslösende Begleiterkrankungen/Faktoren bei Vorliegen einer Hyperkoagulabilität zu einer Thrombose führen.
Hereditäre und erworbene Thrombophilien können die Erstmanifestation einer venösen Thromboembolie begünstigen oder verursachen. In der Regel manifestiert sich eine genetisch determinierte venöse Thromboembolie bis zum 50. Lebensjahr. In späterem Lebensalter kommt der Thrombophilie als Thromboseursache keine Bedeutung mehr zu.
Die Bedeutung der Thrombophilie wird vielfach überschätzt. Außer bei homozygoten Formen der sehr seltenen Faktor-V- Mutation und wenigen weiteren Veränderungen ist das Risiko eher gering.
TVT mit unspezifischen klinischen Symptomen
Klinische Hauptmanifestation in den Becken-Beinvenen (> 90% aller Thrombosen) mit den klinischen Kardinalsymptomen sind Beinschwellung, Schmerz, Überwärmung, livide Verfärbung und vermehrte Venenzeichnung.
Allerdings sind die klinischen Zeichen oft trügerisch oder fehlen ganz. Nur etwa 30% der Patienten weisen die typischen klinischen Zeichen der venösen Thromboembolie (VTE) auf. Häufig findet man sie nur bei proximaler Thrombose. Das bedeutet im Umkehrschluss: Das Fehlen klinischer Symptome schließt eine Thrombose nicht aus!
Jeden Verdacht abklären!
Jeder klinische Verdacht auf Venenthrombose soll umgehend abgeklärt werden. Anamnese und körperliche Untersuchung allein sind hierzu nicht ausreichend.
Ein klinisches Modell zur Abschätzung der klinischen Vortestwahrscheinlichkeit einer tiefen Beinvenenthrombose wurde von Wells entwickelt. Neben anamnestischen Angaben gehen klinische Kriterien (Wadenumfangdifferenz, Ödem, Druckschmerzhaftigkeit der Venen, Rötung) in das Modell mit ein (Tab. 1).
Kriterium |
Punkte |
|---|---|
aktive Tumorerkrankung |
1 |
Immobilisation der Beine (Gips, Lähmung) |
1 |
Bettlägerigkeit für mehr als drei Tage, OP innerhalb von zwölf Wochen |
1 |
Schmerzhaftigkeit im Verlauf der Venen |
1 |
Schwellung des gesamten Beins |
1 |
Umfangdifferenz (Wade) > 3 cm |
1 |
Ödem im symptomatischen Bein |
1 |
oberflächliche Kollateralvenen |
1 |
frühere tiefe Venenthrombose (TVT) |
1 |
alternative Diagnose zur TVT |
-2 |
Wahrscheinlichkeit niedrig |
Summe < 2 |
Wahrscheinlichkeit hoch |
Summe ≥ 2 |
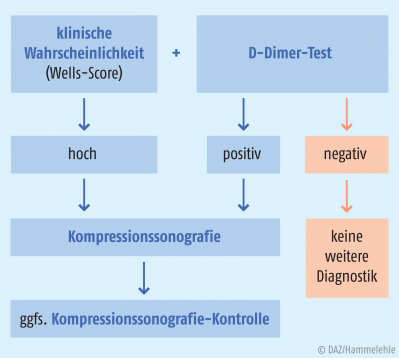
Nach Anamnese und klinischen Symptomen kann anhand des Wells-Score die Wahrscheinlichkeit abgeschätzt und weitere diagnostische Maßnahmen zum Ausschluss oder Nachweis einer tiefen Beinvenenthrombose getroffen werden. Dazu zählen die laborchemische Bestimmung der D-Dimer-Konzentration und bildgebende Verfahren.
D-Dimer-Bestimmung zur Ausschlussdiagnostik
D-Dimere sind Abbauprodukte des Fibrinogens. Es finden sich erhöhte D-Dimer-Konzentrationen bei frischer venöser Thromboembolie, aber auch postoperativ, bei Malignomen und anderen akuten Erkrankungen, die mit einem gesteigerten Fibrinogen-Umsatz einhergehen (z. B. Entzündungen, Verbrennungen).
Positive D-Dimer-Tests sind nicht spezifisch für eine VTE und sind damit allein nicht geeignet zum Nachweis einer venösen Thromboembolie. Allerdings können sie zusammen mit dem Wells-Score bei ambulanten Patienten ohne weitere Erkrankungen und geringer Wahrscheinlichkeit zur Ausschlussdiagnostik einer tiefen Beinvenenthrombose oder Lungenembolie herangezogen werden. Ein negativer D-Dimer-Test (Konzentration < 500 µg/l) schließt bei geringer klinischer Wahrscheinlichkeit (s. o.) eine venöse Thromboembolie mit etwa 95%-iger Sicherheit aus. Die Höhe der D-Dimer-Konzentration ist altersabhängig und steigt mit höherem Lebensalter. Hier gelten deshalb höhere Grenzwerte (Alter × 10 µg/l bei einem Lebensalter > 50 Jahre).
Mittel der Wahl: Kompressionssonografie
Bei hoher klinischer Wahrscheinlichkeit sollte auch bei negativem D-Dimer-Test eine bildgebende Diagnostik erfolgen.
Die bildgebende Diagnostik umfasst die
- Kompressionssonografie
- CT-Phlebografie
- MR-Phlebografie
- Phlebografie
Die Kompressionssonografie ist in Kombination mit der farbkodierten Duplexsonografie die Methode der Wahl zum Nachweis oder Ausschluss einer tiefen Venenthrombose. Dabei können die Lokalisation, aber auch der Anteil der blutumflossenen Thromben sichtbar gemacht werden.
Voraussetzung sind hochauflösende Geräte und Untersuchererfahrung. Mit der Sonografie können zudem noch wichtige Hinweise auf mögliche Differenzialdiagnosen (Zysten, Muskelverletzungen, Hämatome, Aneurysmata u. a.) zuverlässig erkannt werden.
Die MR- oder CT-Phlebografie bzw. Phlebografie kommen nur in unklaren Situationen zum Einsatz, wenn durch die Sonografie die Lokalisation (Becken, Abdomen) nicht genau geklärt werden kann.
Vor invasiven Behandlungsmaßnahmen (z. B. Katheterlyse, Thrombusaspiration) wird die Durchführung einer MR- oder CT-Phlebografie empfohlen (Abb. 1).
Die Diagnostik einer Rezidivthrombose ist schwierig, wenn sie im selben Venensegment auftritt. Hilfreich sind hier Ultraschallkontrollen und D-Dimer-Bestimmungen. Wegen der Problematik der Diagnosestellung der Rezidivthrombose ist es empfehlenswert, zum Zeitpunkt der Beendigung der Antikoagulation eine Bildgebung (Ultraschall) durchzuführen und den Befund zu dokumentieren.
Cave: Malignom bei älteren Patienten
Bei ätiologisch unklarer venöser Thromboembolie, insbesondere bei proximalen Thrombosen sollte eine ergänzende klinische Tumorabklärung erfolgen. Bei Tumorerkrankungen kommt es gehäuft zu venösen Thromboembolien. Bei etwa 15% der Patienten ist zum Diagnosezeitpunkt eine akute Tumorerkrankung bekannt. Das Risiko eines bislang nicht erkannten Malignoms liegt bei 5 bis 15% bei idiopathischer Thrombose und steigt bei älteren Patienten.
Der Umfang der Diagnostik ist individuell festzulegen. Empfohlen werden neben der gezielten Anamnese die klinische Untersuchung sowie Basislabor und die Durchführung der geschlechts- und altersabhängigen gesetzlichen Tumorfrüherkennungsuntersuchungen.
Therapie auch ohne Nachweis
Wenn die bildgebende Diagnostik zum Nachweis einer venösen Thromboembolie notwendig ist, aber nicht zeitnah zur Verfügung steht (z. B. am Wochenende), sollte bei hoher klinischer Wahrscheinlichkeit einer VTE mit einer Antikoagulation begonnen werden. In diesem Fall muss die Bildgebung zu einem späteren Zeitpunkt die Thrombose bestätigen oder ausschließen.
Behandlungsziele der tiefen Venenthrombose sind die Vermeidung einer Thrombusaszension und einer Lungenembolie sowie die Unterstützung der körpereigenen Thrombusauflösung oder Rekanalisation mit Erhaltung der Venenklappen und dadurch Verhinderung eines postthrombotischen Syndroms. Die etablierte Therapie der VTE beinhaltet die Kompressionsbehandlung und die Antikoagulation.
Kompressionsbehandlung mindestens zwei Jahre
Die Kompressionsbehandlung reduziert die akuten Symptome (z. B. Schmerz, Schwellneigung) und reduziert die Häufigkeit eines postthrombotischen Syndroms um etwa 50%. Dabei sind Kompressionsverbände mit Kurzzugbinden gleich wirksam wie angepasste Kompressionsstrümpfe der Kompressionsklasse 2.
Die Dauer der Kompressionsbehandlung richtet sich nach dem Ergebnis der venösen Funktionsuntersuchungen und beträgt mindestens zwei Jahre.
13. Oktober 2016: Welt-Thrombose-Tag
Am 13. Oktober 2016 findet der Welt-Thrombose-Tag unter dem Motto: „Risiko Thrombose – Es gibt eine Lösung“ statt. Veranstaltet wird er vom Aktionsbündnis Thrombose. Mit diesem Tag sollen die öffentliche Aufmerksamkeit und das Problembewusstsein in der Bevölkerung für diese komplikationsträchtige Erkrankung verbessert und die intersektorale Implementierung der Leitlinienempfehlungen unterstützt werden. So soll die Therapie durch die Zusammenarbeit von Hausärzten und Gefäßspezialisten effektiver werden. Dabei sollen auch die Kompetenzen der Apotheker zur Verbesserung der Situation genutzt werden. Mehr öffentliche Aufmerksamkeit und ein Problembewusstsein bei allen Ärzten, bei Apothekern und in der Bevölkerung sind notwendig, um die Patienten optimal versorgen zu können.
Infobüro Aktionsbündnis Thrombose, c/o Deutsche Gesellschaft für Angiologie e. V., Haus der Bundespressekonferenz, Schiffbauerdamm 40, 10117 Berlin, info@dga-gefaessmedizin.de
Diagnose Thrombose: sofort antikoagulieren!
Bei einer nachgewiesenen tiefen Venenthrombose ist eine sofortige Antikoagulation erforderlich, sofern dafür keine vitalen Kontraindikationen vorliegen. Die diagnostizierte asymptomatische Thrombose sollte wie eine symptomatische Thrombose antikoaguliert werden, begleitet von einer Kompressionsbehandlung. Die thrombusbeseitigenden Verfahren (medikamentöse Fibrinolyse, Katheterlyse, mechanische oder offene chirurgische Thrombektomie) kommen nur in Einzelfällen (z. B. May-Thurner Syndrom) zum Einsatz und stellen keine Standardtherapie dar.
Bei der medikamentösen Antikoagulation unterscheidet man eine primäre Therapie (Initialbehandlung) von einer sekundären (Erhaltungstherapie).
Für die initiale Behandlung der tiefen Venenthrombose mit einer therapeutischen Dosis zur Antikoagulation sind unfraktionierte Heparine (UFH), niedermolekulare Heparine (NMH), Fondaparinux und als orale Substanzen die direkten Faktor-Xa-Inhibitoren Apixaban und Rivaroxaban zugelassen.
Wegen der hohen Wirksamkeit und geringer Nebenwirkungen sind niedermolekulare Heparine und Fondaparinux gegenüber unfraktionierten Heparinen als Antikoagulanzien der ersten Wahl zu bevorzugen, wobei unterschiedliche Dosierungsanpassungen im Hinblick auf das Körpergewicht und die Nierenfunktion zu berücksichtigen sind.
Wegen des geringen Risikos einer Heparin-induzierten Thrombozytopenie Typ 2 (HIT Typ II) ist eine Thrombozytenkontrolle erforderlich. Darüber hinaus sind bei niedermolekularen Heparinen keine routinemäßigen Laborkontrollen notwendig. Dies erleichtert die Praktikabilität der Therapie mit niedermolekularen Heparinen oder Fondaparinux und ermöglicht auch die ambulante Behandlung der TVT.
Therapiebesonderheiten
- Die Dauer und die Art der Antikoagulation bei der Muskelvenenthrombose im Unterschenkel sind unklar und richten sich meist nach den subjektiven Beschwerden und dem Thrombosenachweis im Ultraschall. Eine isolierte distale Thrombose sollte nicht länger als drei Monate antikoaguliert werden.
- Bei der Schwangerschaftsthrombose liegen die besten Erfahrungen mit niedermolekularen Heparinen (NMH) vor, die postpartal bis zum Ende des Wochenbettes verabreicht werden sollen.
- Bei Thrombosen der Arm- und Schultervenen ist bei bis zu 30% auch mit Lungenembolien zu rechnen. Die Therapie orientiert sich an der Behandlung von Beinvenenthrombosen, und die Behandlungsdauer mit Antikoagulanzien beträgt in der Regel drei Monate. Die Entwicklung eines schweren postthrombotischen Syndroms ist wesentlich seltener.
- Bei Tumorpatienten haben sich NMH den Vitamin-K-Antagonisten als überlegen erwiesen und sind deshalb hier primäre Antikoagulanzien.
Bei schwerer Niereninsuffizienz (glomeruläre Filtrationsrate [GFR] < 30 ml/min) und bei intravenöser Rekanalisation sollte unfraktioniertes Heparin eingesetzt werden.
In der Sekundärprophylaxe (Erhaltungstherapie) nach der initialen Antikoagulation kommen in der Regel orale Antikoagulanzien zum Einsatz. Bei Verwendung von Vitamin-K-Antagonisten (z. B. Phenprocoumon) liegt der INR-Zielbereich zwischen 2 und 3. Vitamin-K-Antagonisten weisen zahlreiche Limitationen auf, beispielsweise ein schmales therapeutisches Fenster, vielfältige Ernährungs- und Medikamentenwechselwirkungen und die Notwendigkeit von regelmäßigen engmaschigen Gerinnungskontrollen.
Die neuen oralen Antikoagulanzien (NOAK) sind im Vergleich zu der bisherigen Antikoagulation mit niedermolekularen Heparinen und nachfolgender Antikoagulation mit Vitamin-K-Antagonisten mindestens gleichwertig. Vorliegende Studien zeigen eine größere Sicherheit und weniger schwere intrakranielle Blutungen. Als direkte Faktor-Xa-Hemmer sind Apixaban und Rivaroxaban (Initial- und Erhaltungsbehandlung) und Edoxaban (Erhaltungsbehandlung) zugelassen, als oraler Thrombininhibitor ist Dabigatranetexilat (Erhaltungstherapie) auf dem Markt. Ein Gerinnungsmonitoring ist unter ihnen in der Prophylaxe und Therapie nicht erforderlich. Zu beachten ist, dass die herkömmlichen Gerinnungstests bei Einnahme dieser Substanzen nicht aussagefähig sind. In Notfallsituationen müssen spezielle kalibrierte Testverfahren für die einzelnen Substanzen eingesetzt werden. Für Dabigatran steht ein sofort wirkendes spezifisches Antidot (Idarucizumab) zur Verfügung.
Beim Einsatz der verschiedenen Antikoagulanzien ist auf die Dosierung gemäß den Herstellerangaben und dabei besonders auf die Nierenfunktion zu achten (Tab. 2).
Direkte orale Antikoagulanzien |
Initialbehandlung |
Erhaltungsdosis |
|---|---|---|
Dabigatranetexilat (Pradaxa®) |
nicht zugelassen* |
300 mg (2 × 150 mg/d) |
Apixaban (Eliquis®) |
20 mg (2 × 10 mg/d) für 7 Tage |
10 mg (2 × 5 mg/d) |
Edoxaban (Lixiana®) |
nicht zugelassen* |
60 mg/d |
Rivaroxaban (Xarelto®) |
30 mg (2 × 15 mg/d) |
20 mg/d |
*Beginn der Erhaltungstherapie nach mindestens fünftägiger Behandlung mit einem parenteralen Antikoagulanz | ||
Ursachen bestimmen Therapiedauer
Die Dauer der oralen Antikoagulation richtet sich nach der Ursache der venösen Thromboembolie. Die Antikoagulation ist wirksam zur Verhinderung von Rezidiven. Die Therapiedauer richtet sich nach den Ursachen (Tab. 3). Bei ihrer Festlegung muss stets das individuelle Blutungsrisiko berücksichtigt werden.
Indikation |
Dauer |
|---|---|
erstes Ereignis bei transientem Risikofaktor (z. B. Operation) |
3 Monate |
bei idiopathischer Genese distal (Unterschenkel) |
3 Monate |
bei idiopathischer Genese proximal |
> 3 Monate |
bei geringem Blutungsrisiko |
unbegrenzt |
bei aktivem Tumorleiden NMH |
3 – 6 Monate |
dann NMH oder Vitamin-K-Antagonisten |
zeitlich unbegrenzt |
bei Rezidiv einer idiopathischen VTE |
unbegrenzt |
Das Risiko eines VTE-Rezidivs ist in den ersten Wochen nach dem akuten Ereignis am höchsten, deshalb ist hier eine kontinuierliche und suffiziente Antikoagulation unerlässlich.
Nach einem Zeitraum von drei bis zwölf Monaten nimmt das Rezidivrisiko kontinuierlich ab, bleibt aber im Vergleich zu Menschen ohne VTE langfristig erhöht.
Größere Studien zur verlängerten Rezidivprophylaxe zeigen eine Reduktion thromboembolischer Ereignisse ohne eine erhöhte Blutungsrate. Bei Risikopatienten für erneute Thromboserezidive (Männer, Residualthrombus, proximaler Thrombus, idiopathische Genese, persistierend hohe D-Dimer-Werte) kann im Einzelfall bei geringem Blutungsrisiko mit den direkten oralen Antikoagulanzien das Thromboserezidiv durch eine langfristige Antikoagulation (in reduzierter Dosis, z. B. Apixaban 2 × 2,5 mg täglich) vermieden werden.
Nach drei bis sechs Monaten sollte eine Entscheidung über die Beendigung oder Fortführung der Antikoagulation getroffen werden. Acetylsalicylsäure wird zur verlängerten Erhaltungstherapie nicht empfohlen.
Nicht immobilisieren
Während früher die Immobilisierung ein fester Bestandteil der Behandlung war, stellt diese bei regelrecht durchgeführter Antikoagulation kein begründbares Therapieprinzip dar. Es konnte sogar in kleinen, aber kontrollierten Studien nachgewiesen werden, dass sich eine Immobilisierung negativ auf das Abschwellen des Beins und die Beschwerden des Patienten auswirkt. Daher gilt: Patienten mit einer Venenthrombose jedweder Lokalisation und Morphologie sollen nicht immobilisiert werden, es sei denn zur Linderung starker Schmerzen. Im Gegensatz dazu fördert die Mobilisierung des Patienten die venöse Entstauung der betroffenen Extremität durch den Einsatz der Muskelpumpen und bewirkt damit eine Beschwerdelinderung. Diese Mobilität ist essenziell für eine ambulante Thrombosetherapie. Eine Hospitalisierung sollte nur in schweren Fällen erfolgen. Die Bedenken, dass es bei der ambulanten Behandlung der Thrombose vermehrt zu Lungenembolien kommt, erwiesen sich in randomisierten internationalen Studien sowie in großen Kohortenstudien im deutschsprachigen Raum als unbegründet. Alle Elemente der akuten Thrombosetherapie können von erfahrenen niedergelassenen Ärzten korrekt durchgeführt werden. |
Literatur
Encke A et al. S3-Leitlinie Prophylaxe der venösen Thromboembolie (VTE), 2015, awmf-reg. 003/001
Hach-Wunderle V et al. S-Leitlinie Diagnostik und Therapie der Venenthrombose und Lungenembolie. 2015, awmf-reg. 065/002
Konstantinides S et al. Guidelines on the diagnosis and management of acute pulmonary embolism: The Task force for the diagnosis and management of acute pulmonary embolism of the European Society of Cardiology (ESC). Eur Heart 2014;35:3033-3069
Gloviczki P et al. Society of Vascular Surgery. American Venous Forum. The care of patients with varicose veins and associated chronic venous diseases: clinical practice guidelines of the Society of Vascular Surgery and the American Venous Forum. J Vasc Surg 2011;53(5 Suppl.);2-48
Kahle B et al. Evidence-based treatment of chronic leg ulcers. Dtsch Ärztebl Int 2011;108:231-37
Ludwig M, Rieger J, Ruppert V. Gefäßmedizin in Praxis und Klinik. Leitlinienorientierte Angiologie, Gefäßchirurgie und interventionelle Radiologie. Stuttgart, Thieme 2010
Guyatt GH et al. 9th ACCP – Guidelines on the Prevention and Treatment on thromboembolic disease. Chest 2012;141 Suppl. 2.
S3-Leitlinie Diagnostik und Therapie des Ulcus cruris venosum. 2009, www.uni-duesseldorf.de/awmf. Nr.037/009
Shingler S et al. Compression stockings for the initial treatment of varicose veins in patients without venous ulcerations. Cochrane Database Syst. Rev. 9;12:CD008819























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.