
- DAZ.online
- DAZ / AZ
- DAZ 37/2016
- Brustkrebs – ...
Arzneimittel und Therapie
Brustkrebs – Chemotherapie ja oder nein?
Genexpressionsanalysen können bei der Entscheidung helfen
Die adjuvante und neoadjuvante Therapie einer Brustkrebserkrankung richtet sich vornehmlich nach der zugrundeliegenden Tumorbiologie und unterscheidet dabei Hormonrezeptor-positive, triple-negative und HER2-positive Tumore. Eine klare Indikation für eine Chemotherapie besteht bei triple-negativen und HER2-positiven (hier zusammen mit einer Anti-HER2-Therapie) Brustkrebserkrankungen. Bei luminalen Tumoren (Hormonrezeptor-positiv und HER2-negativ) lässt sich hingegen nicht immer klar vorhersagen, welche Patienten von einer Chemotherapie profitieren und welche nicht. Um dies im Vorfeld zu bestimmen, kann man auf prädiktive Gensignaturen zurückgreifen, um mithilfe von Multigentests das Rückfallrisiko einer Patientin besser einschätzen zu können. Diese Tests erfassen unterschiedliche Genmuster, die mit Hormonempfindlichkeit, Proliferation und Tumoraggressivität assoziiert sind und Informationen über das Rezidivrisiko geben. Einige diese Tests erlauben auch eine Abschätzung des Chemotherapienutzens bei Patienten unterschiedlicher Risikogruppen. Die ersten Multigentests wurden vor mehr als zehn Jahren entwickelt. Die ersten Studien zur Validierung waren retrospektiver Natur, nun liegen für einige Tests prospektiv erhobene Daten vor. Derzeit (Stand 2015) sind in Deutschland vier Tests kommerziell erhältlich (Mammaprint®, Oncotype DX®, Endopredict®, Prosigna®). Für Mammaprint® liegen aktuelle Daten der prospektiven Mindact-Studie vor.
Ziel der Mindact-Studie
Die Mindact-Studie (Microarray in Node-negative and 1 to 3 Positive Lymph Node Disease May Avoid Chemotherapy) ist mit knapp 7000 Brustkrebspatientinnen die größte europäische Studie zur Aussagekraft von Genexpressionstests beim frühen Mammakarzinom. Es handelt sich um einen Vergleich zwischen der klinischen Einschätzung des Risikos und der Einschätzung anhand des Genexpressionsprofils im Tumorgewebe der betroffenen Patientinnen. Ausgewählt wurden diejenigen Frauen, bei denen eine diskordante Einschätzung vorlag. Das heißt, der Kliniker stufte das Risiko für ein Fortschreiten der Erkrankung hoch ein, der Genexpressionstest gering. Ein Teil der Frauen aus dieser Diskordanz-Gruppe erhielt eine Chemotherapie, der andere nicht. Anschließend wurden die Überlebensraten verglichen. Das im Vorfeld definierte Ziel war eine Überlebensrate von 92%.
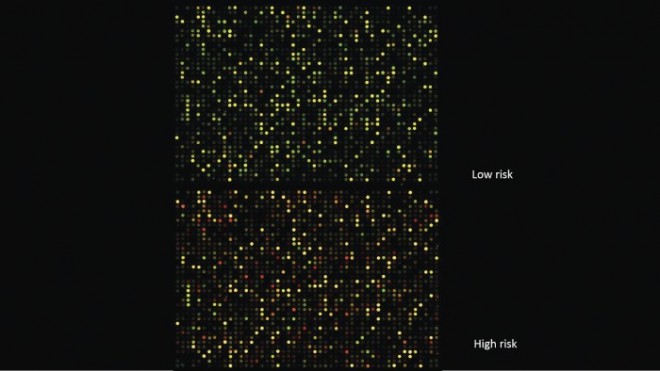
Für die zwischen 2007 und 2011 durchgeführte multizentrische, multinationale, prospektive Studien wurden 6693 Frauen mit einer frühen Brustkrebserkrankung (Befall von weniger als drei Lymphknoten) ausgewählt. Ihr Risiko für das Fortschreiten der Erkrankung wurde klinisch und pathologisch sowie mithilfe eines Genexpressionstests (Mammaprint®; erfasst 70 relevante Gene) bestimmt. Wenn die Ergebnisse beider Methoden auf ein hohes Risiko hinwiesen, wurde den Frauen zu einer Chemotherapie geraten, zeigten beide Methoden ein geringes Risiko auf, wurde von einer Chemotherapie abgeraten. Lagen diskordante Ergebnisse vor – hohes klinisches und geringes genomisches Risiko – wurden die Probandinnen auf zwei Gruppen randomisiert, was bei 1550 Patientinnen der Fall war. Studienendpunkt war das Fünf-Jahres-Überleben ohne Fernmetastasen.
Nur geringe Unterschiede
94,4% der Frauen mit hohem klinischem und geringem genomischem Risiko, die keine Chemotherapie erhalten hatten, waren nach fünf Jahren noch am Leben, ohne Fernmetastasen entwickelt zu haben. Im Vergleich dazu waren es 95,9% der Frauen, die chemotherapeutisch behandelt worden waren. Das entspricht einem nicht-signifikanten Unterschied von 1,5% (p = 0,27). Auch im Hinblick auf weitere Studienendpunkte waren die Unterschiede gering: Der Verzicht auf eine Chemotherapie verringerte das rezidivfreie Überleben um 2,8%, das Gesamtüberleben um 1,4%.
Klinische Auswirkungen
In einem Editorial wird auf die unterschiedliche Interpretation des geringfügigen Unterschieds von 1,5% hingewiesen. Einige betroffene Frauen könnten in ihm eine zu vernachlässigende Größe sehen, andere würden sich für eine Chemotherapie entscheiden, um keine Chance ungenutzt zu lassen. In der klinischen Praxis könnte der Test dazu beitragen, Übertherapien mit den damit verbundenen Toxizitäten zu vermeiden. |
Quelle
Cardoso F et al. 70-gene signature as an aid to treatment decisions in early-stage breast cancer. N Engl J Med 2016;375:717-29
Hudis C et al. Increasing precision in adjuvant therapy für breast cancer. N Engl J Med 2016;375:790-791
Harbeck N et al. Prädiktive Gensignaturen. Wie valide sind sie? Forum 2015;30:134-138





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.