
- DAZ.online
- DAZ / AZ
- DAZ 11/2015
- Silberner Schutz
Wundversorgung
Silberner Schutz
Silberhaltige Wundauflagen fördern die Wundheilung
Aufbau und Zusammensetzung
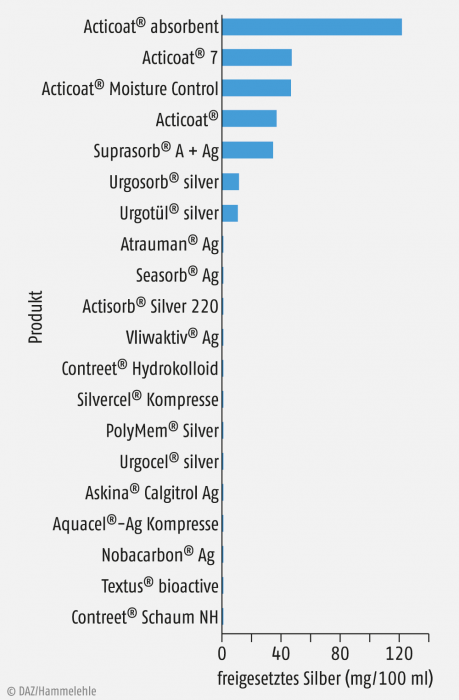
Je nach Hersteller und Produkt sind silberhaltige Wundauflagen sehr unterschiedlich aufgebaut. Sie variieren sowohl im Typ der Wundauflage als auch in der Art der Silbertechnologie und der damit verbundenen Silberfreisetzung. In den entsprechenden Verbänden liegt Silber entweder in elementarer Form (z. B. Silber-Metall, nanokristallines Silber) vor, als anorganische Verbindung (z. B. Silberoxid, Silberphosphat, Silberchlorid, Silbersulfat, Silber-Calcium-Natriumphosphat, Silber-Zirkonium-Verbindung) oder als organischer Komplex (z. B. Silber-Zinkallantoinat, Silberalginat, Silbercarboxymethylcellulose) [1]. Dabei wird der jeweilige Silberbestandteil als Beschichtung auf eine oder beide Außenseiten des Verbands aufgebracht oder aber in die Verbandsstruktur eingebettet. Der Silber-Gehalt in Verbänden differiert erheblich [2]. Je nach Produkt wird eine unterschiedliche Menge von Silber-Ionen an die Wunde abgegeben (siehe Grafik „Freisetzung von Silber-Ionen“) [3, 4].
Wirkungsweise von Silber
In elementarer Form ist Silber nicht reaktionsfähig. Um bakterizid wirken zu können, muss eine Reihe von silberhaltigen Wundauflagen vor der Anwendung erst mit Wasser aktiviert und damit das elementare Silber in seine ionische, wirksame Form gebracht werden [1]. In anorganischen Silberverbindungen sowie in organischen Komplexen liegen bereits Silber-Ionen vor, die sich beim Kontakt mit dem Wundsekret aus der Verbindung lösen und gegen ein breites Spektrum pathogener Keime wirken: gegen grampositive und gramnegative Bakterien [6] – auch gegen resistente Bakterien wie Meticillin-resistente Staphylococcus aureus (MRSA) und Vancomycin-resistente Enterococcen (VRE) [7] – sowie gegen Pilze und Viren.
Silber-Ionen haben mehrere antimikrobielle Wirkungsorte auf den Zielzellen und sind deshalb im Gegensatz zu Antibiotika mit einem geringen Risiko für Bakterienresistenz behaftet. Sie binden an bakterielle Zellmembranen, schädigen die Struktur der Zellwand und führen zu Zellleckage. In die Zelle transportierte Silber-Ionen stören die DNA und RNA der Bakterien und somit die Proteinproduktion und die Zellreplikation [8]. Darüber hinaus haben Laborversuche ergeben, dass Silber die Empfindlichkeit von Bakterien gegenüber Antibiotika erhöht und dass einige silberhaltige Verbände auch weitere vorteilhafte Wirkungen auf die Wundheilung zeigen, indem sie Entzündungen hemmen und die Neovaskularisierung fördern [1].
Einsatzgebiet von silberhaltigen Wundauflagen
Klinische Leitlinien empfehlen die Anwendung von Silberverbänden bei infizierten und infektionsgefährdeten Wunden wie Dekubitalgeschwüren, Ulcus cruris, diabetischem Fußsyndrom, ebenso bei Verbrennungswunden und transplantierter Haut. Produkte mit Aktivkohle sind zudem für unangenehme Wundgerüche indiziert, z. B. in der Palliativmedizin für aufbrechende Karzinome. Nicht verwendet werden sollten Silberverbände hingegen bei sauberen Operationswunden sowie bei kleinen akuten Wunden mit geringem Infektionsrisiko, bei Patienten, die empfindlich auf Bestandteile der Wundauflage oder den Wirkstoff reagieren, bei Wunden unter enzymatischen Débridement und nicht während der Schwangerschaft oder in der Stillzeit [1].
Anwendungshinweise für die Praxis
Bei infizierten Wunden sollte der Verband zunächst zwei Wochen eingesetzt werden, wobei bei Kindern und auf sehr großen Wunden Vorsicht geboten ist. Unbedingt sind die Anweisungen des Herstellers zu beachten bezüglich Indikationen, Kontraindikationen, Anwendungsmethode, Wundreinigungsverfahren und eventuell notwendiger Anfeuchtung des Verbands vor Applikation. Einige Firmen raten von der Anwendung von Silberverbänden ab bei Magnetresonanztomografien sowie auf oder in der Nähe von Körperstellen, die mit Strahlentherapie behandelt werden. Zum Teil sind die Produkte auch nicht kompatibel mit Präparaten auf Ölbasis wie Paraffin.
Kriterien für die Wahl eines Silberverbandes
In der Praxis sollte die Auswahl einer silberhaltigen Wundauflage durch die folgenden Faktoren beeinflusst werden [1]:
- Anforderung der Wunde: gute Absorptionsfähigkeit für eine große Exsudatmenge; erhöhte Anpassbarkeit des Verbands bei einem unregelmäßigen Wundbett
- Bedürfnisse des Patienten: geringe Haftung für schmerzfreien Verbandswechsel; Aktivkohle gegen Geruchsbildung
- Dauer der Silberfreisetzung: möglichst über mehrere Tage anhaltende Abgabe von Silber, um die Notwendigkeit für häufige Verbandswechsel zu reduzieren
- klinische Nachweise und Kosteneffizienz.
Studienlage zu silberhaltigen Verbänden
Silberverbände wurden in vielen unterschiedlichen Studienarten an einer Reihe von akuten und chronischen Wunden untersucht. Einige Studien fanden positive Wirkungen von Silberverbänden auf die Wundheilungsparameter, während andere keine signifikanten Unterschiede zu den Vergleichsprodukten ergaben. Schwierigkeiten bei der Interpretation und dem Vergleich von Studien entstanden aufgrund der oft nur kleinen Patientenzahl sowie der großen Vielfalt an unterschiedlichen Einschlusskriterien, Studienprotokollen und verwendeten Endpunkten [1]. Im Rahmen der Literaturrecherche der S3-Leitlinie „Lokaltherapie chronischer Wunden bei den Risiken CVI, PAVK und Diabetes mellitus“ konnten keine signifikanten Studienergebnisse zum klinischen Nutzen oder Schaden von silberhaltigen Wundauflagen ermittelt werden [4].
Bei einem direkten Vergleich verschiedener Wundverbände fanden sich Abweichungen im Silbergehalt, der freigesetzten Silbermenge und im Umfang und Grad der antimikrobiellen Wirksamkeit [7, 9]. Eine Studie ergab keine Korrelation zwischen dem Silbergehalt oder der freigesetzten Silbermenge und der antimikrobiellen Wirksamkeit in einem Auflösungstest in vitro, was darauf hinweist, dass die Freisetzungsrate aus einem Verband kein Vorhersagefaktor für antimikrobielle Wirksamkeit ist [7]. Andere Studien kamen zu dem Schluss, dass der Silbergehalt zwar bedeutend ist, aber darüber hinaus viele weitere wichtige Faktoren die bakterizide Wirkung eines Wundverbandes beeinflussen, z. B. die Verteilung von Silber im Verband, die Abgabe von Silber-Ionen aus dem Verband und das Flüssigkeitsabsorptionsvermögen der jeweiligen Wundauflage [9, 10, 11].
| Typ der Wundauflage | Produktbeispiele |
|---|---|
| silberhaltige Auflage | Acticoat® (Smith & Nephew), Askina® Calgitrol®Ag (B. Braun), UrgoCel® Silver (Urgo)Cosmopor® (Hartmann) |
| silberhaltiger Polyurethanschaum | Acticoat® Moisture Control und AllevynAg (Smith & Nephew), Biatain® Ag (Coloplast), Mepilex® Ag (Mölnlycke Healthcare), PolyMem Silver™ (mediSet GmbH) |
| Silberalginat | 3M™ Tegaderm™ Alginate Ag (3 M Medica), Acticoat® Absorbent (Smith & Nephew), Algisite® Ag (Smith & Nephew), Sea-Sorb-Ag® (Coloplast), Silvercel®Hydroalginat (Johnson & Johnson), Supra-sorb® A + Ag (Lohmann & Rauscher), Urgosorb Silver (Urgo) |
| silberhaltige Aktivkohle | Actisorb® silver 220 (Johnson & Johnson), Vliwaktiv Ag (Lohmann & Rauscher) |
| silberhaltige Hydrofaser | Aquacel® Ag (ConvaTec), Textus® bioaktiv (biocell Biotechnologie mbH) |
| silberhaltige Kollagen-Wundauflage | Promogran® Prisma (Johnson & Johnson) |
| silberhaltige Wundgaze/Wunddistanzgitter | Atrauman® Ag (Hartmann), Urgotül Silver (Urgo) |
Nebenwirkungen
Elementares Silber bzw. Silber-Ionen sollen praktisch keine toxischen Wirkungen auf menschliche Zellen haben. Als wichtigste Nebenwirkung ist die Argyrie bekannt, eine Silbereinlagerung in die Haut, die sich als blaugraue Verfärbung bemerkbar macht [12]. Diese wird aber üblicherweise nicht durch Silberverbände ausgelöst, sondern eher durch die orale Aufnahme von hochdosierten Silberlösungen im Rahmen alternativer Heilverfahren [13, 14]. Lokale Hautveränderungen oder schwarze Flecken, die gelegentlich durch Silberverbände verursacht werden können, sind harmlos und reversibel [15, 16]. Die Auswirkung von Silber auf die Umwelt ist bisher noch nicht geklärt. Nur sehr geringe Mengen werden systemisch resorbiert [17]. Ob eine Akkumulation im menschlichen Körper erfolgt, ist noch strittig.
Silberauflagen in der Selbstmedikation
Auch kleinere alltägliche Wunden können infiziert sein. Aus diesem Grund verfügen die Hansaplast® MED Sensitive Pflaster über eine Wundauflage, die Silber-Ionen enthält, welche aktiv freigesetzt werden, sobald sie mit der Wunde in Kontakt kommen. Sie schützen die Wunde nicht nur vor Verunreinigungen, Druck und Stößen, sondern weisen zusätzlich eine antiseptische Wirkung auf und bieten damit einen Infektionsschutz. Hier stellt sich allerdings die Frage, ob derartige Wundverbände in der Selbstmedikation ihren berechtigten Platz beanspruchen, denn einerseits sollten infizierte Wunden unbedingt von einem Arzt begutachtet und behandelt werden, und andererseits dürften bei Bagatellverletzungen eine normale Wunddesinfektion und ein herkömmliches Pflaster ausreichen. Laut Expertenempfehlungen sollten Silberverbände in jedem Fall Wunden mit hoher Infektionsgefahr vorbehalten bleiben. |
| Hersteller/Vertreiber | Produktname | Verbandgruppe | auf dem Markt seit | MPG-Klasse | verschreibungspflichtig? | Maß (cm) | Art des Silbers | mg Ag+ pro 10 × 10 cm | Besteht KontraindikationSchwangerschaft/ Stillzeit? | Wundreinigung/Befeuchtung mit NaCl 0,9% möglich? | Eiweißfehlerbekannt? |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 3 M Medica | Tegaderm®Alginate Ag | Alginat mit Silber | 2008 | III | nein | 10 × 10 | Silber-Na-hydrogenzirkoniumphosphat | 7,5 | nein | ja | keine Angaben |
| Acelity | Actisorb® silver 220 | Silber-Aktivkohle | 2000 | III | nein | 10,5 × 10,5 | elementares Silber fest gebunden | 3,3 | nein, aber Anwendung wird nicht empfohlen | ja | keine Angaben |
| Acelity | Silvercel®Kompresse | Alginat mit Silber | 2005 | III | nein | 11 × 11 | elementares Silber | 111,3 | nein, aber Anwendung wird nicht empfohlen | ja | keine Angaben |
| Acelity | Silvercel®non-adherent | Alginat mit Silber | 2009 | III | nein | 11 × 11 | elementares Silber | 111,3 | nein, aber Anwendung wird nicht empfohlen | ja | keine Angaben |
| B. Braun Melsungen AG | Askina® Calgitrol Ag | Schaum mit Silberalginat | 2005 | III | nein | 10 × 10 | ionisches Silber/Silbernitrat (AgNO3) | 141 | nein | ja | keine Angaben |
| B. Braun Melsungen AG | Askina® Calgitrol, Silberalginat aus der Tube | Alginat mit Silber | 2012 | III | nein | 15 g | ionisches Silber | 180/15 g | nein | ja | keine Angaben |
| BioCELL-Ges. für Biotechnologie mbH | [Textus]®bioactiv | Aquafilament Technology® | 2005 | I s | nein | 10 × 10 | ionisches Silber (fest gebunden in PET/PEfaser) | 20 | nein | ja | keine Angaben |
| Coloplast GmbH | SeaSorb®-Ag Kompresse | Alginat mit Silber | 2006 | III | nein | 10 × 10 | Silber-Na-hydrogenzirkoniumphosphat | 8 | nein | ja | nein |
| Coloplast GmbH | Biatain® Silicone Ag | Schaum mit Silber | 2014 | III | nein | 10 × 10 | Silber-Na-hydrogenzirkoniumphosphat | 100 | nein | ja | nein1 |
| Coloplast GmbH | Biatain® Ag Schaum NH, Cavity | Schaum mit Silber | 2003 | III | nein | 10 × 10 | Silber-Na-hydrogenzirkoniumphosphat | 100 | nein | ja | nein1 |
| Coloplast GmbH | Physiotuell® Ag | Distanzgitter | 2009 | III | Ja | 10 × 10 | Silber-Sulfadiazin | 30 | nein | ja | nein |
| ConvaTec GmbH | Aquacel® Ag Kompresse | Hydrofaser mit Silber | 2003 | III | nein | 10 × 10 | ionisches Silber | 10,8 | nein | ja | keine Angaben |
| ConvaTec GmbH | Aquacel® Ag Foam | Schaum mit Silber | 2013 | III | nein | 10 × 10 | ionisches Silber | 12 | nein | ja | keine Angaben |
| ConvaTec GmbH | Aquacel® Ag+ Extra Kompresse | Hydrofaser mit Silber | 2012 | III | nein | 10 × 10 | ionisches Silber | 16,3 | nein | ja | keine Angaben |
| ConvaTec GmbH | Aquacel® Ag Extra Kompresse | Hydrofaser mit Silber | 2012 | III | nein | 10 × 10 | ionisches Silber | 16,3 | nein | ja | keine Angaben |
| Lohmann & Rauscher GmbH & Co. KG | Vliwaktiv® Ag Kompr./Tamp. | Silber-Aktivkohle | 2006 | II B | nein | 10 × 10 | elementares Silber | 3,6 | nein | ja | keine Angaben |
| Lohmann & Rauscher GmbH & Co. KG | Suprasorb® A+ Ag Kompresse | Alginat mit Silber | 2007 | III | nein | 10 × 10 | ionisches Silber | 30 | nein | ja | keine Angaben |
| Mediset Clinical Products GmbH | Polymem® Wic Silber | polymerer Membranverband | 2004 | IIB | nein | 8 × 8 | nanokristallines Silber | 11,9 | nein | ja | keine Angaben |
| Mediset Clinical Products GmbH | Polymem® Silber | polymerer Membranverband | 2004 | IIB | nein | 10 × 10 | nanokristallines Silber | 12,4 | nein | ja | keine Angaben |
| Mediset Clinical Products GmbH | Polymem® Max Silber | polymerer Membranverband | 2006 | IIB | nein | 10 × 10 | nanokristallines Silber | 19,8 | nein | ja | keine Angaben |
| Mölnlycke Health Care GmbH | Melgisorb® Ag | Alginat mit Silber | 2009 | III | nein | 10 × 10 | Silber-Na-hydrogenzirkoniumphosphat | 7,8 | nein | ja | keine Angaben |
| Mölnlycke Health Care GmbH | Mepilex® Ag | Schaum mit Silber | 2007 | III | nein | 10 × 10 | Silbersulfat | 120 | nein | ja | keine Angaben |
| Mölnlycke Health Care GmbH | Mepilex® Border Ag | Schaum mit Silber | 2011 | III | nein | 10 × 12,5 | Silbersulfat | 120 | nein | ja | keine Angaben |
| Mölnlycke Health Care GmbH | Mepilex® Transfer Ag | Wundkontaktauflage | 2014 | III | nein | 10 × 12,5 | Silbersulfat | 120 | nein | ja | keine Angaben |
| Noba-Verbandmittel Danz GmbH & Co. KG | Nobacarbon® Ag | Silber-Aktivkohle | 2005 | IIB | nein | 10 × 10 | elementares Silber, fest gebunden | 3,3 | nein | nicht empfohlen | keine Angaben |
| Paul Hartmann AG | Atrauman® Ag | Distanzgitter | 2004 | IIB | nein | 10 × 10 | metallisches Silber | 50 | nein | ja | keine Angaben |
| Smith & Nephew GmbH | Algisite® Ag Kompresse | Alginat mit Silber | 2007 | III | nein | 10 × 10 | Ionisches Silber | 22 | nein | ja | keine Angaben |
| Smith & Nephew GmbH | Allevyn® Silber Schaumverband | Schaum mit Silber | 2007 | III | nein | 9 × 11 | Silber-Sulfadizin | 65 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® | Auflage | 2001 | III | nein | 10 × 10 | nanokristallines Silber | 109 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® Flex 3 | Auflage | 2009 | III | nein | 10 × 10 | nanokristallines Silber | 117 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® Moisture control | Schaum mit Silber | 2006 | III | nein | 10 × 10 | nanokristallines Silber | 138 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® Flex 7 | Auflage | 2009 | III | nein | 10 × 12,5 | nanokristallines Silber | 143 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® Absorbent | Alginat mit Silber | 2004 | III | nein | 10 × 12,5 | nanokristallines Silber | 144 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Acticoat® 7 | Auflage | 2001 | III | nein | 10 × 12,5 | nanokristallines Silber | 164 | nein | nein, keine Kochsalzlösung vor Anwendung der Silberprodukte | keine Angaben |
| Smith & Nephew GmbH | Durafiber® Ag | Hydrofaser mit Silber | 2014 | III | nein | 10 × 10 | ionisches Silber | 20 | nein | ja | keine Angaben |
| Sorbion GmbH | sorbion® silver flex | Auflage | 2014 | III | nein | 10 × 10 | elementares Silber | 70 | nein, aber Anwendung nicht empfohlen | ja | keine Angaben |
| Urgo GmbH | Urgosorb® Silver | Alginat mit Silber | 2006 | III | nein | 10 × 10 | Silberzeolith | 7,75* (6-9,5) | nein | ja | keine Angaben |
| Urgo GmbH | UrgoTül® SAg | Distanzgitter/Wundgaze | 2006 | III | Ja | 10 × 12 | Silbersulfadiazin | 14 | Ja | ja | keine Angaben |
| Urgo GmbH | UrgoTül® Silver | Distanzgitter/Wundgaze | 2006 | III | nein | 10 × 12 | Silbersulfat | 35 | nein | ja | keine Angaben |
| Urgo GmbH | UrgoCell® Silver | Schaum mit Silber | 2006 | III | nein | 10 × 12 | Silbersulfat | 35 | nein | ja | keine Angaben |
| Urgo GmbH | UrgoCell® Ag Border | Schaum mit Silber | 2012 | III | nein | 13 × 13 | Silbersulfat | 35 | nein | ja | keine Angaben |
| Urgo GmbH | UrgoTül® Ag LiteBorder | Silberwundverband | 2012 | III | nein | 10 × 12 | Silbersulfat | 35 | nein | ja | keine Angaben |
* Mittelwert, 1 Braunwarth H, Brill FHH, Brill H. Bakteriostatische und bakterizide Wirksamkeit antimikrobieller Wundauflagen unter organischer Belastung. Wundmanagement 2012;6:266-269
| |||||||||||
Quelle
[1] Internationaler Konsens. Adäquate Anwendung von Silberverbänden bei Wunden. Konsens einer Expertengruppe. London: Wounds International, 2012. Download: www.woundsinternational.com.
[2] Thomas S, McCubbin P. An in vitro analysis of the antimicrobial properties of 10 silver-containing dressings. J Wound Care 2003;12(8):305-308
[3] www.jalomed.de/pd5/pdf/Silberhaltige-Wundauflagen.pdf; http://www.werner-sellmer.de
[4] www.awmf.org/leitlinien/detail/ll/091-001.html: S3-Leitlinie „Lokaltherapie chronischer Wunden bei den Risiken CVI, PAVK und Diabetes mellitus“
[5] Protz K. Pflegelexikon. Wundauflagen Teil 5, Wund-Management 2008;2(5):176-77
[6] Percival SL, Bowler P, Russell D. Bacterial resistance to silver in wound care.J Hosp Inf 2005;60:1-7
[7] Parsons D, Bowler PG, Myles V, Jones S. Silver antimicrobial dressings in wound management: a comparison of antibacterial, physical, and chemical characteristics. Wounds 2005;17(8):222-232
[8] Lansdown ABG. Silver I: its antibacterial properties and mechanism of action. J Wound Care 2002;11(4):125-130
[9] Thomas S, McCubbin P. An in vitro analysis of the antimicrobial properties of 10 silver-containing dressings. J Wound Care 2003;12(8):305-308
[10] Walker M, Jones S, Parsons D, et al. Evaluation of low-adherent antimicrobial dressings. Wounds UK 2011;7(2):32-45
[11] Cavanagh MH, Burrell RE, Nadworny PL. Evaluating antimicrobial efficacy of new commercially available silver dressings. Int Wound J 2010;7(5):394-405
[12] Vasel - Biergans A. Wundauflagen für die Kitteltasche. 3. Aufl. Wissenschaftliche erlagsgesellschaft Stuttgart, 2010
[13] Kwon HB, Lee JH, Lee SH et al. A case of argyria following colloidal silver ingestion. Ann Dermatol 2009;21(3):308-310
[14] Thompson R, Elliott V, Mondry A. Argyria: permanent skin discoloration following protracted colloid silver ingestion. BMJ Case Rep 2009
[15] Lansdown ABG. A pharmacological and toxicological profile of silver as an antimicrobial agent in medical devices. Adv Pharm Sci 2010;2010:910686
[16] Cutting K, White R, Edmonds M. The safety and efficacy of dressings with silver – addressing clincal concerns. Int Wound J 2007;4(2):177-184
[17] Wilkinson LJ, White RJ, Chipman JK. Silver and nanoparticles of silver in wound dressings: a review of efficacy and safety. J Wound Care 2011;20(11):543-549
Autorin
Ines Winterhagen hat in Marburg Pharmazie studiert und ist seit der Approbation 2003 in der öffentlichen Apotheke tätig. Sie ist Fachapothekerin für Offizinpharmazie, Homöopathie und Naturheilkunde. In der Reihe „Beratungspraxis“, die im Deutschen Apotheker Verlag erscheint, schrieb sie die Bücher „Neurodermitis“ und „Psoriasis“. Sie ist Referentin und Mitglied im Weiterbildungsausschuss der LAK Baden-Württemberg.



















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.