
- DAZ.online
- DAZ / AZ
- DAZ 48/2008
- HIV-Impfstoff-Forschung ...
AIDS
HIV-Impfstoff-Forschung von Rückschlägen gezeichnet
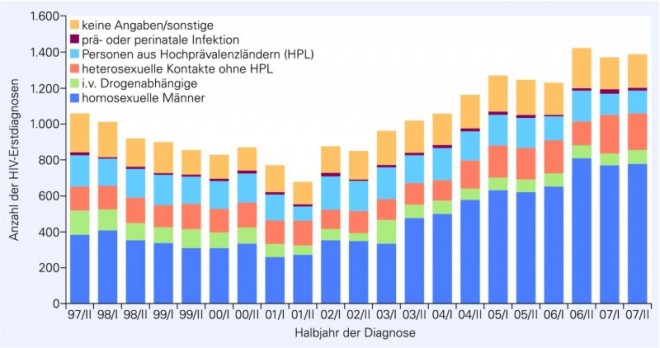
Das heute als AIDS bekannte Syndrom einer erworbenen Immunschwäche ist in der menschlichen Bevölkerung erstmals Mitte der 1980er Jahre aufgetreten. Nach Schätzungen der Weltgesundheitsorganisation WHO sind heute weltweit mehr als 39 Millionen Menschen mit dem Humanen Immunschwäche-Virus (HIV) infiziert. Weltweit kommen pro Jahr mehr als 4 Millionen Neuinfektionen dazu, wobei 95% der Betroffenen in Entwicklungsländern leben. Auch in Deutschland steigt die Zahl der Neudiagnosen HIV-Positiver wieder langsam, trotz Aufklärung: Das Robert-Koch-Institut meldet für das Jahr 2007 insgesamt 2752 neu diagnostizierte HIV-Infektionen, 4% mehr als 2006 (Abb. 1). Die Zahl der Neuinfektionen für 2008 wird auf 3000 geschätzt.
Vermeintlich beherrschbare Infektionskrankheit
Der Nobelpreis für Medizin 2008 wird am 10. Dezember an die Entdecker des HI-Virus als Ursache von AIDS, Françoise Barré-Sinoussi und Luc Montagnier, verliehen. Die Entdeckung des HI-Virus hat damals eine beispiellose weltweite Forschungsaktivität ausgelöst. Als Erfolg dieser Bemühungen gibt es heute in Form der hochaktiven antiretroviralen Therapie (HAART, highly active antiretroviral treatment) eine beachtliche Auswahl an Wirkstoffen, die die HIV-Virämie in infizierten Patienten nachhaltig unterdrücken und damit das Auftreten AIDS-definierender Symptome oft über viele Jahre hinauszögern können. Die HIV-Infektion ist – jedenfalls in den Industrieländern – zu einer zwar potenziell lebensbedrohlichen, aber oft als chronisch verlaufend wahrgenommenen und vermeintlich beherrschbaren Infektionskrankheit "herabgestuft" worden.
Neuinfektionen müssen zurückgedrängt werden
Die HAART löst jedoch nicht die weltweiten Probleme mit der HIV-Pandemie, nicht zuletzt auch deshalb, weil die antiretroviralen Wirkstoffe in den Entwicklungsländern gar nicht oder nur unzureichend zur Verfügung stehen. Deshalb wird es einen signifikanten Rückgang der HIV-Neuinfektionen in der Zunkunft möglicherweise nur geben, wenn es gelingt, eine effektive Vakzine zu entwickeln, die insbesondere den Menschen in den Hochrisikogebieten zur Verfügung gestellt werden kann. Bereits 1995 wurde eine internationale Interessengemeinschaft für die HIV-Impfstoff-Entwicklung gegründet (AVAC, AIDS Vaccine Advocacy Coalition; http://www.avac.org) und am 18. Mai 1997, dem Welt-AIDS-Impfstoff-Tag, rief Präsident Clinton zu einem weltweiten Engagement auf, innerhalb der nächsten 10 Jahre einen Impfstoff gegen AIDS zu entwickeln. Mittlerweile sind mehr als 50 Impfstoffkandidaten präklinisch oder klinisch getestet worden und keiner hat den gewünschten Erfolg gebracht.
Warum die Impfstoffentwicklung so schwierig ist
Der Nobelpreis für Medizin 2008 ging zur Hälfte auch an Harald zur Hausen, den Entdecker des humanen Papillomavirus (HPV). Während gegen HPV inzwischen zwei Impfstoffe zur Verfügung stehen, die vor der Ausbildung eines HPV-bedingten Gebärmutterhalskrebses schützen sollen – Gardasil® erhielt 2007 den PZ-Innovationspreis und wurde 2008 mit dem renommierten Prix Galien Suisse ausgezeichnet –, ist die jüngste Hoffnung auf einen baldigen Impfstoff gegen HIV begraben worden.
Obwohl praktisch jeder HIV-Infizierte Antikörper gegen das HI-Virus produziert, können diese Antikörper das Virus selten neutralisieren und somit eine Virämie und das Auftreten von AIDS verhindern. Ein wesentlicher Grund liegt darin, dass HIV ein RNA-Genom hat, das mit einer hohen Fehlerrate kopiert wird und ständig neue Virusvarianten mit veränderten Epitopen hervorbringt. Auch wenn die Mehrzahl der dabei entstehenden HI-Virusvarianten fehlerhaft und nicht infektiös ist, werden die verbliebenen Viren mit veränderten Epitopen mit hoher Wahrscheinlichkeit in der Lage sein, die Immunantwort des Infizierten zu unterlaufen. Das führt in der Regel sogar dazu, dass aus einem individuellen Patienten gewonnene Antikörper die HI-Viren aus anderen Patienten schlecht oder gar nicht erkennen.
Das andere Problem bei HIV liegt darin, dass das Virus genau die Zellen des Immunsystems, nämlich die T-Helferzellen, infiziert und schädigt, die für eine erfolgreiche Immunantwort nötig sind und bei einer Impfung normalerweise mit stimuliert werden müssen.
Ansätze für einen HIV-Impfstoff
Bei der Entwicklung eines Impfstoffes gegen HIV werden zwei Ziele verfolgt:
- die Verminderung der Zahl von Neuinfektionen,
- die Reduzierung der Viruslast in bereits infizierten Personen.
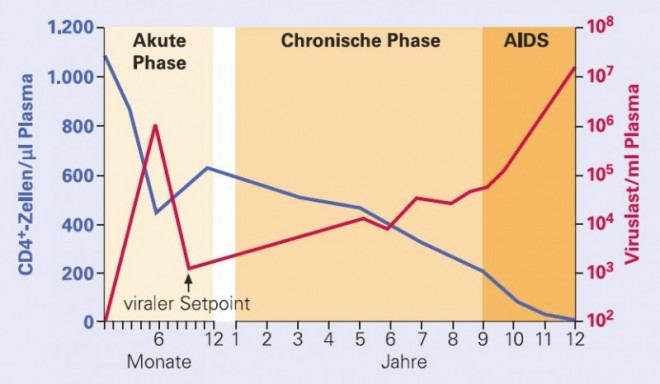
In der Therapie der HIV-Infektion ist die Viruslast (Kopien des Virusgenoms pro ml Blutplasma) ein bedeutender diagnostischer Parameter. Zu einem Zeitpunkt etwa vier bis sechs Monate nach einer Neuinfektion, wenn das Immunsystem in seiner ersten Reaktion die Virämie auf ein Minimum reduziert hat, spricht man von dem "viralen Setpoint" (Abb. 2). Der virale Setpoint kann einige Monate bis Jahre relativ stabil bleiben und ist einer der wichtigsten prognostischen Marker für den Verlauf der HIV-Infektion und das Fortschreiten der Krankheit zum Vollbild AIDS (Abb. 2). Seit längerer Zeit ist bekannt, dass eine effektive Kontrolle der HIV-Replikation durch das Immunsystem wesentlich von der Bildung zytotoxischer T-Zellen (CTL, cytotoxic T lymphocytes) und T-Helferzellen des Typs TH1 abhängt. Man geht davon aus, dass in einer infizierten Person die Senkung des viralen Setpoints durch einen Impfstoff um nur eine halbe Log-Stufe einen signifikanten klinischen Nutzen bringen würde. Das Erreichen dieses Ziels scheint davon abhängig zu sein, ob ein Impfstoff eine gegen HIV-Epitope gerichtete zytotoxische T-Zellantwort induzieren kann. Zur Induktion HIV-spezifischer CTL benötigt man demnach einen Impfstoff, der in der Lage ist, die HLA-Moleküle der Klasse I mit Peptiden aus den HIV-Proteinen zu beladen, so dass diese Epitope den CTL präsentiert werden können (Abb. 3). In der Folge würden die virusinfizierten Zellen durch die aktivierten CTL abgetötet werden.
Subunit-Impfstoffe waren ungeeignet
Ganz analog zu anderen Impfstoffen, wie gegen Hepatitis B, wurden große Phase-III-Studien wie die AIDS Vax Trials mit Subunit-Impfstoffen durchgeführt, die im Wesentlichen aus dem Hüllprotein gp120 des HI-Virus bestanden. Auch andere Proteine aus der äußeren Hülle wie gp160 oder gp41 wurden als Antigene in Impfstudien getestet. Allen diesen Studien ist gemeinsam, dass sie in gesunden Probanden aus Hochrisikogruppen zwar eine Bildung von Antikörpern (Serokonversion) verursacht haben, diese Antikörper jedoch letztlich nicht zu einer Senkung der Zahlen von Neuinfektionen geführt haben. Außerdem waren diese Vakzine ungeeignet, in bereits infizierten Personen die Viruslast nachhaltig zu senken und damit den Krankheitsverlauf positiv zu beeinflussen.
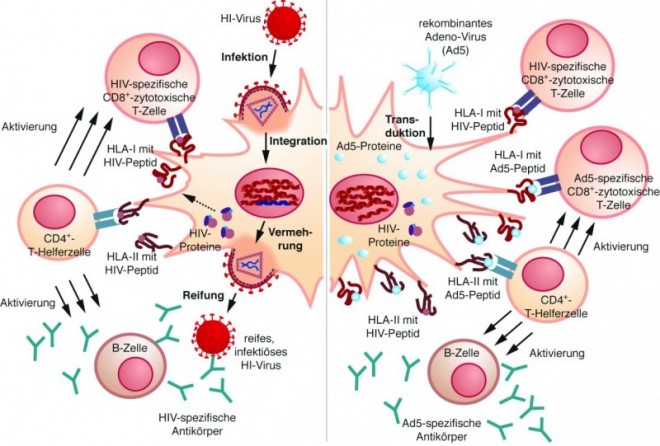
Subunit-Impfstoffe scheinen nicht in der Lage zu sein, eine ausreichende HIV-spezifische T-Zell-Antwort zu generieren. Die logische Konsequenz wäre demnach der Einsatz eines Lebend-Impfstoffes. Allerdings verbietet sich die Nutzung lebender, attenuierter HI-Viren als Vakzine aus Sicherheitsgründen. Deshalb war die Überlegung folgerichtig, ein attenuiertes Impfvirus als "Vehikel" mit HIV-Epitopen zu beladen und damit eine T-Zell-abhängige Immunreaktion des Patienten auf das Vehikel-Virus und gleichzeitig auch gegen die HIV-Epitope zu induzieren (Abb. 3).
Versuch mit attenuiertem Impfstoff: Die STEP-Studie
Ein internationales Konsortium, bestehend aus dem National Institute of Allergy and Infectious Diseases (NIAID), dem HIV Vaccine Trials Network (HVTN) und dem Pharmakonzern Merck hatte im Dezember 2004 eine breit angelegte Studie (STEP) mit einem neuen HIV-Impfstoff-Konzept aufgelegt. In dem eingesetzten Impfstoff V520 (auch bekannt als MRKAd5) der Firma Merck wurde eine Mischung rekombinanter, replikationsunfähiger Typ-5-Adenoviren (Ad5) verwendet, die die relativ konservierten HIV-Proteine GAG, POL oder Nef exprimierten. Adenovirus-5-basierte Vakzine gehören zu den immunogensten Impfstoffen, die sehr effizient eine Zell-vermittelte Immunität induzieren. Wahrscheinlich werden derartige Adenovektoren trotz des Fehlens viraler Transkriptions-Aktivatoren in geringem Umfang in den transduzierten Zellen exprimiert. Ein in Ad5 identifiziertes, immundominantes Epitop kann dann sehr effizient auf HLA-I-Molekülen von Dentritischen Zellen präsentiert werden und Adenovirus-spezifische CTL aktivieren. Ungefähr zwei Drittel der Erwachsenen in Nordamerika und Westeuropa haben bereits als Kind eine Ad5-vermittelte Infektion des Respirationstrakts durchgemacht und sind Ad5-seropositiv.
STEP (HVTN 502) war eine multizentrische, doppelblinde, placebokontrollierte Phase-IIb-Studie. Rekrutiert wurden 3000 HIV-negative Freiwillige im Alter zwischen 18 und 45 Jahren aus Nord- und Südamerika, der Karibik und Australien, die zu Hochrisikogruppen bezüglich der Infektion mit HIV gerechnet wurden. Ursprünglich war geplant, nur Probanden zu rekrutieren, die einen geringen Antikörpertiter gegen Ad5 hatten (≤ 200 Einheiten), da von diesen eine bessere, gegen HIV gerichtete Immunantwort erwartet wurde als von Probanden mit hohem Antikörpertiter, in denen die Vakzine möglicherweise zu schnell neutralisiert werden würde. Von diesem Rekrutierungsplan wurde allerdings abgewichen, weil man zwischenzeitlich Daten gewonnen hatte, die zeigten, dass der Impfstoff auch in Probanden mit hohem Ad5-Titer eine Serokonversion bewirkte.
Warum die Step-Studiegestoppt wurde
Primäre Endpunkte der Studie waren die Verhinderung von Neuinfektionen und/oder die Reduktion der Viruslast in solchen Probanden, die während der Laufzeit der Studie neu mit HIV infiziert wurden. Nach einer routinemäßigen Zwischenauswertung eines Teils des Probanden-Kollektivs wurde nun die Studie wegen der offensichtlichen Unwirksamkeit des Impfstoffes gestoppt. Bislang wurden die Daten von ca. 1500 Studienteilnehmern ausgewertet. Von 741 mit der Vakzine behandelten Personen wurden in der Studienperiode 24 mit HIV infiziert, in der Placebo-Gruppe waren es 21 von 762. Leider waren auch die Virustiter in den infizierten Probanden beider Studiengruppen vergleichbar: Etwa acht bis zwölf Wochen nach der Erstdiagnose hatten die Infizierten der Vakzine-Gruppe eine Viruslast von 40.000/ml Blut verglichen mit 37.000/ml in der Vergleichsgruppe.
Höhere Infektionsrate durch Impfung?
In einer Post-hoc-Analyse der Daten wurde ein Trend zur Korrelation der Antikörpertiter gegen Ad5 und der Effektivität des Impfstoffes festgestellt: Bei insgesamt 941 männlichen Studienteilnehmern wurden 49 Neuinfektionen in der Impfstoffgruppe festgestellt, gegenüber 33 Neuinfektionen in der Placebogruppe (n = 922). Eine Subgruppen-Analyse erbrachte das Ergebnis, dass unter den Probanden der Verum-Gruppe mit Ad5-Antikörpertitern > 200 Einheiten 22 Neuinfektionen auftraten, gegenüber neun Neuinfektionen in der Kontrollgruppe.
Es scheint unlogisch zu sein, dass ein Impfstoff, der eine Infektion eigentlich verhindern soll, diese sogar zu fördern scheint. Wie könnte man das immunologisch erklären?
Eine mögliche Antwort liegt in der Art und Weise, wie T-Zellen aktiviert werden. Dendritische Zellen (DC) sind die wichtigsten Regulatoren einer potenten T-Zell-Antwort, da sie Antigene aufnehmen, zu Peptiden prozessieren und diese Peptide sowohl über HLA-I- als auch HLA-II-Moleküle den T-Zellen präsentieren. Antigen-Präsentation über HLA-I aktiviert CD8-positive CTL, während die CD4-positiven T-Helferzellen durch Präsentation von Antigenen über HLA-II aktiviert werden.
In der STEP-Studie entstanden in Probanden mit hohen Antikörper-Titern gegen Ad5 vermehrt Immunkomplexe mit dem MRKAd5-Impfstoff, die von DC aufgenommen werden können. Ausgereifte DC präsentieren dann sowohl Ad5-Antigene als auch HIV-Antigene, und zwar in einem höheren Ausmaß als in Ad5-seronegativen Personen. Durch die vermehrte Aufnahme von Ad5-Immunkomplexen durch DC in Probanden mit hohen Ad5-Antikörper-Titern entsteht eine vergleichsweise größere Population von aktivierten DC, die gleichzeitig Ad5- und HIV-Epitope präsentieren. Dies aktiviert CTL mit Spezifität für Ad5- oder HIV-Epitope, allerdings werden wesentlich mehr Ad5- als HIV-spezifische CTL gebildet (Abb. 3). Dies könnte die Ausbildung HIV-spezifischer CTL unterdrücken, weil die DC selbst zum Ziel der Ad5-spezifischen CTL werden, so dass der DC-Pool und damit die Präsentation von HIV-Epitopen und damit letztlich die Effektivität des Impfstoffes vermindert wird. Und schließlich werden durch die Impfung Ad5-spezifische CD4-positive Gedächtnis-T-Helferzellen mobilisiert, die wiederum einer Infektion durch und einer Vermehrung von HIV zur Verfügung stehen.
Erfolge durch kombinierte Stimulierung?
STEP ist leider nicht die erste negativ verlaufende HIV-Impfstudie. Allerdings ist der Ausgang dieser Studie besonders enttäuschend, weil unter den Experten von dem Impfkonzept, gezielt die T-Zell-Antwort zu stimulieren ein Durchbruch in der Suche nach effektiven HIV-Impfstoffen erhofft und auch erwartet wurde. Unglücklicherweise hat sich bei dieser Studie auch gezeigt, dass die Aussagekraft der vorangegangenen Studien an Primaten eher schlecht ist. Dennoch hoffen die Autoren der Studie, dass die sorgfältige Analyse der Studiendaten neue Wege aufzeigen wird, T-Zell-Pools mit Spezifität für HIV-Epitope zu generieren und dadurch einen wirksamen HIV-Impfstoff zu gewinnen. Immerhin ist jetzt wirklich klar, dass man nicht einfach Impfkonzepte, die bei anderen Viren funktionieren, an HIV anpassen kann und dass man nicht nur die humorale (Antikörper) oder nur die zelluläre (T-Zellen) Schiene des spezifischen Immunsystems adressieren darf. Ein Schritt in die Richtung einer kombinierten Stimulierung ist das Konzept der "prime-boost"-Immunisierung, bei der die Antigene während des Immunisierungsschemas gewechselt werden, beispielsweise von einer DNA-Vakzine mit viralen Genen hin zu rekombinanten Virusvektoren, die die Virusproteine exprimieren.
Sicherlich muss aber noch einmal genau überprüft werden, wie es die Immunsysteme der Langzeit-HIV-Positiven schaffen, die Viruslast "in Schach" zu halten, um daraus eventuell Strategien für eine erfolgreiche Impfstrategie zu entwickeln. Und sicherlich muss zukünftig auch genauer darauf geachtet werden, wie der Immunstatus von Studienteilnehmern ist, um so unangenehme Überraschungen, wie z. B. Ad5-Immunkomplexe zu vermeiden. Mit mehr Wissen um die Zusammenhänge in unserem komplizierten Immunsystem müsste es dann auch möglich sein, einen schützenden Impfstoff gegen HIV zu entwickeln.
Literatur: Bruce D et al.: Toward an AIDS Vaccine. Science 320 (2008); 760–764. Perreau M et al.: Activation of a dendritic cell – T cell axis by Ad5 immune complexes creates an improved environment for replication of HIV in T cells. J Exp Med. 2008 Online-Publikation 3. November 2008. Buchbinder SP et al. and the Step Study Protocol Team: Efficacy assessment of a cell-mediated immunity HIV-1 vaccine (the Step Study): a double-blind, randomised, placebo-controlled, test-of-concept trial. Lancet 2008; Online-Publikation, 13. November 2008 McElrath MJ et al. and the Step Study Protocol Team: HIV-1 vaccine-induced immunity in the test-of-concept Step Study: a case–cohort analysis. Lancet 2008; Online-Publikation 13. November 2008.
Autoren:Prof. Dr. Thomas WincklerUniversität JenaInstitut für PharmazieLehrstuhl für Pharmazeutische BiologieSemmelweisstraße 1007743 JenaDr. Ilse Zündorf, Prof. Dr. Theo DingermannUniversität FrankfurtInstitut für Pharmazeutische BiologieBiozentrumMax-von-Laue-Str.60438 Frankfurt am Main
Glossar
AIDS-definierende Symptome
Die Einteilung der klinischen Manifestationen der HIV-Infektion folgt folgenden Kriterien:
Attenuierte Impfviren Aus humanpathogenen Viren kann durch wiederholtes Passagieren auf Zellkulturzellen und die nachfolgende Suche nach weniger virulenten Stämmen ein Impfstamm gewonnen werden, der zwar noch infektiös ist, aber keine Krankheitssymptome verursacht (Lebendvakzine) CTL – zytotoxische T-Lymphozyten CD8-positive, zytotoxische T-Zellen; verantwortlich für die Lyse von (Körper-)Zellen, die ein für die CTL-spezifisches Epitop über HLA-I präsentieren (insbesondere virusinfizierte Zellen) DC – Dendritische Zellen Professionelle antigenpräsentierende Zellen, die Antigene aufnehmen, in Peptide aufspalten und sie über HLA-I- oder HLA-II-Moleküle präsentieren HAART Hochaktive antivirale Therapie; eine Therapie der HIV-Infektion mit einer Kombination aus mindestens drei Wirkstoffen, von denen mindestens einer nicht aus der Gruppe der nukleosidischen Reverse-Transkriptase-Inhibitoren stammt HLA – Human leukocyte antigen Haupt-Histokompatibilitäts-Antigen; Membranproteine, die für die Gewebeverträglichkeit (Histokompatibilität) bei Transplantationen und für die immunologische Individualität wichtig sind; Körperzellen besitzen in der Regel nur HLA-I-Moleküle, während Zellen des Immunsystems HLA-I- und HLA-II-Moleküle exprimieren. Über HLA-Moleküle werden aus Antigenen hergestellte Peptide präsentiert, was zur Aktivierung von CD8-positiven T-Zellen (HLA-I) oder CD4-positiven T-Zellen (HLA-II) führen kann. Pandemie Länder- und Kontinent-übergreifende (Infektions-)Krankheit Transduktion Infektion einer Zelle mit einem replikationsunfähigen Virus, d. h. das Virus kann in die Zelle eindringen, aber es werden keine neuen Viruspartikel gebildet Viraler Setpoint Minimale HIV-Viruslast nach der initialen Virämie nach Neuinfektion; Gleichgewicht aus stattfindender Virus-Replikation und Elimination von Viren durch das Immunsystem Viruslast Anzahl von Viren bzw. Virusgenomen pro ml Blutplasma |


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.