
- DAZ.online
- DAZ / AZ
- DAZ 10/2008
- Essenzielle Fettsäuren ...
Nahrungsergänzung
Essenzielle Fettsäuren und Hirnfunktion bei Kindern
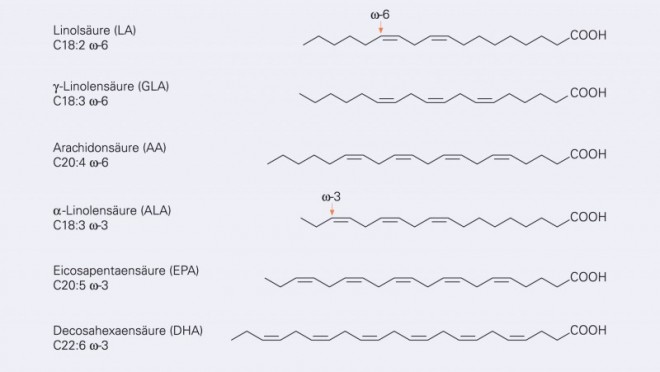
Aus ernährungsphysiologischer Sicht werden mehrfach ungesättigte Fettsäuren (Polyenfettsäuren, Polyunsaturated fatty acids, PUFAs), abweichend von der rationalen chemischen Nomenklatur, nach der Position der ersten Doppelbindung ab dem Methylende (Omega-Ende) klassifiziert:
ω-3-Fettsäuren wie α-Linolensäure (ALA, C18:3 ω-3) und ihre längerkettigen Derivate Eicosapentaensäure (EPA, C20:5 ω-3) und Docosahexaensäure (DHA, C22:6 ω-3) weisen ihre erste Doppelbindung am dritten Kohlenstoffatom auf (Abb. 1).
Bei ω-6-Fettsäuren befindet sich die erste Doppelbindung hingegen an sechster Position; bekannteste Vertreter sind hier Linolsäure (LA, C18:2 ω-6), γ-Linolensäure (GLA, C18:3 ω-6) sowie Arachidonsäure (AA, C20:4 ω-6).
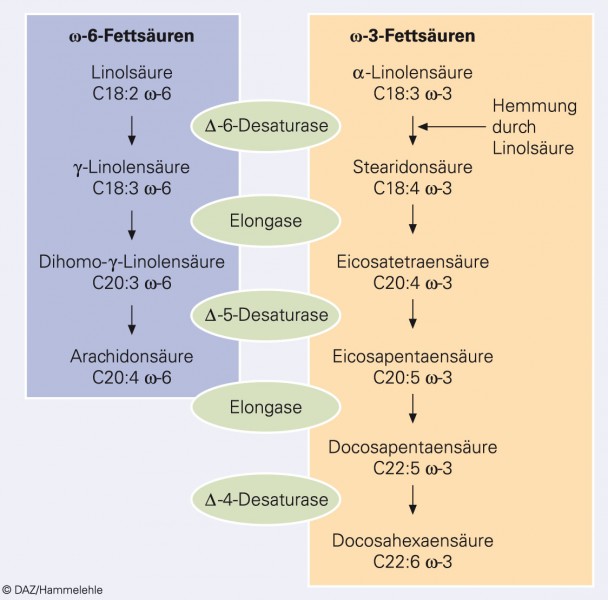
Säugetiere sind im Gegensatz zu Pflanzen nicht zur De-novo-Synthese der Stammverbindungen beider Fettsäurenfamilien, der ω-6-Fettsäure LA sowie der ω-3-Fettsäure ALA, befähigt. LA und ALA sind damit für den Menschen essenzielle Nährstoffe. Anders verhält es sich mit den längerkettigen Derivaten dieser Fettsäuren, insbesondere der ω-6-Fettsäure AA und den ω-3-Fettsäuren EPA und DHA. Säugetiere können sie in einem vielstufigen Konversionsprozess, der vornehmlich im endoplasmatischen Retikulum der Leberzellen abläuft, aus LA bzw. ALA bilden (Abb. 2). Obwohl ω-3-Fettsäuren die größere Affinität zu den entsprechenden Enzymsystemen aufweisen, erfolgt die Synthese von EPA und DHA aus ALA nur in einem geringen Ausmaß, denn sie wird durch die – bei der heutigen Ernährungsweise in großen Mengen, vor allem in Form von Fleisch- und Wurstwaren, zugeführte – LA kompetitiv gehemmt (Pawlosky et al., 2001; Salem et al., 1999). So müssten etwa 20 g ALA zugeführt werden, um 1 g EPA zu erhalten. Vor diesem Hintergrund wird zunehmend diskutiert, dass auch EPA und DHA mit der Nahrung zugeführt werden müssen.
Allgemeine physiologische Bedeutung von ω-3-Fettsäuren
ω-3-Fettsäuren besitzen vielfältige physiologische Funktionen (s. Kasten) und agieren über verschiedene Wirkmechanismen. So sind sie gemeinsam mit ω-6-Fettsäuren integrale Bestandteile jeder Zellmembran und beeinflussen dort nicht nur Stabilität und Flüssigkeitsversorgung der Membranen, sondern sind auch in die Regulation von Ionenkanälen eingebunden. Zudem modulieren ω-3-Fettsäuren die Endo- und Exozytose sowie die hormonelle und immunologische Aktivität (Drevon, 1992; Simopoulos, 1999). Wie experimentelle Studien der letzten Jahre gezeigt haben, reicht die Wirkung von ω-3-Fettsäuren dabei bis auf die Ebene der Genexpression (Jump, 2002). Aufgrund ihrer genregulatorischen Wirkung ist insbesondere DHA für die Entwicklung des Fötus und Säuglings von essenzieller Bedeutung (Uauy et al., 2001; Metz, 2000).
Physiologische Rolle von ω-3-Fettsäuren
|
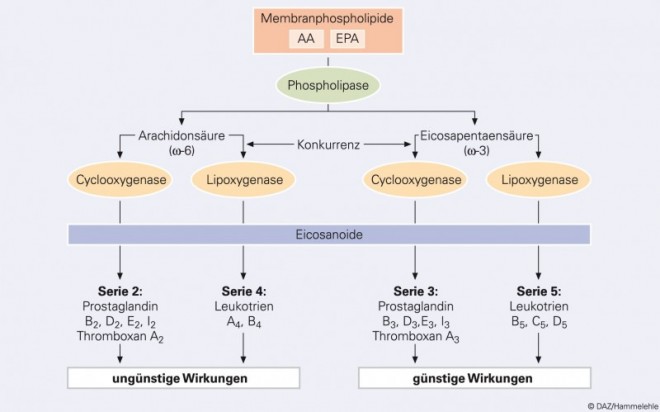
Eine wesentliche ernährungsphysiologische Bedeutung der ω-3-Fettsäure EPA beruht auf ihrer Funktion als Vorläufersubstanz bestimmter Eicosanoide (griech. eikosi = 20). Es sind Prostaglandine, Thromboxane und Leukotriene, die als lokale Mediatoren fungieren und durch ihre hormonähnliche Wirkung bereits in sehr geringen Konzentrationen zahlreiche Stoffwechselprozesse beeinflussen. EPA wird – ebenso wie die ω-6-Fettsäure AA – aus den Phospholipiden der Zellmembranen durch das Enzym Phospholipase A2 freigesetzt. In Abhängigkeit von der Enzymausstattung der jeweiligen Zelle (z. B. Thrombozyt, Leukozyt oder Endothelzelle) wird sie anschließend unter der katalytischen Einwirkung der Cyclooxygenase oder von Lipoxygenasen verstoffwechselt. Hierbei konkurriert EPA mit AA um dieselben Enzymsysteme (Abb. 2; Ströhle et al., 2002). Aus EPA und AA entstehen Eicosanoide verschiedener Serien, die sich in ihren Wirkspektren erheblich voneinander unterscheiden. Im Allgemeinen sind die aus EPA gebildeten Eicosanoide (Serie 3 und 5) mit günstigeren Wirkungen behaftet als solche, die aus AA gebildet werden (Serie 2 und 4). Welche Eicosanoide in welchen Mengen gebildet werden, hängt vom Angebot der jeweiligen Vorstufen in der Nahrung ab. Daher ist es möglich, physiologische Prozesse, die durch Eicosanoide gesteuert werden, diätetisch zu beeinflussen (Ströhle et al., 2002).
ω-3-Fettsäuren in der Zerebralisierungsphase
Der Einfluss von ω-3-Fettsäuren auf die Entwicklung und Funktion des Nervengewebes ergibt sich durch ihre Beteiligung an zahlreichen Prozessen (Tab. 1). Während diese in einigen Fällen schon lange bekannt ist, wurde sie in anderen Bereichen erst in jüngerer Vergangenheit deutlich.
Tab. 1: Wirkung von ω-3-Fettsäuren auf neuronale Phänomene und Vorgänge (nach Freeman et al., 2006) | |
Wirkung |
Autoren |
Gehirnentwicklung |
Wainright 2002; Uauy et al., 2001 und 2006 |
Entwicklung des Sehvermögens |
Neuringer et al., 1994; Uauy et al., 2001 |
Bestandteil der neuronalen Membranphospholipide |
Bourre et al., 1991; Yehuda et al., 1998; Lee, 2001 |
Wirkungen auf Neurotransmittersysteme |
Kodas et al., 2004; Hibbeln et al., 1998; Zimmer et al., 1998 und 2002; Bourre et al., 1993; Delion et al., 1994; Kinsella, 1990 |
Regulation des Corticotropin-Releasing-Hormons |
Hibbeln et al., 2004 |
Inhibition von Proteinkinasen |
Mirnikjoo et al., 2001; Kim et al., 2001 |
Modulation der Herzfrequenzvariabilität über den vagalen Mechanismus |
Villa et al., 2002 |
Verbesserte zerebrale Durchblutung und Sauerstoffversorgung |
Tsukada et al., 2000 |
Verhinderung der neuronalen Apoptose |
Kim et al., 2001 und 2003 |
Einfluss auf den Energiewechsel |
Ximenes da Silva et al., 2002 |
Einfluss auf das Neuritenwachstum |
Calderon und Kim, 2004; Ikemoto et al., 1997 |
Regulation der Genexpression |
Wainwright, 2002; Kitajka et al., 2002; Barcelo-Cobljin et al., 2003 |
Antiinflammatorische Effekte |
Calder, 1997; Meydani et al., 1991 und 1993; Kelley et al., 1999; Mamalakis et al., 2004; Simopoulos et al., |
Ab Beginn des 3. Trimenons (25. Schwangerschaftswoche) ist der Fötus auf die ausreichende Versorgung mit EPA und DHA, aber auch mit den ω-6-Fettsäuren AA und Dihomo-γ-Linolensäure angewiesen, da nun die Entwicklung des ZNS stark voranschreitet (Wainright 2002; Willatts et al., 1998). In dieser Zerebralisierungsphase, die sich bis in die ersten Monate nach der Geburt erstreckt, wächst das Gehirn am schnellsten und reagiert am empfindlichsten auf einen Mangel an Nährstoffen: Schwere Defizite können deshalb bleibende Schädigungen verursachen. Offenbar ist die Plazenta an der Synthese von DHA und AA beteiligt (Crawford, 2000). Es wird davon ausgegangen, dass der Fötus pro Woche ca. 30 mg ω-3-Fettsäuren im Gehirn anreichert. 75% aller ungesättigten Fettsäuren im Gehirn entfallen auf AA und DHA, die in einer Relation von 1:1 bis 2:1 vorkommen. DHA akkumuliert – abhängig von der Versorgungslage – verstärkt in den Neuronen des Cortex. In den ersten Monaten nach der Geburt nimmt vor allem die Zahl der Synapsen und dendritischen Verzweigungen im visuellen Cortex zu (Garey 1984; Huttenlocher und de Courten, 1987).
DHA stellt auch einen bedeutenden Baustein der membranständigen Phosphoglyceride in Photorezeptoren der Netzhaut (Retina) dar; die Photorezeptoren besitzen die höchsten DHA-Gehalte aller Körperzellen. Die photochemische Aktivität des Sehfarbstoffs Rhodopsin beruht auf einer schnellen und reversiblen Änderung seiner Konformation und erfordert eine hohe Flexibilität der umgebenden Membran (DeMar et al., 1999); dabei bestimmen die DHA-haltigen Phosphoglyceride die Reizschwelle zur Lichtwahrnehmung. Eine adäquate Versorgung mit DHA in der Zerebralisierungsphase ist wegen ihrer Rolle sowohl im Cortex als auch in der Retina unabdingbar für die normale visuelle und kognitive Entwicklung (Neuringer et al, 1986, 1994, 1996; Uauy et al., 2001).
Risiken eines ω-3-Fettsäuren-Mangels
|
Faktoren der Versorgung
Die Umwandlung von LA und ALA in die längerkettigen Fettsäuren ist abhängig von genetischen Faktoren, der Aufnahme an gesättigten Fettsäuren, der Versorgung mit Vitaminen und mineralischen Kofaktoren, dem Status an Stresshormonen und auch von Geschlechtshormonen. So zeigten In-vivo-Studien, dass die Konversion von ALA zu EPA und DHA bei jungen Frauen weitaus effizienter verläuft als bei jungen Männern (Burdge et al., 2002a, 2002b). Deshalb kann es trotz an sich ausreichender Versorgung mit ALA zu einem Mangel an EPA und DHA und den damit verbundenen Funktionsbeeinträchtigungen kommen. Weitere Untersuchungen zeigten, dass hohe Testosterongehalte im Fruchtwasser einen Einfluss auf Struktur und Funktion neuronaler Gewebe des Fötus haben (Knickmeyer und Baron-Cohen, 2006) und mit einer reduzierten sozialen Entwicklung und Aufmerksamkeit der heranwachsenden Kinder in Verbindung stehen (Knickmeyer et al., 2005). Auch Befunde an Ratten deuten darauf hin, dass männliche Tiere häufiger unter PUFA-Defizienzen und -Imbalancen leiden. Die Ursache ist, dass Testosteron die Synthese von längerkettigen PUFAs inhibiert, während Östrogene sie vor Abbau schützen (Huang und Horrobin, 1987; Marra und de Alaniz, 1989).
Vor dem Hintergrund der insgesamt eher knappen nutritiven Versorgung mit EPA und DHA wird verständlich, dass genetische und geschlechtsspezifische Unterschiede im Metabolismus von PUFAs als mögliche Risikofaktoren für Neuroentwicklungsstörungen gesehen werden (Crawford, 1993; Yoshida et al., 1998). Die geschlechtsspezifischen Unterschiede könnten schließlich sogar die höhere Prävalenz bestimmter neuropsychiatrischer Störungen wie ADHS und Autismus bei Jungen im Vergleich zu Mädchen erklären (Richardson, 2004).
Das höchste Risiko neuronaler Entwicklungsstörungen besteht bei Neugeborenen mit geringem Geburtsgewicht. Ein geringes Geburtsgewicht und ein verringerter Kopfumfang sind häufig mit einem Mangel an AA und DHA assoziiert (Richardson, 2004). Aus Anwendungsbeobachtungen ist bekannt, dass mit steigendem Fischkonsum der Schwangeren das Risiko einer Frühgeburt (mit niedrigem Geburtsgewicht) sinkt (Olsen und Secher, 2002); dafür dürften die in den Fischen enthaltenen ω-3-Fettsäuren verantwortlich sein.
Risiken eines ω-3-Fettsäuren-Mangels
|
Studien zur Supplementierung essenzieller Fettsäuren
Da die Hirnentwicklung bereits beim Embryo beginnt, hängt sie von der Ernährung der werdenden Mutter ab. Eine kontrollierte Studie zeigte, dass Säuglinge im Alter von vier Monaten eine bessere Sehschärfe aufwiesen, wenn ihre Mütter während der Schwangerschaft DHA supplementiert hatten (Tab. 2; Judge et al., 2007).
Tab. 2: Kontrollierte Studien zum Einfluss der Supplementierung von ω-3- und ω-6-Fettsäuren (DHA und AA) auf kognitive Funktionen bei Säuglingen. Kontrolle: keine Supplementierung. | ||||
|
Probanden,
Anzahl
|
Supplementierung pro Tag1 |
Behandlungsdauer |
Ergebnisse der Behandlung |
Autoren |
|
Schwangere Frauen*
n = 30
|
214 mg DHA |
16 Wochen (Durchschnitt) |
Signifikant bessere Sehschärfe im Alter von 4 Monaten; nach 6 Monaten kein Unterschied mehr |
Judge et al., 2007 |
|
Säuglinge**
n = 56
|
0,35% DHA bzw.
0,36% DHA und 0,72% AA
|
17 Wochen |
Signifikant gesteigerte kognitive und motorische Entwicklung;
keine Veränderungen bei sprachlichen und psychomotorischen Entwicklungen sowie Verhalten
|
Birch et al., 2000 |
Abgestillte Säuglinge nach 6-wöchiger Stillzeit**, n = 65 |
0,36% DHA und 0,72% AA |
46 Wochen |
Signifikant bessere Sehkraft (Schärfe und Stereosehen) korrelierte mit DHA-Konzentration im Plasma |
Birch et al., 2002 |
|
Säuglinge***
n = 79
|
0,35% DHA bzw.
0,36% DHA und 0,72% AA
|
17 Wochen |
Keine signifikant bessere Sehschärfe; verbaler IQ bei DHA-Supplementierung war sogar geringer |
Birch et al., 2007 |
1
Prozentwerte = Anteile an den Gesamt-Fettsäuren in der Säuglingsnahrung * ab 24. Schwangerschaftswoche bis zur Geburt ** Ernährung mit Säuglingsnahrung (Formula-Baby-Milch) *** Verumgruppe erhielt Säuglingsnahrung (Formula-Baby-Milch) mit DHA bzw. DHA und AA, Kontrollgruppe wurde gestillt | ||||
Zwar weist die Muttermilch eine hohe Konzentration an essenziellen Fettsäuren auf. Dennoch ist fraglich, ob die Gehalte für den Bedarf der Säuglinge ausreichend sind. Eine Untersuchung zeigte, dass eine Supplementierung von Säuglingen mit DHA und AA auch nach einer vorangegangenen sechswöchigen Stillzeit noch zu einer signifikant verbesserten Sehleistung (Schärfe, Stereosehen) führt (Birch et al., 2002). In einer anderen Studie hatte eine an DHA und AA angereicherte Säuglingsnahrung im Vergleich zu Muttermilch jedoch keinen signifikanten Einfluss auf die Sehschärfe der Säuglinge. Der verbale IQ der Säuglinge, bei denen lediglich DHA supplementiert wurde, war sogar geringer (Birch et al., 2007). Es ist daher nicht klar, ob eine postnatale Supplementierung von gestillten Säuglingen den gleichen positiven Effekt auf die kognitive Entwicklung und Sehschärfe hat wie eine pränatale Supplementierung (Simmer, 2001).
In einer weiteren Studie wiesen die mit DHA supplementierten Säuglinge und Kleinkinder eine signifikante Korrelation zwischen den Plasma-DHA-Gehalten und ihrem mentalen Entwicklungs-Index auf (Tab. 2; Birch et al., 2000). Im Alter von vier Monaten zeigten sich positive Effekte auf die visuelle und kognitive Entwicklung der Säuglinge; bei 12- und 18-monatigen Kleinkindern war dieser Effekt allerdings nicht nachweisbar.
Einfluss von Polyenfettsäuren auf Störungen bei Kindern
Die zahlreichen Einflüsse von ω-3-Fettsäuren auf neuronale Mechanismen (Tab. 1) erklären, dass ein Mangel an diesen Fettsäuren zu einer Beeinträchtigung verschiedener Gehirnfunktionen führt (Tab. 3). Neben Anwendungsbeobachtungen zum Zusammenhang zwischen der Aufnahme von ω-3-Fettsäuren und neuronalen Funktion bzw. bestimmten psychiatrischen Erkrankungen liegen auch entsprechende Interventionsstudien vor (Peet und Stokes, 2005). Demnach ist ein Mangel an ω-3-Fettsäuren bei Kindern beispielsweise mit dem Aufmerksamkeitsdefizit-Hyperaktivitäts-Syndrom (ADHS) und Autismus assoziiert (Richardson und Ross, 2000; Richardson et al. 2005, Freeman et al., 2006).
Tab. 3: Kontrollierte Studien zum Einfluss der Supplementierung mit ω-3- und ω-6-Fettsäuren sowie Vitamin E bei Kindern mit ADHS. Kontrolle: keine Supplementierung. | ||||
|
Probanden,
Anzahl
|
Supplementierung pro Tag |
Behandlungs-dauer |
Ergebnisse der Behandlung |
Autoren |
n = 53 |
480 mg DHA, 80 mg EPA, 96 mg GLA ,40 mg AA, 24 mg α -Tocopherylacetat |
16 Wochen |
Signifikante Besserung bei 2 von 16 Verhaltensskalen |
Stevens et al., 1995 |
n = 50 |
480 mg DHA, 80 mg EPA, 96 mg GLA ,40 mg AA, 24 mg α -Tocopherylacetat |
16 Wochen |
Signifikante Besserung bei ADHS-Verhaltenssymptomen (oppositionelles Verhalten, Zerstörungsverhalten); starker Anstieg der Gehalte an EPA, DHA und α -Tocopherol in Plasmaphospholipiden |
Stevens et al., 2003 |
|
6 bis 12 Jahre alt
n = 63
|
345 mg DHA |
16 Wochen |
Keine signifikanten Effekte auf ADHS-Symptome; DHA-Gehalt in Plasmaphospholipiden 2,6-fach höher als bei Kontrollgruppe |
Voigt et al., 2001 |
|
6 bis 12 Jahre alt
n = 40
|
514 mg DHA und 100 mg EPA |
8 Wochen |
Keine signifikanten Effekte auf ADHS-Symptome |
Hirayama et al., 2004 |
|
8 bis 12 Jahre alt
n = 41
|
480 mg DHA, 186 mg EPA, 96 mg GLA, 42 mg AA, 60 IE α -Tocopherylacetat |
12 + 12 Wochen nach cross-over |
Signifikante Besserung kognitiver Störungen und genereller Verhaltensauffälligkeiten |
Richardson u. Puri, 2002 |
|
5 bis 12 Jahre alt
n = 117
|
558 mg EPA, 174 mg DHA, 60 mg LA, 9,6 mg α -Tocopherol |
12 + 12 Wochen nach cross-over |
Signifikante Verbesserung von Lesen, Aussprache und Verhalten; keine Effekte auf motorische Funktionen |
Richardson u. Montgomery, 2005 |
ADHS mit seinen assoziierten Syndromen ist die häufigste neuro-kognitive Störung bei Kindern. Nach Schätzungen sind etwa 10 bis 20% aller Schulkinder davon betroffen (Richardson, 2004a). Die Symptome des ADHS sind Unaufmerksamkeit (Ablenkbarkeit, Konzentrationsschwäche), Überaktivität sowie kognitive, motivationale und emotionale Impulsivität. Kinder mit ADHS sind häufig unruhig, können schlecht Anweisungen befolgen, Aufgaben bearbeiten oder alltägliche Dinge erledigen, sind vielfach schlecht organisiert und undiszipliniert, haben ein geringes Selbstwertgefühl und in der Regel große Probleme in der Schule. Dies alles belastet auch die Familie, die Erzieher und die Lehrer. Begleitende Syndrome des ADHS sind
- Dyslexie (Lese- und Rechtschreibschwierigkeiten),
- Dyspraxie (Koordinations- und Entwicklungsstörung mit der Schwierigkeit, Bewegungen und Handlungen in Einklang zu bringen) sowie
- Dysgraphie (reine Rechtschreibschwäche).
Diese Störungen persistieren häufig bis ins Erwachsenenalter.
Die Ätiologie der Störungen ist komplex und multifaktoriell, ihre pathogenetischen Mechanismen sind noch weitgehend unbekannt. Es finden sich allerdings zunehmend Belege, dass bei den Betroffenen ein veränderter PUFA-Metabolismus zu Störungen des Phospholipid-Stoffwechsels führt, die wiederum im Zusammenhang mit den Neuroentwicklungsstörungen stehen (Richardson und Ross, 2000; Richardson, 2004). Auch einige psychiatrische Erkrankungen bei Erwachsenen, wie Depressionen, bipolare Störungen, Schizophrenien sowie Persönlichkeitsstörungen, werden mit konstitutionellen Abnormitäten des Fettsäuren- bzw. Phospholipid-Metabolismus in Verbindung gebracht (Biederman et al., 1987; Hellgren et al., 1994; Horrobin et al., 1995; Rasmussen et al., 2000, Bennett und Horrobin, 2000).
In den Membranphospholipiden der Erythrozyten von Kindern mit ADHS sind ω-3-Fettsäuren wie ALA und DHA, aber auch ω-6-Fettsäuren wie AA in unterdurchschnittlichen Konzentrationen vorhanden (Stevens et al., 1995; Stevens et al., 2003; Chen et al., 2004). In einer Studie wiesen Kinder mit geringeren ω-3-Fettsäuren-Spiegeln in den Plasmaphospholipiden größere Verhaltensprobleme und Lernschwierigkeiten auf als Kinder mit höheren ω-3-Fettsäuren-Spiegeln (Burgess et al., 2000).
Inzwischen liegen verschiedene placebokontrollierte klinische Studien vor, in denen Kinder mit ADHS bzw. assoziierten Syndromen wie Dyslexie und Dyspraxie unterschiedliche Polyenfettsäuren teils einzeln, teils in Kombination erhielten (Tab. 3). Die alleinige Gabe der ω-6-Fettsäure GLA bei hyperaktiven und ADHS-Kindern ergab nur einen geringen therapeutischen Nutzen (Aman et al., 1987; Arnold et al., 1989). Ebenso wenig erfolgreich war die Verabreichung von ω-3-Fettsäuren in Monotherapie. So ergaben zwei Studien, in denen Kinder mit ADHS entweder DHA alleine oder kombiniert mit EPA erhielten, keinen Effekt auf Verhaltensmerkmale wie Aufmerksamkeit und Impulsivität oder assoziierte Symptome (Voigt et al., 2001; Hirayama et al., 2004).
Allerdings führte die Supplementierung der ω-6-Fettsäuren EPA oder DHA in Kombination mit den ω-6-Fettsäuren LA, GLA oder AA in verschiedenen Studien zu einem Rückgang der ADHS-Symptome. In einer Pilot-Studie stellten Richardson und Puri (2002) bei dyslektischen ADHS-Kindern nach der Supplementierung von vier PUFAs (EPA, DHA, AA, GLA) einen signifikanten Rückgang der Symptomatik fest. Die Effekte waren besonders ausgeprägt bei psychosomatischen Symptomen wie Ängstlichkeit und Schüchternheit, bei kognitiven Problemen, Unaufmerksamkeit, Hyperaktivität und Impulsivität. Auch in zwei weiteren Studien mit ADHS-Kindern (Stevens et al., 1995; Stevens et al. 2003) führte die Supplementierung von DHA und EPA in Kombination mit AA und GLA zu einem Rückgang zahlreicher ADHS-Verhaltenssymptome wie oppositionellem Verhalten und Zerstörungsverhalten. Die Effekte gingen mit einem starken Anstieg der EPA- und DHA-Gehalte in den erythrozytären Membranphospholipiden einher (Stevens et al., 1995; Stevens et al. 2003; Richardson und Montgomery, 2005). In der randomisierten Oxford-Durham Study erhielten 117 Kinder mit Dyspraxie EPA und DHA in Kombination mit GLA (Richardson und Montgomery, 2005). Die Supplementierung führte zu signifikanten Verbesserungen des Lesens, der Aussprache und des Verhaltens. Nach einem einseitigen cross-over traten diese Effekte auch bei den zuvor placebobehandelten Kindern auf. Allerdings konnten keine Verbesserungen bei den motorischen Funktionen der Kinder festgestellt werden.
Autistische Störungen
Autistische Störungen beruhen auf tief greifende Wahrnehmungs- und Informationsverarbeitungsveränderungen des Gehirns. Sie treten bereits im frühen Kindesalter auf und sind charakterisiert durch Schwächen der sozialen Interaktion und Kommunikation sowie durch stereotype Verhaltensweisen einerseits und durch Stärken der Wahrnehmung und Aufmerksamkeit, des Gedächtnisses und der Intelligenz andererseits. Zudem zeigen autistische Kinder häufig Verhaltensauffälligkeiten wie selbstverletzendes Handeln, Aggressionen und Wutanfälle. Die Behandlung mit Psychopharmaka unterschiedlichster Wirkstoffklassen hat nur einen mäßigen Erfolg und häufig unakzeptable Nebenwirkungen (Posey und McDougle 2001). Wie bei ADHS, Dyslexie und Dypraxie bestehen auch bei autistischen Störungen Zusammenhänge mit Fettsäuren-Defizienzen oder -Imbalancen (Richardson 2004a; Vancassel et al., 2001). So zeigen auch autistische Kinder unterdurchschnittliche ω-3-Fettsäurengehalte im Plasma (Vancassel et al., 2001) und in erythrozytären Membranphospholipiden (Bell et al., 2004).
In einer Anwendungsbeobachtung berichteten Eltern, dass sich der Gesundheitszustand ihrer autistischen Kinder nach der Supplementierung von ω-3-Fettsäuren-reichen Fischölen generell verbessert habe (Bell et al., 2004). Die Kinder konnten besser schlafen, sich leichter konzentrieren, wiesen verbesserte kognitive und motorische Fähigkeiten auf, waren umgänglicher und weniger gereizt bzw. aggressiv sowie weniger hyperaktiv. Dieser Erfolg gab Anlass zu weiteren Untersuchungen. Inzwischen liegen Daten einer kleinen randomisierten, doppelblinden und placebokontrollierten Studie vor, in der 13 autistische Kinder im Alter von fünf bis 17 Jahren sechs Wochen lang mit ω-3-Fettsäuren behandelt wurden (Amminger et al., 2007). Die Supplementierung hatte einen deutlich positiven Effekt auf Hyperaktivität und Stereotypie. Um das therapeutische Potenzial genauer abzuschätzen, bedarf es weiterer Studien mit größeren Patientenkollektiven.
Depressionen
Kinder leiden häufiger unter Depressionen, als allgemein angenommen wird. Die American Academy of Child and Adolescent Psychiatry (AACAP) schätzt, dass die Prävalenz bei etwa 2 bis 4% liegt (AACAP, 1998). Die Depressionen werden häufig von Panikattacken sowie Angst- oder Zwangszuständen begleitet; sie treten oft zusammen mit ADHS auf. Depressive Kinder und Jugendliche weisen eine geringe psychosoziale Kompetenz auf und sind häufig suizidgefährdet. Die frühe Diagnose und Behandlung derartiger Störungen ist daher von großer Bedeutung.
Nachdem zahlreiche Studien einen positiven Effekt von ω-3-Fettsäuren in der Behandlung von depressiven Erwachsenen gezeigt haben, wurde kürzlich eine entsprechende Studie mit Kindern durchgeführt (Nemets et al., 2006). Die zwischen 6 und 12 Jahre alten Kinder wurden 16 Wochen mit EPA und DHA supplementiert. Die Behandlung zeigte in allen drei angewandten Bewertungsskalen der depressiven Symptomatik (Children’s Depression Rating Scale, CDRS; Children’s Depression Inventory, CDI; Clinical Global Impression, CGI) einen signifikanten Effekt.
Das Wichtigste in Kürze
|
Aktuelle Versorgungssituation
Zur Aufrechterhaltung lebensnotwendiger Funktionen ist nach heutigem Kenntnisstand die Zufuhr von mindestens 0,1 bis 0,2 g EPA und DHA pro Tag notwendig; als wünschenswert gelten 0,3 bis 0,4 g EPA und DHA (Singer, 2000). Nach den Empfehlungen der Deutschen Gesellschaft für Ernährung (DGE) sollten Kinder, Jugendliche und Erwachsene rund 0,5% der Gesamtenergie in Form von ω-3-Fettsäuren aufnehmen, wobei die ω-3- zu ω-6-Relation 1:5 betragen soll (DGE et al. 2000). Dies entspricht bei 1000 kcal einem Bedarf von ca. 0,5 ALA und ca. 2,6 g LA; schwangere und stillende Frauen sollten 150 bis zu 350 mg ω-3-Fettsäuren pro Tag zusätzlich aufnehmen. Die Britische Fachgesellschaft für Ernährung empfiehlt, 0,5% der Gesamtenergie in Form von EPA und DHA aufzunehmen (British Nutrition Foundation; BNF, 1995).
Zwischen der wünschenswerten und der tatsächlichen Aufnahme herrscht häufig eine Diskrepanz. Das liegt in erster Linie an den üblichen Ernährungsgewohnheiten in westlichen Industrieländern. In der hier vorherrschenden Nahrung, speziell in Fertignahrungsprodukten ist der Gehalt an ω-3-Fettsäuren äußerst gering. EPA und DHA finden sich in größeren Konzentrationen nur in einigen wenigen fettreichen Kaltwasserfischen wie Lachs, Makrele oder Hering, während sich ALA in einigen grünen Gemüsesorten sowie bestimmten Nüssen und Saaten findet. Laut Ernährungsbericht der DGE nehmen Kinder zwischen vier und zehn Jahren etwa 0,1 g EPA und DHA sowie 1,39 g ALA pro Tag zu sich (DGE, 2004). Die ALA-Zufuhrmenge ergibt bei einer Konversionsrate von 5 bis 10% eine zusätzliche Menge von 0,05 bis 0,1 g EPA und DHA pro Tag. Zur Verbesserung der Versorgungssituation kommen Nahrungsergänzungsmittel wie Fischöl-Kapseln oder funktionelle Lebensmittel wie mikroverkapselte ω-3-Fettsäuren-Produkte in Betracht (Schmitt et al., 2002).
Auch die ausgewogene Versorgung mit ω-6-Fettsäuren ist in westlichen Industrieländern nicht sichergestellt. Während die meisten Pflanzenöle eine genügende Menge LA liefern, ergibt sich durch die im Allgemeinen zu fleischreiche Ernährungsweise eine zu hohe Zufuhr an AA und dadurch eine Imbalance zwischen ω-3- und ω-6-Fettsäuren.
Literatur
Aman, M. G., Mitchell, E. A. Turbott, S. H., 1987. The effects of essential fatty acid supplementation by Efamol in hyperactive children. J. Abnorm. Child Psychol., 15(1): 75-90.
Amminger, G. P., Berger, G. E., Schafer, M. R., Klier, C., Friedrich, M. H., Feucht, M., 2007. Omega-3 fatty acids supplementation in children with autism: a double-blind randomized, placebo-controlled pilot study. Biol. Psychiatry, 61(4): 551-553.
Arnold, L. E., Kleykamp, D., Votolato, N. A., Taylor, W. A., Kontras, S. B., Tobin, K., 1989. Gamma-linolenic acid for attention-deficit hyperactivity disorder: placebo-controlled comparison to D-amphetamine. Biol. Psychiatry, 25(2): 222-228.
Barcelo-Coblijn, G., Hogyes, E., Kitajka, K., Puskas, L. G., Zvara, A., Hackler, L., Jr., Nyakas, C., Penke, Z., Farkas, T., 2003. Modification by docosahexaenoic acid of age-induced alterations in gene expression and molecular composition of rat brain phospholipids. Proc. Natl. Acad. Sci. U.S.A., 100(20): 11321-11326.
Bell, J. G., MacKinlay, E. E., Dick, J. R., MacDonald, D. J., Boyle, R. M., Glen, A. C., 2004. Essential fatty acids and phospholipase A2 in autistic spectrum disorders. Prostaglandins Leukot. Essent. Fatty Acids, 71(4): 201-204.
Bennett, C. N., Horrobin, D. F., 2000. Gene targets related to phospholipid and fatty acid metabolism in schizophrenia and other psychiatric disorders: an update. Prostaglandins Leukot. Essent. Fatty Acids, 63(1-2): 47-59.
Biederman, J., Munir, K., Knee, D., Armentano, M., Autor, S., Waternaux, C., Tsuang, M., 1987. High rate of affective disorders in probands with attention deficit disorder and in their relatives: a controlled family study. Am. J. Psychiatry, 144(3): 330-333.
Birch, E. E., Garfield, S., Hoffman, D. R., Uauy, R., Birch, D. G., 2000. A randomized controlled trial of early dietary supply of long-chain polyunsaturated fatty acids and mental development in term infants. Dev. Med. Child Neurol., 42(3): 174-181.
Birch, E. E., Hoffman, D. R., Castaneda, Y. S., Fawcett, S. L., Birch, D. G., Uauy, R. D., 2002. A randomized controlled trial of long-chain polyunsaturated fatty acid supplementation of formula in term infants after weaning at 6 wk of age. Am. J. Clin. Nutr., 75(3): 570-580.
Birch, E. E., Garfield, S., Castaneda, Y., Hughbanks-Wheaton, D., Uauy, R., Hoffman, D., 2007. Visual acuity and cognitive outcomes at 4 years of age in a double-blind, randomized trial of long-chain polyunsaturated fatty acid-supplemented infant formula. Early Hum. Dev., 83(5): 279-284.
Bourre, J. M., Dumont, O., Piciotti, M., Clement, M., Chaudiere, J., Bonneil, M., Nalbone, G., Lafont, H., Pascal, G., Durand, G., 1991. Essentiality of omega 3 fatty acids for brain structure and function. World Rev. Nutr. Diet., 66: 103-117.
Bourre, J. M., Dumont, O., Durand, G., 1993. Brain phospholipids as dietary source of (n-3) polyunsaturated fatty acids for nervous tissue in the rat. J. Neurochem., 60(6): 2018-2028.
British Nutrition Foundation (BNF), 1995. n-3 fatty acids and health. Briefing paper. London, BNF.
Burdge, G. C., Wootton, S. A., 2002a. Conversion of alpha-linolenic acid to eicosapentaenoic, docosapentaenoic and docosahexaenoic acids in young women. Br. J. Nutr., 88(4): 411-420.
Burdge, G. C., Jones, A. E., Wootton, S. A., 2002b. Eicosapentaenoic and docosapentaenoic acids are the principal products of alpha-linolenic acid metabolism in young men. Br. J. Nutr., 88(4): 355-363.
Burgess, J. R., Stevens, L., Zhang, W., Peck, L., 2000. Long-chain polyunsaturated fatty acids in children with attention-deficit hyperactivity disorder. Am. J. Clin. Nutr., 71(1 Suppl): 327S-330S.
Calder, P. C., 1997. n-3 polyunsaturated fatty acids and cytokine production in health and disease. Ann. Nutr. Metab., 41(4): 203-234.
Calderon, F., Kim, H. Y., 2004. Docosahexaenoic acid promotes neurite growth in hippocampal neurons. J. Neurochem., 90(4): 979-988.
Chen, J. R., Hsu, S. F., Hsu, C. D., Hwang, L. H., Yang, S. C., 2004. Dietary patterns and blood fatty acid composition in children with attention-deficit hyperactivity disorder in Taiwan. J. Nutr. Biochem., 15(8): 467-472.
Crawford, M. A., 1993. The role of essential fatty acids in neural development: implications for perinatal nutrition. Am. J. Clin. Nutr., 57(5 Suppl): 703S-709S.
Crawford, M., 2000. Placental delivery of arachidonic and docosahexaenoic acids: implications for the lipid nutrition of preterm infants. Am. J. Clin. Nutr., 71(1 Suppl): 275S-284S.
DGE, Deutsche Gesellschaft fur Ernahrung, 2004. Ernahrungsbericht 2004. Hrsg. Deutsche Gesellschaft fur Ernahrung e.V., Bonn, 2004.
Delion, S., Chalon, S., Herault, J., Guilloteau, D., Besnard, J. C., Durand, G., 1994. Chronic dietary alpha-linolenic acid deficiency alters dopaminergic and serotoninergic neurotransmission in rats. J. Nutr., 124(12): 2466-2476.
DeMar, J. C., Jr., Rundle, D. R., Wensel, T. G., Anderson, R. E., 1999. Heterogeneous N-terminal acylation of retinal proteins. Prog. Lipid Res., 38(1): 49-90.
Drevon, C. A., 1992. Marine oils and their effects. Nutr. Rev., 50(4 ( Pt 2)): 38-45.
Freeman, M. P., Hibbeln, J. R., Wisner, K. L., Davis, J. M., Mischoulon, D., Peet, M., Keck, P. E., Jr., Marangell, L. B., Richardson, A. J., Lake, J., Stoll, A. L., 2006. Omega-3 fatty acids: evidence basis for treatment and future research in psychiatry. J. Clin. Psychiatry, 67(12): 1954-1967.
Garey, L. J., 1984. Structural development of the visual system of man. Hum. Neurobiol., 3(2): 75-80.
Hahn, A., Strohle, A., 2004. Pravention degenerativer Erkrankungen, ƒÖ-3-Fettsauren. Chem. unserer Zeit, 38, 310-318.
Hahn, A., Strohle, A., Wolters, M., 2006. Ernahrung . Physiologische Grundlagen, Pravention, Therapie. 2. Auflage, Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart.
Hahn, A., Strohle, A., Wolters, M., 2007. Ernahrung bei Erkrankungen des rheumatischen Formenkreises. Medizinische Monatsschrift fur Pharmazeuten, 30, 138-146.
Hellgren, L., Gillberg, I. C., Bagenholm, A., Gillberg, C., 1994. Children with deficits in attention, motor control and perception (DAMP) almost grown up: psychiatric and personality disorders at age 16 years. J. Child Psychol. Psychiatry, 35(7): 1255-1271.
Hibbeln, J. R., 1998. Fish consumption and major depression. Lancet, 351(9110): 1213.
Hibbeln, J. R., Bissette, G., Umhau, J. C., George, D. T., 2004. Omega-3 status and cerebrospinal fluid corticotrophin releasing hormone in perpetrators of domestic violence. Biol. Psychiatry, 56(11): 895-897.
Hirayama, S., Hamazaki, T., Terasawa, K., 2004. Effect of docosahexaenoic acid-containing food administration on symptoms of attention-deficit/hyperactivity disorder - a placebo-controlled double-blind study. Eur. J. Clin. Nutr., 58(3): 467-473.
Horrobin, D. F., Glen, A. I., Hudson, C. J., 1995. Possible relevance of phospholipid abnormalities and genetic interactions in psychiatric disorders: the relationship between dyslexia and schizophrenia. Med. Hypotheses, 45(6): 605-613.
Huang, Y. S., Horrobin, D. F., 1987. Sex differences in n-3 and n-6 fatty acid metabolism in EFA-depleted rats. Proc. Soc. Exp. Biol. Med., 185(3): 291-296.
Huttenlocher, P. R., de Court, C., 1987. The development of synapses in striate cortex of man. Hum. Neurobiol., 6(1): 1-9.
Ikemoto, A., Kobayashi, T., Watanabe, S., Okuyama, H., 1997. Membrane fatty acid modifications of PC12 cells by arachidonate or docosahexaenoate affect neurite outgrowth but not norepinephrine release. Neurochem. Res., 22(6): 671-678.
Judge, M. P., Harel, O., Lammi-Keefe, C. J., 2007. A docosahexaenoic acid-functional food during pregnancy benefits infant visual acuity at four but not six months of age. Lipids, 42(2): 117-122.
Jump, D. B., 2002. Dietary polyunsaturated fatty acids and regulation of gene transcription. Curr. Opin. Lipidol., 13(2): 155-164.
Kelley, D. S., Taylor, P. C., Nelson, G. J., Schmidt, P. C., Ferretti, A., Erickson, K. L., Yu, R., Chandra, R. K., Mackey, B. E., 1999. Docosahexaenoic acid ingestion inhibits natural killer cell activity and production of inflammatory mediators in young healthy men. Lipids, 34(4): 317-324.
Kim, H. Y., Akbar, M., Kim, K. Y., 2001. Inhibition of neuronal apoptosis by polyunsaturated fatty acids. J. Mol. Neurosci., 16(2-3): 223-227.
Kim, H. Y., Akbar, M., Lau, A., 2003. Effects of docosapentaenoic acid on neuronal apoptosis. Lipids, 38(4): 453-457.
Kinsella, J. E., 1990. Lipids, membrane receptors, and enzymes: effects of dietary fatty acids. JPEN J. Parenter. Enteral Nutr., 14(5 Suppl): 200S-217S.
Kitajka, K., Puskas, L. G., Zvara, A., Hackler, L., Jr., Barcelo-Coblijn, G., Yeo, Y. K., Farkas, T., 2002. The role of n-3 polyunsaturated fatty acids in brain: modulation of rat brain gene expression by dietary n-3 fatty acids. Proc. Natl. Acad. Sci. U.S.A., 99(5): 2619-2624.
Knickmeyer, R., Baron-Cohen, S., Raggatt, P., Taylor, K., 2005. Foetal testosterone, social relationships, and restricted interests in children. J. Child Psychol. Psychiatry, 46(2): 198-210.
Knickmeyer, R. C., Baron-Cohen, S., 2006. Fetal testosterone and sex differences in typical social development and in autism. J. Child Neurol., 21(10): 825-845.
Kodas, E., Galineau, L., Bodard, S., Vancassel, S., Guilloteau, D., Besnard, J. C., Chalon, S., 2004. Serotoninergic neurotransmission is affected by n-3 polyunsaturated fatty acids in the rat. J. Neurochem. , 89(3): 695-702.
Lee, A., 2001. Membrane structure. Curr. Biol., 11(20): R811-R814.
Leitzmann, C., Muller, C., Michel, P., Brehme, U., Hahn, A., Laube, H., 2003. Ernahrung in Pravention und Therapie, 2. Aufl., Hippokrates, Stuttgart, 328.
Mamalakis, G., Kiriakakis, M., Tsibinos, G., Kafatos, A., 2004. Depression and adipose polyunsaturated fatty acids in the survivors of the Seven Countries Study population of Crete. Prostaglandins Leukot. Essent. Fatty Acids, 70(6): 495-501.
Marra, C. A., de Alaniz, M. J., 1989. Influence of testosterone administration on the biosynthesis of unsaturated fatty acids in male and female rats. Lipids, 24(12): 1014-1019.
Meydani, S. N., Endres, S., Woods, M. M., Goldin, B. R., Soo, C., Morrill-Labrode, A., Dinarello, C. A., Gorbach, S. L., 1991. Oral (n-3) fatty acid supplementation suppresses cytokine production and lymphocyte proliferation: comparison between young and older women. J. Nutr., 121(4): 547-555.
Meydani, S. N., Lichtenstein, A. H., Cornwall, S., Meydani, M., Goldin, B. R., Rasmussen, H., Dinarello, C. A., Schaefer, E. J., 1993. Immunologic effects of national cholesterol education panel step-2 diets with and without fish-derived N-3 fatty acid enrichment. J. Clin. Invest, 92(1): 105-113.
Mirnikjoo, B., Brown, S. E., Kim, H. F., Marangell, L. B., Sweatt, J. D., Weeber, E. J., 2001. Protein kinase inhibition by omega-3 fatty acids. J. Biol. Chem., 276(14): 10888-10896.
Nemets, H., Nemets, B., Apter, A., Bracha, Z., Belmaker, R. H., 2006. Omega-3 treatment of childhood depression: a controlled, double-blind pilot study. Am. J. Psychiatry, 163(6): 1098-1100.
Neuringer, M., Connor, W. E., Lin, D. S., Barstad, L., Luck, S., 1986. Biochemical and functional effects of prenatal and postnatal omega 3 fatty acid deficiency on retina and brain in rhesus monkeys. Proc. Natl. Acad. Sci. U.S.A., 83(11): 4021-4025.
Neuringer, M., Reisbick, S., Janowsky, J., 1994. The role of n-3 fatty acids in visual and cognitive development: current evidence and methods of assessment. J. Pediatr., 125(5 Pt 2): S39-S47.
Pawlosky, R. J., Hibbeln, J. R., Novotny, J. A., Salem, N., Jr., 2001. Physiological compartmental analysis of alpha-linolenic acid metabolism in adult humans. J. Lipid Res., 42(8): 1257-1265.
Peet, M., Stokes, C., 2005. Omega-3 fatty acids in the treatment of psychiatric disorders. Drugs, 65(8): 1051-1059.
Posey, D. J., McDougle, C. J., 2001. Pharmacotherapeutic management of autism. Expert. Opin. Pharmacother., 2(4): 587-600.
Olsen, S. F., Secher, N. J., 2002. Low consumption of seafood in early pregnancy as a risk factor for preterm delivery: prospective cohort study. BMJ, 324(7335): 447.
Rasmussen, P., Gillberg, C., 2000. Natural outcome of ADHD with developmental coordination disorder at age 22 years: a controlled, longitudinal, community-based study. J. Am. Acad. Child Adolesc. Psychiatry, 39(11): 1424-1431.
Richardson, A. J., Ross, M. A., 2000. Fatty acid metabolism in neurodevelopmental disorder: a new perspective on associations between attention-deficit/hyperactivity disorder, dyslexia, dyspraxia and the autistic spectrum. Prostaglandins Leukot. Essent. Fatty Acids, 63(1-2): 1-9.
Richardson, A. J., Puri, B. K., 2000. The potential role of fatty acids in attention-deficit/hyperactivity disorder. Prostaglandins Leukot. Essent. Fatty Acids, 63(1-2): 79-87.
Richardson, A. J., 2004a. Long-chain polyunsaturated fatty acids in childhood developmental and psychiatric disorders. Lipids, 39(12): 1215-1222.
Richardson, A. J., 2004b. Clinical trials of fatty acid treatment in ADHD, dyslexia, dyspraxia and the autistic spectrum. Prostaglandins Leukot. Essent. Fatty Acids, 70(4): 383-390.
Richardson, A. J., Montgomery, P., 2005. The Oxford-Durham study: a randomized, controlled trial of dietary supplementation with fatty acids in children with developmental coordination disorder. Pediatrics, 115(5): 1360-1366.
Salem, N., Jr., Pawlosky, R., Wegher, B., Hibbeln, J., 1999. In vivo conversion of linoleic acid to arachidonic acid in human adults. Prostaglandins Leukot. Essent. Fatty Acids, 60(5-6): 407-410.
Schmitt, B., Strohle, A., Watkinson, B.M., Hahn, A., 2002. Wirkstoffe funktioneller Lebensmittel in der Pravention der Arteriosklerose, Teil 2: ƒÖ-3-Fettsauren . Versorgungssituation und Zufuhrempfehlung, Ernahrungs-Umschau 49 (2002) Heft 6.
Seung Kim, H. F., Weeber, E. J., Sweatt, J. D., Stoll, A. L., Marangell, L. B., 2001. Inhibitory effects of omega-3 fatty acids on protein kinase C activity in vitro. Mol. Psychiatry, 6(2): 246-248.
Simmer, K., 2001. Longchain polyunsaturated fatty acid supplementation in infants born at term. Cochrane Database Syst. Rev., (4): CD000376.
Simopoulos, A. P., 1999. Essential fatty acids in health and chronic disease. Am. J. Clin. Nutr., 70(3 Suppl): 560S-569S.
Simopoulos, A. P., 2002. Omega-3 fatty acids in inflammation and autoimmune diseases. J. Am. Coll. Nutr., 21(6): 495-505.
Singer, P., 2000. Was sind, wie wirken ƒ-3-Fettsauren? Frankfurt/M., Umschau Zeitschriftenverlag.
Stevens, L. J., Zentall, S. S., Deck, J. L., Abate, M. L., Watkins, B. A., Lipp, S. R., Burgess, J. R., 1995. Essential fatty acid metabolism in boys with attention-deficit hyperactivity disorder. Am. J. Clin. Nutr., 62(4): 761-768.
Stevens, L., Zhang, W., Peck, L., Kuczek, T., Grevstad, N., Mahon, A., Zentall, S. S., Arnold, L. E., Burgess, J. R., 2003. EFA supplementation in children with inattention, hyperactivity, and other disruptive behaviors. Lipids, 38(10): 1007-1021.
Strohle, A., Schmitt, B., Hahn, A., 2002. Functional Foods . Eine Ubersicht zur aktuellen Situation. Journal fur orthomolekulare Medizin, 10, 326-349.
Tsukada, H., Kakiuchi, T., Fukumoto, D., Nishiyama, S., Koga, K., 2000. Docosahexaenoic acid (DHA) improves the age-related impairment of the coupling mechanism between neuronal activation and functional cerebral blood flow response: a PET study in conscious monkeys. Brain Res., 862(1-2): 180-186.
Uauy, R., Hoffman, D. R., Peirano, P., Birch, D. G., Birch, E. E., 2001. Essential fatty acids in visual and brain development. Lipids, 36(9): 885-895.
Vancassel, S., Durand, G., Barthelemy, C., Lejeune, B., Martineau, J., Guilloteau, D., Andres, C., Chalon, S., 2001. Plasma fatty acid levels in autistic children. Prostaglandins Leukot. Essent. Fatty Acids, 65(1): 1-7.
Villa, B., Calabresi, L., Chiesa, G., Rise, P., Galli, C., Sirtori, C. R., 2002. Omega-3 fatty acid ethyl esters increase heart rate variability in patients with coronary disease. Pharmacol. Res., 45(6): 475.
Voigt, R. G., Llorente, A. M., Jensen, C. L., Fraley, J. K., Berretta, M. C., Heird, W. C., 2001. A randomized, double-blind, placebo-controlled trial of docosahexaenoic acid supplementation in children with attention-deficit/hyperactivity disorder. J. Pediatr., 139(2): 189-196.
Wainwright, P. E., 2002. Dietary essential fatty acids and brain function: a developmental perspective on mechanisms. Proc. Nutr. Soc., 61(1): 61-69.
Willatts, P., Forsyth, J. S., DiModugno, M. K., Varma, S., Colvin, M., 1998. Effect of long-chain polyunsaturated fatty acids in infant formula on problem solving at 10 months of age. Lancet, 352(9129): 688-691.
Ximenes da Silva, S. A., Lavialle, F., Gendrot, G., Guesnet, P., Alessandri, J. M., Lavialle, M., 2002. Glucose transport and utilization are altered in the brain of rats deficient in n-3 polyunsaturated fatty acids. J. Neurochem., 81(6): 1328-1337.
Yoshida, S., Sato, A., Okuyama, H., 1998. Pathophysiological effects of dietary essential fatty acid balance on neural systems. Jpn. J. Pharmacol., 77(1): 11-22.
Zimmer, L., Hembert, S., Durand, G., Breton, P., Guilloteau, D., Besnard, J. C., Chalon, S., 1998. Chronic n-3 polyunsaturated fatty acid diet-deficiency acts on dopamine metabolism in the rat frontal cortex: a microdialysis study. Neurosci. Lett., 240(3): 177-181.
Anschrift der Verfasser:
Dr. Jan Philipp Schuchardt und Prof. Dr. Andreas Hahn
Leibniz Universität Hannover
Institut für Lebensmittelwissenschaft und Ökotrophologie
Abteilung für Ernährungsphysiologie und Humanernährung
Wunstorfer Str. 14, 30453 Hannover
E-Mail: andreas.hahn@lw.uni-hannover.de
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.