
- DAZ.online
- DAZ / AZ
- DAZ 45/2005
- Thermogravimetrie – ...
Analytik
Thermogravimetrie – Eine Analysenmethode des Arzneibuchs
Grundlagen der Thermogravimetrie
Mit Hilfe der thermogravimetrischen Analyse (TA, TGA) lassen sich Masse und Massenänderungen einer Probe in Abhängigkeit von Temperatur, Zeit und Atmosphäre erfassen. Die dazu verwendeten Waagen samt Zubehör werden als TG-Waagen oder Thermowaagen bezeichnet. Im Handel finden sich verschiedene Konstruktionen, denen gemeinsam ist, dass sie einen Ofen und eine Waage besitzen (Abb. 1 und 2).
Ausschnitte mit Ofen und Waage.
1: Vertikaler Rohrofen mit oberschaliger Waage; 2: Vertikaler Rohrofen mit unterschaliger Waage; 3: Horizontaler Rohrofen; 4: Kleiner, die Probe umschließender Ofen in Tiegelform. Aus [2] und [6].
Bei einer TGA wird die Probe einem festen Temperaturprogramm unterzogen, welches isothermal sein kann oder Abschnitte mit unterschiedlichen Heizraten aufweisen kann. Da die Masse der Probe keine Funktion der Temperatur ist, sind Messungen nur sinnvoll, wenn die Probe mit der gasförmigen Umgebung Masse austauschen kann. Die Probe kann beispielsweise verdampfen, bei Zersetzung flüchtige Bestandteile an die Umgebung abgeben oder bei Oxidationsprozessen flüchtige Bestandteile aus der Umgebung aufnehmen. Derartige Prozesse führen zu einer messbaren Massenänderung der untersuchten Probe.
Für die Vorgehensweise der TGA sind einige wenige, aber wesentliche Regeln, zu beachten.
- Da die TGA mit kleinen Probenmassen auskommt, hat bereits die Probenziehung erheblichen Einfluss auf das Ergebnis. Es muss sichergestellt werden, dass die Probe repräsentativ für das Gesamtkollektiv ist.
- Bei der Analyse ist auf folgende Faktoren zu achten, die das Ergebnis beeinflussen können: Atmosphäre (Spülgas), Einwaage, Heizrate und Tiegelform.
Thermogravimetrisch auswertbare Prozesse
- Reaktion der Probe führt zu Massenverlust: Probe -> Gas (Sublimation, Zersetzung, Verdampfung) oder Probe -> Gas + fester Rückstand (Zersetzung, Desorption).
- Reaktion der Probe führt zu Massenzunahme: Probe + Gas -> festes oder flüssiges Reaktionsprodukt (Oxidation).
- Änderung der physikalischen Eigenschaften der Probe ohne Einfluss auf die Masse: ferromagnetische Probe <-> paramagnetische Probe (fiktiver Massenverlust).
Kurvenverlauf und Auswertung
Bei der Thermogravimetrie wird die Massenänderung einer Probe in Abhängigkeit von der Temperatur und/oder der Zeit entweder absolut in Milligramm oder relativ in Prozent der Einwaage in Form einer Kurve (TG-Kurve) aufgezeichnet. Massenänderungen können dabei entweder einstufig (Abb. 3) oder mehrstufig erfolgen.
Die Ereignistemperaturen sollten nur auf 1 °C genau angegeben werden. Bei mehrstufigen Massenänderungen kann es vorkommen, dass die einzelnen Stufen ineinander übergehen. In solchen Fällen oder bei nur geringfügigen Massenänderungen ist es vorteilhaft, die erste zeitliche Ableitung des Messsignals
d(Δm)/dt = d(m - mA)/dt = dm/dt
für die Auswertung heranzuziehen [2].
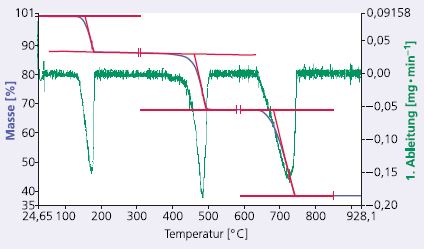
dm(T)/dt wird als "differenzierte thermogravimetrische Kurve" (kurz: DTG-Kurve) bezeichnet. Die zusätzlich zur TG-Kurve aufgezeichnete DTG-Kurve (Abb. 4) ermöglicht es
- einzelne Schritte eines komplexen Prozesses besser voneinander abzutrennen,
- kleine, schwer erkennbare Massenänderungen als deutliches Signal darzustellen und damit den Beginn und das Ende eines Prozesses eindeutig zu bestimmen,
- die Temperatur des maximalen Stoffumsatzes aus dem DTG-Maximum zu bestimmen (Wendepunkt der TG-Kurve).
Hier: mehrstufige Massenänderung von Calciumoxalat-Monohydrat.
1: Massenverlust durch Verflüchtigung von Bestandteilen
oder Reaktionsprodukten der
Probe; 2: Massenzunahme durch Aufnahme von Sauerstoff (z.B. bei Metallen); 3: Annähernd konstanter Massenverlust (z.B. bei Verbrennung von Ruß in O2-Atmosphäre); 4:
Zweistufige Massenänderung;
5: Überlagerung der Kurve
durch einen Rückstoß bei explosiver
Reaktion. Aus [7].
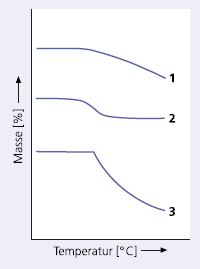
Es lassen sich verschiedene Typen der Massenänderung und folglich verschiedene Kurvenverläufe unterscheiden (Abb. 5):
- Die meisten Massenänderungen verlaufen stufenförmig, entweder als Massenverlust durch Verflüchtigung von Bestandteilen oder Reaktionsprodukten der Probe oder als Massenzunahme durch Aufnahme von Sauerstoff.
- Diffusionskontrollierte Reaktionen, bei denen der Abtransport eines Produktes oder die Zufuhr eines Reaktionspartners limitierend ist, verlaufen mit annähernd konstanter Geschwindigkeit. Ein Beispiel dafür ist die Verbrennung von Ruß nach Austausch einer Stickstoff- gegen eine Sauerstoffatmosphäre (Gaswechsel).
- Oft sind mehrstufige Massenänderungen zu beobachten.
- Bei Explosivstoffen kann es zu einer schlagartigen Zersetzung der Substanz kommen, sodass das TG-Signal durch einen Rückstoß überlagert wird.
SCHMELZPROZESS 1: durch Verdampfung der Probe; 2: durch
Verflüchtigung einer Komponente;
3: durch Verflüchtigung eines
Zersetzungsprodukts. Aus [7].
Bei Überschreitung des Schmelzpunktes ist zumeist kein Effekt auf die TG-Kurve zu erwarten, da sich die Masse der Probe durch die Verflüssigung nicht ändert. Der Auftrieb bei eventuell auftretenden Dichteunterschiede von fester und flüssiger Probe bewirkt nur in den seltensten Fällen eine Abweichung von mehr als 1 µg. Häufiger findet man nach dem Überschreiten des Schmelzpunktes jedoch einen Massenverlust aufgrund des höheren Dampfdruckes der Probe oder ihrer Komponenten oder ihrer Reaktionsprodukte (Abb. 6).
Kalibrierung
Thermowaagen müssen bezüglich der angezeigten Masse und Temperatur kalibriert werden. Zur Temperaturkalibrierung schreibt das Europäische Arzneibuch (Monographie 2.2.34) das übliche Verfahren über die Curie-Temperatur von Nickel vor, zur Kalibrierung der Masse die Bestimmung des Hydratwasserverlustes von Calciumoxalat-Monohydrat CRS; das letztere Verfahren ersetzt die hier allgemein übliche Abgleichung über Eichgewichte [6].
Kalibrierung der Temperatur
Die Temperaturkalibrierung erfolgt über die Bestimmung der Curie-Temperatur verschiedener Metalle oder Legierungen (Tab. 1). Bei der Curie-Temperatur (TC), auch als Curiepunkt bezeichnet, verliert eine Substanz ihre ferromagnetischen Eigenschaften.
Tab. 1: Ferromagnetische Metalle und Legierungen zur Kalibrierung von Thermowaagen pber die Curie-Tempertatur (TC) [6].
| Substanz | Zusammensetzung | TC [°C] |
|---|---|---|
| Alumel | 94,45% Ni; 1,98% Mn; 1,26% Al; 0,59% Co; 0,042% Mg; 0,021% Fe; 0,002% Cu; 0,001% Zr | 163 |
| Permenorm 3601 | 61% Fe; 37% Ni | 253 ± 5 |
| Nickel | 100% Ni | 351 ± 5 |
| Mumetall | 76,5% Ni; 15% Fe; 4,5% Cu; 3,3% Mo | 377 ± 6 |
| Permenorm 5000H3 | 51% Fe; 47,5% Ni | 451 ± 7 |
| Perkalloy | 74,74% Ni; 24,25% Fe; 50 ppm Si; 10 ppm Cu | 596 |
| Trapoferm N2 | 96,5% Fe; 2,8% Si | 750 ± 11 |
| Eisen | 100% Fe | 770 |
| Kobalt | 100% Co | 1131 |
Ferromagnetismus setzt den kristallinen Zustand einer Substanz voraus und unterscheidet sich vom Paramagnetismus dadurch, dass in mikroskopisch kleinen, als Weißsche Bezirke bezeichneten Kristallbereichen die magnetischen Momente der Atome durch spontane Magnetisierung gleichgerichtet sind [3]. Die Ausrichtung des magnetischen Momentes zwischen zwei Weißschen Bezirken ändert sich dabei nicht sprunghaft, sondern kontinuierlich über eine Distanz von 100 bis 1000 Gitterkonstanten, der Blochwand. Oberhalb der Curie-Temperatur wird die vorherrschende Ordnung aufgrund der stärkeren Bewegung der Atome zerstört, ein ferromagnetischer Stoff wird paramagnetisch. Je nachdem, ob vom ferromagnetischen oder paramagnetischen Zustand aus auf TC extrapoliert wird, erhält man die ferromagnetische Curie-Temperatur TC, oder die paramagnetische Curie-Temperatur TCp, wobei die letztere zumeist etwas höher liegt, was bei der Kalibrierung der Thermowaage zu beachten ist. Der Übergang von ferromagnetisch zu paramagnetisch ist ein Phasenübergang zweiter Art, bei dem sich zahlreiche weitere Eigenschaften der betreffenden Substanz ändern können, z. B. der elektrische Widerstand, die spezifische Wärme oder der thermische Ausdehnungskoeffizient.
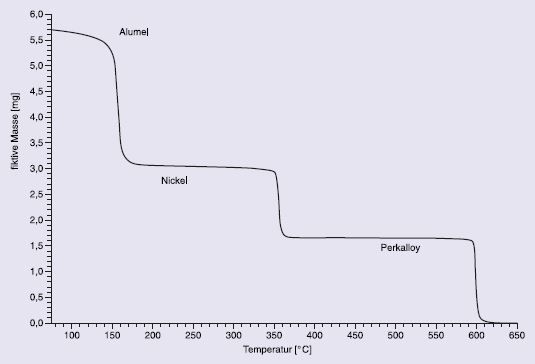
Bei der Temperaturkalibrierung werden zunächst die unterschiedlichen Standards in die Waagschale der Thermowaage überführt und dann die Waage auf "Null" tariert. Durch das Anbringen eines geeigneten Magneten unterhalb der Waage erhält man eine fiktive Probenmasse, welche allein auf der Anziehung zwischen Magnet und Probe beruht. Beim Überschreiten der Curie-Temperatur verschwindet diese fiktive Masse (Abb. 7).
Die Fehlergrenze einer auf der Curie-Temperatur beruhenden Kalibrierung liegt je nach Probe und Anlage bei ca. 5 °C. Die Curie-Temperatur für das vom Europäischen Arzneibuch vorgeschriebene Nickel wird in der Literatur mit 351,4 ± 4,8 °C angegeben [6].
sich gemeinsam auf der Waagschale und werden von einem Magneten nach unten gezogen. Bei Erreichen der Curie-Temperatur schwindet die Anziehungskraft und damit die fiktive Masse der Substanzen. Aus [6].
Kalibrierung der Masse
Die Kalibrierung der Masse erfolgt zumeist analog zu der einer normalen Analysenwaage mit geeichten Gewichten und elektronischem Abgleich. Das Europäische Arzneibuch schreibt hier die Auswertung des Hydratwasserverlustes von Calciumoxalat-Monohydrat CRS vor, das sich beim Erhitzen sukzessive zu Calciumoxalat, Calciumcarbonat und schließlich Calciumoxid umwandelt, was sich in einer stufenförmigen TG-Kurve zeigt (Abb. 4 zeigt). Die Abweichung sollte deutlich unter 0,5% betragen.
Fehlerquellen und Fallstricke
Probleme bei der Auswertung thermogravimetrischer Messungen sind zumeist durch die jeweilige Konstruktion der Thermowaage bedingt. Sie werden im folgenden skizziert.
Auftriebs- und Strömungseffekte
Ein Körper mit dem Volumen V erfährt in einem ihn umgebenden Medium die Auftriebskraft
Luft besitzt bei einem Luftdruck von 1013 hPa und einer Temperatur von 0 °C eine Dichte von 1,293 kg/m³, bei demselben Luftdruck und einer Temperatur 30 °C aber nur eine Dichte von 1,164 kg/m³. Die Luftdichte nimmt folglich bei dieser (für die TGA geringen) Temperaturdifferenz um rund 10% ab. Entsprechend nimmt der Auftrieb einer in Luft befindlichen Probe ab: Der Auftrieb einer 0,001 cm³ großen Probe wird bei 0 °C durch eine Masse von 0,1293 mg kompensiert, bei 30 °C aber durch eine Masse von nur 0,1164 mg. Bei 30 °C Lufttemperatur ist die Probe also scheinbar schwerer.
Ebenso übt strömendes Gas in der Thermowaage eine Kraft auf die Waagschale aus. Diese messbaren Strömungseffekte überlagern die scheinbare Massenzunahme durch den bei höheren Temperaturen geringeren Auftrieb, sodass sich eine scheinbare Massenabnahme ergibt. Aufgrund des geringfügigen Ausmaßes sind solche Effekte aber zumeist vernachlässigbar.
Eine weitere Fehlerquelle ist die Rohrströmung. Diese Konvektionsströmung, die den Spülgasfluss überlagert, hat ihre Ursache darin, dass an der beheizten Ofenwand heiße Luft aufsteigt, die im kälteren Teil des Ofens, meist in der Nähe der Probe, wieder absinkt.
Probenpackung und Probenmasse
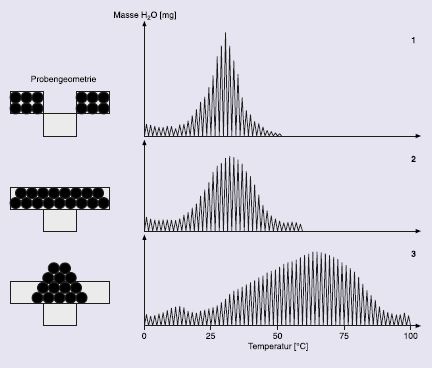
Die Packung, Schichtung oder Schüttung der Probe im Ofen kann sich ebenfalls auf das Messergebnis auswirken. Dies zeigt sich z. B. an der Geschwindigkeit der Dehydratation von Calciumoxalat-Monohydrat während der Erhitzung. Sie erfolgt im Idealfall gleichmäßig, kann aber durch eine ungünstige Packung der Probe behindert werden und deshalb ungleichmäßig verlaufen (Abb. 8) [1].
während der Erhitzung gleichmäßig (oben, Mitte) oder ungleichmäßig
(unten) dehydriert. Massenspektrometrische Messung. Aus [6].
Auch die Probenmasse beeinflusst den Verlauf einer TGA. Hohe Einwaagen verschieben die Ereignistemperatur hin zu höheren Temperaturen. Das Beispiel von Calciumoxalat-Monohydrat zeigt eine beachtliche Temperaturdrift in Abhängigkeit von der gewählten Einwaage, während der Einfluss der Einwaage auf den prozentualen Massenverlust nur gering ist (Tab. 2).
Tab. 2: Einfluss der Einwaage auf den prozentualen Massenverlust und die Curie-Temperatur (TC) bei den drei Stufen der thermischen Zersetzung von Calciumoxalat-Monohydrat. Heizrate: +10 °C/min.
| Einwaage | CaC2O4 * H2O → CaC2O4 | CAC2O4 → CaCO3 + CO | CaCo3 → CaO + CO2 |
|---|---|---|---|
Theoretischer Massenverlust | |||
| 12,32% | 29,06% | 61,62% | |
Massenverlust und TC | |||
| 0,509 mg | 12,24% – 168,7 °C | 32,72% – 484,2 °C | 63,56% – 671,0 °C |
| 3,139 mg | 12,09% – 186,6 °C | 31,39% – 504,5 °C | 61,86% – 727,8 °C |
| 4,136 mg | 12,00% – 191,6 °C | 31,47% – 516,2 °C | 61,81% – 730,1 °C |
| 8,052 mg | 12,09% – 201,1 °C | 31,53% – 514,0 °C | 61,71% – 756,0 °C |
Heizrate
Da Probe und Ofen nicht in direktem Kontakt miteinander stehen, erfolgt die Wärmeübertragung hauptsächlich durch Strahlung und Konvektion. Dies bedingt beim Durchlaufen von Temperaturprogrammen oft eine Temperaturdifferenz zwischen Ofen (Programm) und Probe. Die Probentemperatur hinkt der Programmtemperatur hinterher, und zwar umso mehr, je höher die Heizrate ist. Zudem benötigen die ablaufenden Prozesse auch eine gewisse Reaktionszeit. Zu hohe Heizraten führen daher zum "Überfahren" detektierbarer Abläufe.
Tab. 3: Einfluss von Heizrate und EInwaage auf den prozentualen Massenverlust und die Curie-Temperatur (TC) bei den drei Stufen der thermischen Zersetzung von Calciumoxalat-Monohydrat.
| Heizrate und Einwaage | CaC2O4 * H2O → CaC2O4 | CaC2O4 → CaCO3 + CO | CaCO3 → CaO + CO2 |
|---|---|---|---|
Theoretischer Massenverlust | |||
| 12,32% | 29,06% | 61,62% | |
Massenverlust und TC | |||
| 5,0 °C/min – 6,336 mg | 12,60% – 174,34 °C | 32,34% – 482,8 °C | 61,61% – 726,2 °C |
| 10,0 °C/min – 3,139 mg | 12,09% – 186,6 °C | 31,39% – 504,5 °C | 61,51% – 727,8 °C |
| 25,0 °C/min – 2,140 mg | 12,24% – 198,6 °C | 31,39% – 527,8 °C | 61,86% – 737,1 °C |
| 50,0 °C/min – 4,284 mg | 12,40% – 225,9 °C | 31,15% – 546,1 °C | 61,85% – 814,5 °C |
| 100,0 °C/min – 6,336 mg | 12,62% – 230,7 °C | 31,33% – 558,0 °C | 61,66% – 809,1 °C |
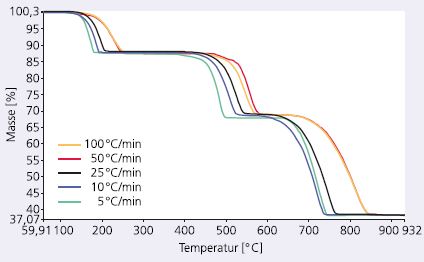
Die Curie-Temperatur wird durch eine hohe Heizrate zumeist deutlicher in Richtung höherer Temperatur verschoben als durch die Verwendung großer Probeneinwaagen. So wirken sich unterschiedlicher Temperaturgradienten auch auf die TGA von Calciumoxalat-Monohydrat aus, die das Europäische Arzneibuch zur Kalibrierung vorschreibt. Dass das EuAB dabei keine Heizrate vorgibt, ist vertretbar, da sich unterschiedliche Temperaturgradienten zwar deutlich auf die Ereignistemperatur, aber kaum auf die Stufenhöhe auswirken (Abb. 9, Tab. 3).
den Verlauf der Messkurven deutlich, die Stufenhöhe jedoch kaum.
Anwendungsbeispiele
In vielen Fällen kann die Thermogravimetrie eine sinnvolle Alternative zu klassischen Analysenverfahren sein. Ein großer Vorteil der TGA ist dabei, dass sie keine Reagenzien oder sonstige Chemikalien benötigt, denn damit entfällt auch deren Entsorgung.
Für die Bestimmung des Wassergehaltes diverser Substanzen bietet die TGA eine schnelle und genaue Alternative zur Trockenschrankmethode oder zur Karl-Fischer-Titration. So eignet sie sich hervorragend zur Messung des Wassergehalts von Stärke, der während der Lagerung teilweise erheblich abnimmt [4].
Das Wichtigste in Kürze
- Die Thermogravimetrie ist eine schnelle und einfache Methode zur Bestimmung von Massenänderungen einer Probe in Abhängigkeit von der herrschenden Atmosphäre und Temperatur.
- Zur Analyse werden nur kleine Probenmengen benötigt.
- Außer den zur Herstellung der gewünschten Atmosphäre benötigten Gasen sind keine weiteren Chemikalien erforderlich.
- Besonders geeignet ist die Thermogravimetrie zur Bestimmung von bei höherer Temperatur leichtflüchtigen Komponenten.
- Bei der Wassergehaltsbestimmung bietet sie eine schnelle und genaue Alternative zur IR-Waage, Trockenschrankmethode oder Karl-Fischer-Titration. Das EuAB 4 schreibt sie u. a. zur Bestimmung des Trockenverlustes der Vincaalkaloide vor.
- Zu beachten ist, dass Temperaturgradient, Probenschüttung und Probenmasse die Messwerte teilweise erheblich beeinflussen.
Unter bestimmten Voraussetzungen lassen sich mit Hilfe der Thermogravimetrie der Wasser- und Wirkstoffgehalt von Pulvermischungen simultan bestimmen. Ein Beispiel dafür ist die quantitative Bestimmung von Wasser und Coffein in einer Extrusionsmischung, die zu 90% aus Weißmaisstärke und zu 10% aus Coffein besteht. Hier weist die TG-Kurve zwei Stufen auf: Die erste Stufe entspricht dem Verdampfen des aus der Stärke stammenden Wassers, die zweite Stufe entspricht der Verflüchtigung des Coffeins, das oberhalb von 150 °C vollständig sublimiert [5].
Hubert Rein
Literatur
[1] Georg Schwedt: Analytische Chemie. Thieme, Stuttgart 1995, S. 163 ff.
[2] Wolfgang F. Hemminger, Heiko K. Cammenga: Methoden der Thermischen Analyse. Springer, Berlin 1989, S. 57 ff.
[3] Peter Rennert, Herbert Schmiedel, Christian Weißmantel: Kleine Enzyklopädie der Physik. VEB Bibliographisches Institut,
Leipzig 1988, S. 87, 361 f.
[4] Hubert Rein: Mikroverkapseln mit Stärke. Diss. Marburg 1993, S. 37ff.
[5] Hubert Rein: Extrudierte orale Arzneiformen auf Stärkebasis. Habilitationsschrift, Bonn 2004, S. 74 ff.
[6] Hubert Rein, in: Kommentar zum Europäischen Arzneibuch (Ph. Eur. 4.00), Bd. 1, Monographie 2.2.34 Thermogravimetrie. WVG Stuttgart 2004 (16. Lieferung).
[7] Georg Widmann: Interpretation von TGA-Kurven. Mettler Toledo UserCom, Nr. 13, 1, 2001, S. 1 ff.
[8] Berthold Göber, Peter Surmann: Arzneimittelkontrolle. WVG Stuttgart 2005, S. 346 ff.




























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.