
- DAZ.online
- News
- Pharmazie
- Aus Sicherheitsgründen...
Überprüfung durch den PRAC bis September
Aus Sicherheitsgründen – Metamizol verliert Zulassung in Finnland
Stuttgart - 11.07.2024, 09:15 Uhr

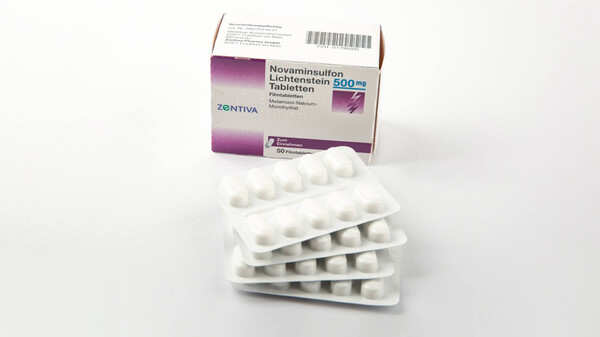
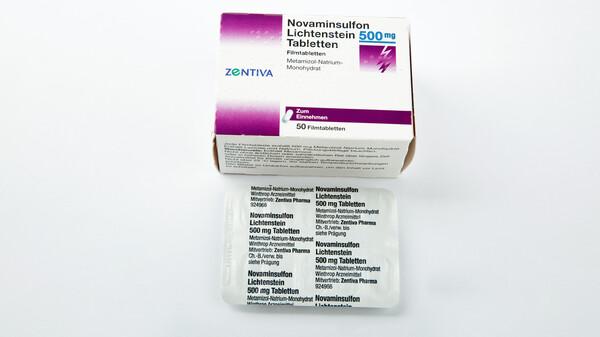
Metamizol ist in Europa unter vielen verschiedenen Handelsnamen erhältlich, darunter etwa: Analgin, Berlosin, Novalgin und Novaminsulfon. (Foto: Semi / AdobeStock)
Agranulozytose gilt als seltene, aber gefürchtete Nebenwirkung des in Europa weit verbreiteten Schmerzmittels Metamizol. In Finnland hat sich nun der Zulassungsinhaber des einzigen dort verfügbaren Präparates aus Sicherheitsgründen dazu entschieden, auf dessen Zulassung zu verzichten. Was das für das Nutzen-Risiko-Verhältnis aller Metamizol-Präparate in Europa bedeutet, überprüft nun der europäische Pharmakovigilanzausschuss (PRAC).
Am 14. Juni berichtete das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), dass in Finnland dem dort einzigen zugelassenen Metamizol-haltigen Arzneimittel die Zulassung entzogen werden soll. Der Zulassungsinhaber habe sich aus Sicherheitsgründen für diesen Schritt entschieden.
Zudem hat die finnische Arzneimittelbehörde auch beim europäischen Pharmakovigilanzausschuss PRAC eine Sicherheitsüberprüfung von Metamizol (Novaminsulfon) initiiert – es geht um das bereits gut bekannte Risiko einer Agranulozytose. Laut BfArM wird Metamizol in Europa bereits seit den 1920er Jahren eingesetzt, die Maßnahmen zur Minimierung des Agranulozytose-Risikos seien jedoch von Land zu Land unterschiedlich. Alle Metamizol-haltigen Arzneimittel seien in den entsprechenden Ländern national zugelassen (in Deutschland, Österreich, Belgien, Bulgarien, Kroatien, Tschechische Republik, Ungarn, Italien, Lettland, Litauen, Luxemburg, Niederlande, Polen, Portugal, Rumänien, Slowakei, Slowenien und Spanien).
Mehr zum Thema
Vorsicht Nebenwirkungen
Wird Metamizol zu häufig verordnet?
Im Dezember 2022 war in Deutschland im „Bulletin zur Arzneimittelsicherheit“ darauf hingewiesen worden, dass die Verordnungszahlen von Metamizol trotz der bekannten Risiken hoch seien und kontinuierlich steigen würden. Mit den Verordnungszahlen würden auch die Meldungen von Agranulozytosefällen (mit vermutetem Zusammenhang zu Metamizol) steigen, hieß es. Problematisch in diesem Zusammenhang sei vor allem, dass Metamizol auch bei Indikationen eingesetzt wird, für die der Wirkstoff nicht zugelassen ist. Beispielsweise bei Kopf-, Zahn- oder Rückenschmerzen ist Metamizol nicht indiziert.
Eine Agranulozytose könne auch bereits nach kurzfristiger Anwendung von Metamizol auftreten. Bei jedem Verdacht auf das Vorliegen einer Agranulozytose sei die Behandlung mit Metamizol sofort zu beenden, hieß es.
Finnland hatte Warnhinweise vor kurzem verschärft
In Finnland waren mit Warnhinweisen auf der Außenverpackung und mittels Patientenkarten die Maßnahmen zur Risikominimierung erst vor kurzem (2021) verschärft worden. Da dennoch weiterhin Agranulozytose-Fälle gemeldet wurden, wurde nun das PRAC-Verfahren eingeleitet.
Aus der Meldung Finnlands an den PRAC geht hervor, dass es sich bei dem betroffenen finnischen Präparat um ein Kombinationspräparat aus Metamizol und Pitofenon handelt (Handelsname Litalgin, Tabletten oder Injektionslösung). Zugelassen war es in Finnland seit 1966 zur Behandlung von Kolikschmerzen und Blasenkrämpfen. Das Spasmolytikum Pitofenon ist laut Lauer-Taxe (Stand: 10.07.2024) in deutschen Fertigarzneimitteln aktuell nicht enthalten.
Risiko von Land zu Land unterschiedlich?
Finnland gibt in seiner Meldung an den PRAC zu bedenken, dass – obwohl das Agranulozytoserisiko lange bekannt ist – die Inzidenz dieser schweren Nebenwirkung nicht geklärt sei. Es gebe Unterschiede zwischen den Ländern, die sich durch verschiedene Risikomaßnahmen, die unterschiedliche Nutzung, aber auch durch eine unterschiedliche Empfänglichkeit für die Nebenwirkung je nach Ethnizität erklären lassen könnten. Das Risiko für schwerwiegende Infektionen infolge einer Agranulozytose könne durch Indikationen wie Koliken erhöht sein, wenn den Schmerzen bereits eine Infektion zugrunde lag.
Mit einer abschließenden Einschätzung des PRAC zu diesen Fragen ist im September 2024 zu rechnen.
Laut dem Nachrichtenportal „Arznei-Telegramm“ ist Metamizol in Ländern wie Großbritannien, den USA, Kanada oder Australien bereits seit Jahrzehnten nicht mehr im Handel. Der „Spiegel“ berichtete am 20. Juni, dass in Europa bald das letzte Werk für die Metamizol-Herstellung schließen soll.
Mehr zum Thema




























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.