
- DAZ.online
- News
- Spektrum
- Deuterierung vereinfachen...
Isotopen-Austausch
Deuterierung vereinfachen: Wie Arzneimittel länger im Körper bleiben
Düsseldorf - 20.01.2023, 12:15 Uhr

In sogenannten Schlenkgefäßen werden neue luft- und wasserempfindliche Katalysatoren unter Schutzgasatmosphäre hergestellt und gelagert. (Foto: LIKAT / Nordlicht)
Eine junge Forscherin am Leibniz-Institut für Katalyse in Rostock hat eine günstigere Methode entwickelt, in organischen Molekülen Wasserstoffatome durch das schwerere Isotop Deuterium auszutauschen. Arzneimittel erhalten so etwa eine höhere Halbwertszeit im Körper, bevor sie abgebaut werden.
„Normale“ Wasserstoffatome bestehen nur aus einem einzelnen Proton (weshalb sie auch Protium genannt werden) und einem Elektron. Kommt ein Neutron hinzu, ist dies chemisch betrachtet immer noch Wasserstoff – Deuterium aber, wie dieses Isotop des Wasserstoffs genannt wird, verändert die physikalischen Eigenschaften. Auch dann, wenn das Deuterium in einem komplexen organischen Molekül gebunden ist. Mehr Masse macht dabei nicht nur deuterierte Verbindungen schwerer als ihre Protium-Analoga, sondern auch träger in vielen Reaktionen. Man spricht dabei von einem „kinetischen Isotopeneffekt“.
Mehr zum Thema

Wie sich Erkenntnisse der Chronopharmakologie nutzen lassen
Arzneimitteltherapie im Takt
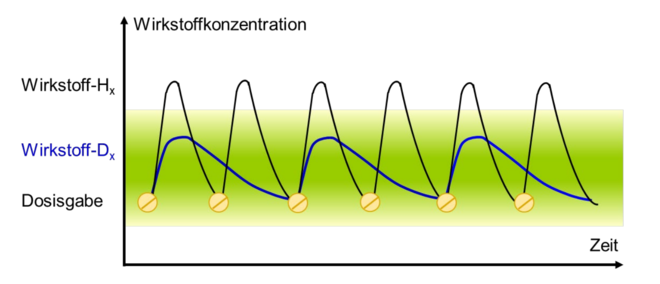
Bereits seit einigen Jahren weiß man, dass das für deuterierte Arzneimittel unter anderem bedeutet, dass sie länger im Körper verweilen, weil sie langsamer verstoffwechselt werden. Das hat zur Folge, dass solche „schweren“ Arzneimittel in geringerer Dosierung gegeben werden können oder auch seltener eingenommen werden müssen. Für manche Verbindungen, die bislang als Therapeutikum nicht infrage kamen, weil sie schneller abgebaut werden als sie eine Wirkung entfalten könnten, bedeutet eine Deuterierung überhaupt erst einen möglichen sinnvollen Einsatz.
Erstes deuteriertes Arzneimittel 2017 zugelassen
Bereits im Jahr 1970 gab es erste Patente auf deuterierte Moleküle. Ein erstes deuteriertes Arzneimittel erhielt allerdings erst im Jahr 2017 eine Zulassung durch die US-amerikanische FDA (die US Food and Drug Administration). Deutetrabenazin ist ein Arzneimittel zur Behandlung der erblichen Nervenkrankheit Chorea Huntington. Gegenüber dem bereits zuvor zugelassenen Wirkstoff Tetrabenazin, der analog ist, hat Deutetrabenazin eine längere Halbwertszeit. Seitdem gibt es aber nur wenige weitere deuterierte Wirkstoffe, die sich derzeit in verschiedenen Phasen der Erforschung befinden – allerdings wird ihnen eine große Zukunft vorhergesagt und es gab bereits millionenschwere entsprechende Patentgeschäfte in der Pharmabranche. Interessanterweise machen sich manche Autoren auch bereits Gedanken um die Auswirkungen „schwerer“ Drogen.
Ein Grund aber, warum deuterierte Arzneimittel noch ein Nischendasein führen, ist ihre Herstellung, die noch teuer und aufwändig ist. Deuterium ist auf der einen Seite ein seltenes Isotop – Verfahren es zu gewinnen und aufzureinigen sind damit die eine Herausforderung, Herstellungsprozesse zu vergünstigen die nächste. Erst im April 2022 veröffentlichten etwa Forscher der TU Dresden ein Verfahren im Fachmagazin Science, um Deuterium aus Wasserstoff einfach herauszufiltern.
Günstigere Katalysatoren, günstigeres Substrat
Die andere Herausforderung ist, das Deuterium statt des Protiums in die Wirkstoffmoleküle zu bekommen. Eine Synthese etwa mit schwerem Wasser von vorneherein wäre möglich, aber sehr teuer. Schweres Wasser ist Wasser, bei dem die Wasserstoffmoleküle des Wassers (H2O) durch Deuterium ersetzt sind, also D2O. Stattdessen nutzt man katalytische Methoden, um einzelne Wasserstoffatome durch Deuteriumatome auszutauschen. Die bisherigen Methoden nutzen dabei insbesondere das seltene Edelmetall Iridium als Katalysator und recht teures Deuteriumgas (D2 – also Wasserstoffgas, bei dem die Atome aus Deuterium bestehen) als Substrat.
Methoden, diesen gezielten Austausch günstiger und einfacher zu machen, werden von Forschern intensiv gesucht. Nachdem bereits im Jahr 2021 Forscher der Uni Bonn eine für einige Moleküle anwendbare Methode im Fachmagazin „Angewandte Chemie“ vorgestellt haben, bei der sie mit Titan und Epoxiden etwa deuterierte Vorstufen von Ibuprofen herstellen konnten, hat jetzt eine junge Forscherin am Leibniz-Institut für Katalyse in Rostock (LIKAT) in ihrer Dissertation möglicherweise den Weg zu einer einfacheren und universelleren Methode eröffnet. Ihre Ergebnisse veröffentlichen Dr. Sarah Kopf und die Forscher ihrer Arbeitsgruppe am LIKAT jetzt im Fachmagazin Chemical Reviews.
Eine katalytische C-H-Aktivierung mit schwerem Wasser statt Deuterium als Substrat und den Metallen Ruthenium und Mangan als Katalysatoren sind das, was Kopf in zwei Jahren Forschung zu ihrer Dissertation entwickeln konnte. Günstiger was das Katalysatormaterial anbelangt und mit einem im Vergleich zum herkömmlichen Verfahren günstigeren Substrat. „Ruthenium kommt häufiger als Iridium vor, ist gut erforscht und bietet in Sachen C-H-Aktivierung viel Literatur“, sagt Kopf. Mangan gebe es in großen Vorkommen, es ähnele in seinen Eigenschaften dem Eisen, sei ähnlich kostengünstig, nicht-toxisch, und gerate in der Fachwelt immer stärker in den Fokus, weil es einen Weg in Richtung „grüne Chemie“ öffne, sagt sie.
Durchbruch mit dirigierenden funktionellen Gruppen
Der Durchbruch bei ihrer Forschung sei ihr aber erst gelungen, als es ihr gelang, funktionelle Gruppen wie Keto- oder die Aldehyd-Gruppe zu nutzen, um den katalytischen Deuterium-Austausch zielgerichtet zu steuern. „Der Trick besteht darin, weitere Strukturen im Molekül sozusagen als Dirigenten zu verwenden, welche die entsprechenden C-H-Gruppen und den Katalysator zusammenbringen“, erklärt Kopf. „Je mehr Gruppen ich als Dirigenten in den Molekülen zugänglich machen kann, desto mehr Pharmazeutika kann ich dann mittels Deuterium ‚labeln‘“, sagt sie. So eigne sich die neue Isotopenaustausch-Methode für breite Anwendungsfelder. Diese Steuerung der Reaktion bezeichnen Chemiker auch mit dem Begriff „transient directing groups“.
Noch sei die Methode aber ein gutes Stück von einer möglichen praktischen Anwendung entfernt. Ein Nachteil sei die noch benötigte Reaktionstemperatur: „Aufgrund der recht hohen Temperaturen, die für die Deuterierungsreaktionen mit Ruthenium und Mangan nötig sind – von 100 bis 120 Grad Celsius –, ist die Anwendung dieser Methoden auf Moleküle begrenzt, die unter diesen Bedingungen stabil sind. Aus ähnlichen Gründen wären kürzere Reaktionszeiten wünschenswert. Möglicherweise können solche und andere Limitationen durch die Entwicklung neuer Katalysatorgenerationen behoben werden, was dann zu einer breiteren Anwendbarkeit führen könnte. Wo nach eventuellen Verbesserungen der Systeme dann die Grenzen liegen werden, ist schwer vorherzusagen“, erklärt die Chemikerin. Ideal sei es, die Methode so zu verbessern, dass 40 Grad Celsius oder sogar Raumtemperatur genügen würden.
Insofern seien die nun entwickelten Methoden bisher zunächst ein Beitrag zur Grundlagenforschung, sagt Kopf. „Der Hauptfokus unserer Methode ist weniger die großtechnische Anwendung und vielmehr die Synthese von deuterierten Verbindungen in kleinerem Maßstab für Anwendungen in der medizinischen Chemie, aber auch hier sind die Arbeiten erst einmal als Grundlagenforschung zu verstehen“, sagt sie. Als Leibniz-Institut verstehe man sich allerdings als „an der Schnittstelle von Grundlagenforschung und Anwendung verortet“. Das bedeute, dass Ergebnisse aus der Grundlagenforschung schnellstmöglich über einen Pilotmaßstab in die Anwendung transferiert werden sollen. Die Zusammenarbeit mit geeigneten Projektpartnern – etwa aus der Pharmaindustrie –, die über die finanziellen Mittel verfügen, ein Verfahren „upzuscalen“, sei sehr bedeutsam, erklärt LIKAT-Sprecherin Martha Höhne dazu.
Forschungskollegen veröffentlichten weitere Methode für Arene und Heteroarene
„Tests für Deuterierungen in größerem Maßstab wurden für die von uns entwickelten Reaktionen bisher nicht durchgeführt, weshalb uns entsprechende Daten, zum Beispiel im Hinblick auf Katalysatorstabilität und Wiederverwendbarkeit nicht zur Verfügung stehen. Aussagen über die großtechnische Anwendbarkeit unserer Methoden können wir deshalb bisher nicht treffen. Vermutlich wäre die Entwicklung von neuen Katalysatorgenerationen hierfür notwendig. Eine andere, in der gleichen Arbeitsgruppe entwickelte Methode, wurde schon in größerem Maßstab getestet“, sagt Kopf.
Bei dieser Methode, die ihre Forschungskollegen im Fachmagazin Nature veröffentlichten, lassen sich Arene und Heteroarene wie Anilin, Phenol, Indol und andere durch nanostrukturierte Eisenkatalysatoren mit D2O deuterieren.
„Für die Synthese von deuterierten Arzneistoffen werden zurzeit aufwendige mehrstufige Synthesen durchgeführt, also eine gänzlich andere Methode als die, an der wir arbeiten“, erklärt Kopf. „Im Hinblick auf Fortschritte in der Skalierung von direktem H-D-Austausch ist es aber denkbar, dass dieser direkte H-D-Austausch in einigen Jahren auch auf technischem Maßstab möglich sein wird. Ob diese Methode aber letztendlich von Pharmafirmen für die Produktion von deuterierten Arzneistoffen verwendet wird und die mehrstufige Synthese ersetzen kann und inwiefern unsere Beiträge dabei eine Rolle spielen, ist schwer abzuschätzen und hängt wahrscheinlich auch von finanzieller Risikobereitschaft und Interesse der Pharmaindustrie ab“, sagt die Chemikerin, die ihre Dissertation mit dem höchstmöglichen Prädikat „summa cum laude“ verteidigte.
Weitere Forschung auch zu Deuterierung von Aliphaten
Die rutheniumkatalysierte Methode von Kopf würde sich dabei grundsätzlich auch eignen, andere Atome statt Deuterium mit dem Wasserstoff auszutauschen. Das sei bereits von anderen Forschungsgruppen gezeigt worden. „Für die mangankatalysierte Methode haben wir solche Anwendungen bisher erfolglos getestet. Es ist aber denkbar, dass andere Funktionalisierungsreaktionen als Deuterierungen unter Mangankatalyse mit ‚transient directing groups‘ in Zukunft gefunden werden“, sagt Kopf.
Mit ihrer weiteren Forschung will die Forscherin zum einen das Verfahren weiter verbessern, aber auch das Spektrum noch erweitern. „Die Vielzahl an in Pharmazeutika vorkommenden Strukturen erfordert auch eine Vielzahl an Reaktionen, um verschiedene Substrate umsetzen zu können. Bisher haben wir uns auf die Deuterierung vor allem von aromatischen Strukturen konzentriert. Wir arbeiten nun daran, Deuterierungsmethoden für aliphatische Moleküle als Substrate zu entwickeln, um Zugang zu weiteren deuterierten Strukturen zu ermöglichen“, sagt Kopf.




























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.