
- DAZ.online
- News
- Politik
- Zolgensma: Kassen fordern...
Teuerstes Arzneimittel der Welt
Zolgensma: Kassen fordern Härtefallprogramm auf Herstellerkosten
Berlin - 19.11.2019, 06:59 Uhr
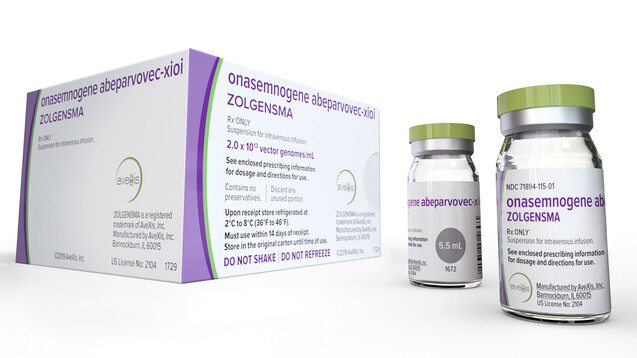
Zolgensma muss man nur ein Mal anwenden – dafür kostet es knapp zwei Millionen Euro. In der EU ist das neue Gentherapeutikum noch nicht zugelassen, doch die Kassen sind bereits alarmiert. (b/Foto: Novartis/AP Photo)
Blaupause für weitere neue Arzneimittel?
Die Unterzeichner halten das derzeit zu beobachtende Vorgehen aus vielerlei Hinsicht für bedenklich: Unter anderem wegen der Unsicherheiten zu Wirksamkeit und Sicherheit und den erheblichen haftungsrechtlichen Risiken für den behandelnden Arzt bei einem Einzelimport. Zudem fürchten sie, dass die aktuelle Entwicklung mit Zolgensma® eine „Blaupause“ für weitere neue Arzneimittel sein könnte, die eine entsprechende relevante Marktpenetration noch vor Zulassung anstreben – „und damit nicht nur die Zulassung, sondern auch die Verfahren des Gemeinsamen Bundesausschuss wie auch zum geregelten Erstattungsbetrag aushebeln“.
Grundsätze für ein verbindliches Verfahren
Vor diesem fordern Kassen und G-BA ein verbindliches Verfahren für den Einsatz von Zolgensma®. So müsse die Indikationsstellung sehr kritisch im konkreten Einzelfall gestellt werden und dabei die bestehende Behandlungsalternative berücksichtigt werden. Die Indikationsstellung müsse durch Experten im Benehmen mit dem Medizinischen Dienst der Krankenversicherung erfolgen. Zudem dürften die Arzneimittelabgabe und die weitere Therapie ausschließlich in hochspezialisierten Zentren stattfinden, die Behandlungsverläufe seien zu dokumentieren. Die Rahmenbedingungen für eine qualitätsgesicherte Anwendung der komplexen Gentherapie seien zeitnah durch den G-BA unter Berücksichtigung der zuständigen Fachgesellschaften festzulegen. Grundsätzlich dürften nicht zugelassene Arzneimittel nur in den Fällen zulasten der GKV verordnet werden, bei denen unmittelbare Lebensgefahr ohne erfolgversprechende Alternativtherapie besteht (vgl. § 2 Abs. 1a SGB V). Nicht zuletzt fordern die Unterzeichner den Hersteller Novartis zu einem Härtefallprogramm zu verpflichten. Denn die Kostentragung für eine Anwendung nicht zugelassener Arzneimittel liege im Verantwortungsbereich des Herstellers. Solle das Arzneimittel vor der europäischen Zulassung verabreicht werden, könne dies nur im Rahmen eines Härtefallprogramms erfolgen, bei dem unter Studienbedingungen eine qualitätsgesicherte Anwendung gesichert werde.
Da zu erwarten sei, dass die vorliegende Konstellation in der näheren Zukunft erneut auftreten wird, regen die Kassen und ihre Mitstreiter an, diese Grundsätze, insbesondere die Verpflichtung der Hersteller, ein Härtefallprogramm aufzulegen, gesetzlich zu regeln.
Damit würde perspektivisch für alle Beteiligten Klarheit über das Vorgehen bestehen. Die Sicherstellung und Finanzierung qualitativ hochwertiger Arzneimitteltherapie muss auf dem Stand des medizinischen Wissens und der gesetzlichen Vorgaben erfolgen und darf nicht in die Abhängigkeit von Pressekampagnen abgleiten“.
Auszug aus dem Brief des AOK-BV, des BKK-Dachverbands, des vdek, der Knappschaft Bahn-See, des IKK e.V., der SVLFG, des GKV-Spitzenverbands, des G-BA und des Verbands der Universitätsklinika Deutschlands an Gesundheitsminister Jens Spahn.
Spahn möge daher kurzfristig seine Erwartung an den Einsatz von Zolgensma® im Sinne der genannten Grundsätze äußern – und entsprechend auf das anbietende Pharmaunternehmen einwirken.




























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.