
- DAZ.online
- DAZ / AZ
- DAZ 8/2018
- Update HPV-Schutz
Krebsprophylaxe
Update HPV-Schutz
Impfempfehlung ausgeweitet – Zervixkarzinom-Screening-Programm geändert
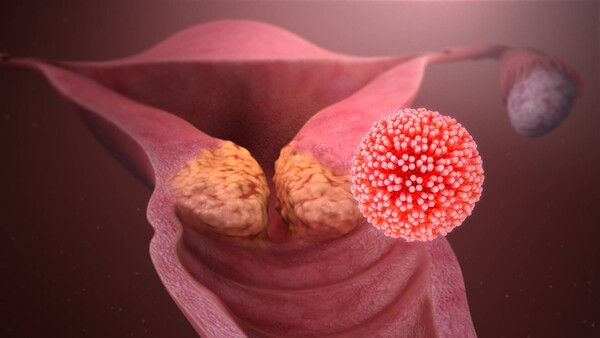
Der Mediziner Harald zur Hausen hatte als erster nachgewiesen, dass HP-Viren Gebärmutterhalskrebs verursachen können. Dafür erhielt er 2008 den Nobelpreis für Medizin oder Physiologie. Mittlerweile sind mehr als 200 verschiedene HPV-Typen bekannt, die die Haut und Schleimhäute befallen können. Etwa 40 von ihnen sind sexuell übertragbar – wahrscheinlich nur über engen Hautkontakt und Schleimhautzellen, jedoch nicht über Sperma, Speichel oder Blut. Man teilt sie in Niedrig- und Hochrisikotypen ein:
- Niedrigrisikotypen wie HPV 6 und 11 rufen vor allem Feigwarzen (Condylomata acuminata) – die häufigste sexuell übertragbare Erkrankung in Deutschland – hervor.
- Dagegen induzieren Hochrisikotypen (vor allem HPV 16 und 18) Tumoren wie Gebärmutterhalskrebs und anogenitale Karzinome (an Anus, Vagina, Vulva und Penis) bzw. ihre Vorstufen.
Weniger bekannt ist, dass HPV-Infektionen auch in anderen Körperregionen zu Krebserkrankungen führen können, vor allem im Oropharynx, dem Übergangsbereich zwischen Mundhöhle und Rachen.
Immunsystem wehrt Viren meist ab
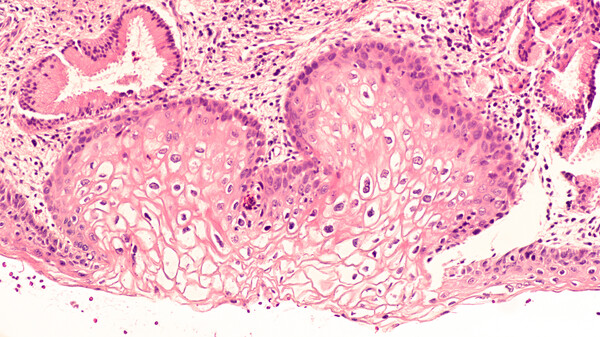
Schätzungen zufolge infizieren sich 70 bis 80 Prozent der sexuell aktiven Frauen im Laufe ihres Lebens mit HPV. Bei den meisten bleibt die Infektion asymptomatisch und heilt vollständig aus. Persistieren die Viren, weil z. B. das Immunsystem sie nicht eliminieren kann, entwickeln sich in der Schleimhaut des Gebärmutterhalses zervikale intraepitheliale Neoplasien (CINs), insbesondere nach Infektion mit Hochrisikotypen. Bilden sich die CINs nicht von selbst zurück, kann sich daraus ein Tumor entwickeln. Ob dies geschieht, hängt vom Vorhandensein weiterer Risikofaktoren ab. Als solche wurden Rauchen, andere Genitalinfektionen (z. B. mit Chlamydien), Immunschwäche, eine langjährige hormonelle Kontrazeption sowie genetische Faktoren identifiziert.
HPV-Impfung kann vor vielen Krebsarten schützen
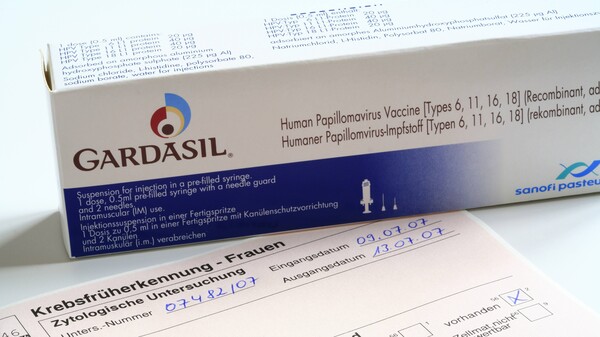
Die seit rund zehn Jahren verfügbaren HPV-Impfstoffe können daher nicht nur vorm Zervixkarzinom, sondern auch vor anderen Krebsarten schützen. Die Zulassungen decken diese Indikationen bereits ab. Der 2006 zugelassene tetravalente Impfstoff Gardasil® enthält nichtinfektiöse virusähnliche Partikel (virus-like particles, VLPs) der HPV-Typen 6, 11, 16 und 18. VLPs sind leere Virushüllen ohne virale DNA, die somit keine Infektion verursachen, aber das Immunsystem zur Bildung spezifischer Antikörper stimulieren können. Gardasil ist seit August 2017 in Deutschland nicht mehr erhältlich. An seine Stelle ist mit gleicher Indikation (s. u.) das 2015 zugelassene nonavalente Gardasil® 9 getreten, das vor neun HPV-Typen schützen kann (6, 11, 16, 18, 31, 33, 45, 52 und 58). Die HPV-Typen 31, 33, 45, 52 und 58 werden für 15 bis 20 Prozent aller Zervixkarzinome verantwortlich gemacht.
Gardasil 9 ist ab einem Alter von neun Jahren zugelassen zur Prävention von Vorstufen maligner Läsionen im Genitalbereich (Zervix, Vulva und Vagina) und im Analbereich sowie von Zervix- und Analkarzinomen, die durch bestimmte onkogene HPV-Typen (s. o.) hervorgerufen werden. Außerdem kann es zur Verhinderung von Genitalwarzen (Condylomata acuminata) eingesetzt werden.
Seit 2007 ist das bivalente Cervarix® zugelassen, das VLPs der HPV-Typen 16 und 18 enthält. Es ist ebenfalls ab einem Alter von neun Jahren mit den gleichen Indikationen zugelassen.
Auch Jungen sollten geimpft werden
Cervarix und Gardasil 9 sind für Mädchen und Jungen, Frauen und Männer zugelassen. Die STIKO empfiehlt jedoch derzeit eine generelle HPV-Impfung nur für Mädchen im Alter von neun bis 14 Jahren. Diese Empfehlung löste die vorherige, zwischen 2007 und 2014 gültige Empfehlung mit einem Impfalter von zwölf bis 17 Jahren ab.
Die sächsische Impfkommission (SIKO) hatte bereits 2013 eine Impfempfehlung auch für männliche Jugendliche veröffentlicht. Experten befürworten, diese Empfehlung deutschlandweit auszusprechen. Denn die Durchimpfungsrate bei den Mädchen sei noch zu gering, als dass Jungen von einem Herdenschutz profitieren könnten – und homosexuell orientierte männliche Jugendliche können davon ohnehin nicht profitieren.
HPV-Impfempfehlungen der STIKO
Aktuell empfiehlt die Ständige Impfkommission:
- HPV-Impfung für alle Mädchen von 9 bis 14 Jahren
- versäumte Impfungen spätestens bis zum vollendeten 18. Lebensjahr (d. h. vor dem 18. Geburtstag) nachholen (die gesetzlichen Krankenkassen erstatten die Kosten einer versäumten Impfung bis zum Alter von 17 Jahren)
- die Impfserie sollte vor dem ersten Geschlechtsverkehr beendet sein
- bei Impfbeginn im Alter von 9 bis 14 Jahren: 2-Dosen-Impfschema mit Impfabstand von fünf Monaten
- bei Impfungen im Alter über 14 Jahren oder zu geringem Impfabstand zwischen 1. und 2. Dosis: 3. Dosis erforderlich
- die Impfserie möglichst mit dem gleichen Impfstoff durchführen
- gegebenenfalls auch ungeimpfte Frauen über 17 Jahren impfen; individuelle ärztliche Nutzen-Risiko-Abschätzung notwendig
Effektivität der Impfung
Die Zulassungsstudien und weitere Untersuchungen hatten gezeigt, dass die verfügbaren Impfstoffe bei der Verhinderung von Infektionen durch die darin enthaltenen HPV-Typen sehr effektiv sind (Cervarix: 83,5%, Gardasil 9: 96,7%). Langzeitstudien mit geimpften Mädchen und Frauen, die im Median sechs Jahre lang nachbeobachtet wurden, gaben keine Hinweise darauf, dass der Impfschutz nachlässt. Wäre dies dennoch der Fall, müssten Auffrischimpfungen in Erwägung gezogen werden.
Die Durchimpfungsrate der Mädchen liegt gegenwärtig bei ca. 40 Prozent und ist im internationalen Vergleich niedrig. Beispielsweise ist sie in Australien und Großbritannien doppelt so hoch, da dort die Immunisierung in Schulen erfolgt. Rund vier Jahre nach Einführung der Impfung beobachtete man in Australien bei jungen Frauen 40 Prozent weniger Neuerkrankungen an Zervixkarzinom-Vorstufen und eine 90-prozentige Verringerung des Auftretens von Genitalwarzen.
Da die Inzidenz der HPV-assoziierten Tumorerkrankungen im deutschen Krebsregister erfasst wird, lässt sich mithilfe langfristiger epidemiologischer Studien beobachten, wie die HPV-Impfung zu ihrer Verringerung beiträgt. So hat eine Arbeitsgruppe um Dr. Nina Buttmann-Schweiger vom Robert Koch-Institut (RKI) berechnet, wie viele HPV-bedingte Tumoren verhindert werden könnten, wenn alle Mädchen die Impfempfehlung befolgen würden. Dabei fokussierten die Wissenschaftler nicht nur auf das Zervixkarzinom, sondern auf alle HPV-assoziierten Tumoren, also auch Plattenepithelkarzinome des Anus, der Vagina, der Vulva, des Penis sowie des Oropharynx. Von den im Jahr 2013 im Krebsregister erfassten Tumoren waren 1,6 Prozent HPV-assoziiert – 6239 bei Frauen und 1358 bei Männern. Bei den Frauen waren es meistens Zervixkarzinome (70,9%), bei den Männern oropharyngeale Tumoren (46,9%).
Da die HPV-Impfempfehlung erst im Jahr 2007 ausgesprochen wurde, erwarten die Autoren eine Auswirkung auf die Krebsinzidenz nicht vor 2023, wenn die ersten geimpften Frauen das 35. Lebensjahr erreicht haben. Das Monitoring des Effekts der HPV-Impfung auf die Krebsinzidenz ist also ein langfristiges Projekt.
Schätzungen zufolge könnten in den Industrieländern insgesamt 120.000 neue Krebserkrankungen pro Jahr durch HPV-Impfungen von Mädchen und Frauen sowie Jungen und Männern verhindert werden.
Zahlen und Fakten
Alle zwei Jahre veröffentlicht das Robert Koch-Institut in Berlin die Publikation „Krebs in Deutschland“, die von der Gesellschaft der epidemiologischen Krebsregister in Deutschland (GEKID) und dem Zentrum für Krebsregisterdaten (ZfKD) gemeinsam erarbeitet wird. Anfang Dezember 2017 erschien die 11. Ausgabe, die auf Daten des deutschen Krebsregisters bis zum Jahr 2014 beruht.
Danach erkrankten an Gebärmutterhalskrebs (Zervixkarzinom) im Jahr 2014 etwa 4540 Frauen. Diese Zahl ähnelt denen der letzten zehn Jahre. Die höchsten Erkrankungsraten weisen derzeit die 35- bis 59-jährigen Frauen auf. An einem Zervixkarzinom sterben zurzeit jährlich etwa 1540 Frauen; vor 30 Jahren waren es noch mehr als doppelt so viele. Nach der Diagnose eines invasiven Gebärmutterhalstumors beträgt die relative 5-Jahres-Überlebensrate 69 Prozent. Dank der Früherkennungsmaßnahmen wird mehr als jedes zweite invasive Karzinom bereits in einem frühen Stadium (T1) diagnostiziert.
Neues Screening-Programm: HPV-DNA-Test ergänzt Pap-Test
Die STIKO weist in ihren Empfehlungen darauf hin, dass die HPV-Impfung Früherkennungsmaßnahmen nicht ersetzen kann, da sie nur vor den häufigsten Hochrisiko-HP-Viren schützt. Bisher bietet das Screening-Programm für Gebärmutterhalskrebs der gesetzlichen Krankenkassen Frauen ab 20 Jahren die Möglichkeit, jährlich einen Pap-Test durchführen zu lassen (zytologische Untersuchung eines Zellabstrichs vom Gebärmutterhals; benannt nach George Nicholas Papanicolaou, dem Erfinder dieses Tests). Die Teilnahme am Pap-Test ist freiwillig und erfolgt ohne Einladung.
Anfang dieses Jahres wurde ein neues Screening-Programm eingeführt. Grundlage dafür ist das im April 2013 verabschiedete „Gesetz zur Entwicklung der Krebsfrüherkennung und zur Qualitätssicherung durch klinische Krebsregister“ (Krebsfrüherkennungs- und -registergesetz, KFRG), das die Etablierung eines strukturierten und qualitätsgesicherten Screening-Programms fordert. Das neue Screening-Programm beinhaltet folgende Hauptpunkte:
- Frauen im Alter von 20 bis 60 Jahren werden alle fünf Jahre von ihren Krankenkassen angeschrieben und über das Zervixkarzinom-Screening informiert.
- Frauen im Alter von 20 bis 34 Jahren können wie bisher einmal jährlich den Pap-Test in Anspruch nehmen.
- Frauen ab 35 Jahren wird künftig (statt dem jährlichen Pap-Test) alle drei Jahre eine Kombination aus Pap-Test und molekularem HPV-Test (HPV-DNA-Test) angeboten.
Auch beim HPV-DNA-Test wird ein Abstrich vom Gebärmutterhals im Labor untersucht. Keiner der beiden Tests ist hundertprozentig zuverlässig, sodass sowohl falsch-negative als auch falsch-positive Ergebnisse auftreten können. Der HPV-DNA-Test besitzt eine höhere Sensitivität. Studien zufolge kann er um 60 bis 70 Prozent besser vor einem invasiven Zervixkarzinom schützen als der Pap-Test. Er kann auch eingesetzt werden, um bei jüngeren Frauen ein auffälliges Pap-Test-Ergebnis abzuklären. Eine Unterscheidung zwischen „nur“ infizierten Frauen und bereits erkrankten Frauen ist mit dem HPV-DNA-Test nicht möglich.
Screening nach Risiko stratifizieren?
In den Niederlanden wurde der HPV-DNA-Test bereits im Januar 2017 in das Screening-Programm für Gebärmutterhalskrebs aufgenommen. Auch in England könnte das in naher Zukunft der Fall sein. Vor diesem Hintergrund beschäftigten sich die medizinische Statistikerin Dr. Rebecca Landy und ihr Team (Queen Mary University, London) in einer Untersuchung mit der Frage, ob beim Screening eine Risiko-Stratifizierung je nach dem HPV-Impfstatus sinnvoll sein könnte, um Kosten zu sparen. Mithilfe eines Simulationsmodells fanden sie heraus, dass bei Frauen, die den bivalenten HPV-16/18-Impfstoff erhalten hatten, drei Früherkennungsuntersuchungen pro Lebenszeit ausreichend sind, um ein Zervixkarzinom zu verhindern. Bei Frauen, die mit dem nonavalenten Impfstoff vakziniert wurden, würden sogar nur zwei solche Untersuchungen genügen. Dagegen sollte man nicht HPV-geimpften Frauen siebenmal in ihrem Leben eine Screening-Untersuchung anbieten.
Um eine derartige Individualisierung durchführen zu können, müsste den Krankenkassen der Impfstatus bekannt sein und in die entsprechenden Datenbanken, auf deren Grundlage die Einladungen zur Früherkennungsuntersuchung verschickt werden, eingearbeitet werden, betonen die Autoren. In Deutschland ist eine Risiko-Stratifizierung in Screening-Programmen derzeit noch kein Thema. |
Quellen
Robert Koch-Institut (Hrsg). Krebs in Deutschland für 2013/2014, Gemeinsame Publikation des Zentrums für Krebsregisterdaten und der Gesellschaft der epidemiologischen Krebsregister in Deutschland e. V., 11. Ausgabe 2017
Fachinformationen von Cervarix und Gardasil 9
Empfehlungen der Ständigen Impfkommission (STIKO) am Robert Koch-Institut 2017/2018. Epidemiologisches Bulletin Nr. 34/2017, 24. August 2017
Einladungsschreiben und Entscheidungshilfen zum Zervixkarzinom-Screening – Abschlussbericht. Stand 29.09.2017. IQWiG-Berichte Nr. 548; www.iqwig.de
Einladung und Entscheidungshilfe Zervixkarzinom-Screening: IQWiG legt finale Fassung vor. www.iqwig.de, Pressemitteilung vom 24.11.2017
Gille G et al. HPV-induzierte Kondylome, Karzinome und Vorläufer-Läsionen – eine interdisziplinäre Herausforderung. Dtsch Med Wochenschr 2014;139:2405-10
Beachler DC et al. Multisite HPV16/18 vaccine efficacy against cervical, anal, and oral HPV infection. J Natl Cancer Inst 2016;108(1)
Joura EA et al. A 9-valent HPV vaccine against infection and intraepithelial neoplasia in women. N Engl J Med 2015;372(8):711–723
Saraiya M et al. US assessment of HPV types in cancers: implications for current and 9-valent HPV vaccines. J Natl Cancer Inst 2015;107(6):djv086
Deleré Y et al. Effektivität und Dauer des Impfschutzes gegen humane Papillomviren. Dtsch Arztebl Int 2014;111:584-91
Landy R et al. What cervical screening is appropriate for women who have been vaccinated against high risk HPV? a simulation study. Int J Cancer 2018;142(4):709-718
Buttmann-Schweiger N et al. Cancer incidence in Germany attributable to human papillomavirus in 2013. BMC Cancer 2017;17:682
S3-Leitlinie zur Impfprävention HPV-assoziierter Neoplasien. Stand 31.12.2013, gültig bis 31.12.2018, AWMF-Reg.-Nr. 082/002
Robert Koch-Institut (Hrsg). Impfung gegen humane Papillomviren (HPV) bei Mädchen. Faktenblatt zu KiGGS Welle 1: Studie zur Gesundheit von Kindern und Jugendlichen in Deutschland – Erste Folgebefragung 2009 – 2012. RKI, Berlin 2015; www.kiggs-studie.de


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.