
- DAZ.online
- DAZ / AZ
- DAZ 7/2013
- Längeres Überleben ...
Arzneimittel und Therapie
Längeres Überleben durch Angiogenesehemmung
Das kolorektale Karzinom gehört mit weltweit etwa 1,2 Millionen Neuerkrankungen im Jahr 2008 zu den häufigsten Krebsarten [1]. Dr. Mark Sievert, Berlin, betonte im Rahmen einer von Sanofi Aventis unterstützten Pressekonferenz in Berlin die Bedeutung einer frühzeitigen Diagnose. So liegt die Heilungsrate bei einem kolorektalen Karzinom im Stadium I bei circa 95%, im Stadium IV nur noch bei 10%. Erschwerend ist die Tatsache, dass in frühen Stadien die Symptome weniger stark ausgeprägt sind, sodass bei Diagnose ein Viertel der Patienten bereits ein metastasiertes kolorektales Karzinom (mCRC) aufweist. Die Leitlinien empfehlen zur Erst-Linien-Therapie bei mCRC das FOLFOX-Regime, eine Kombination aus 5-Fluorouracil, Leucovorin und Oxaliplatin, sowie das FOLFIRI-Regime, bestehend aus 5-Fluorouracil, Leucovorin sowie Irinotecan in Kombination mit Bevacizumab [3, 4, 5, 20].
Tumorwachstum durch Angiogenese
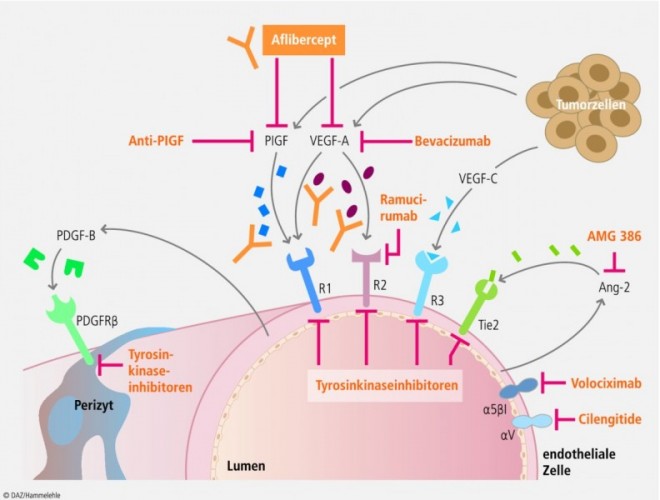
Ab einer Gesamtgröße von etwa 2 mm3 benötigt ein Tumor eigene Anbindungen an das Gefäßsystem, um den Eigenbedarf an Sauerstoff und Nährstoffen zu decken. Die hierfür notwendige Neubildung von Blutgefäßen wird als Angiogenese bezeichnet [6, 7]. Während seiner Wachstumsphase wuchert der Tumor häufig über die Kapazität seiner Gefäßversorgung hinaus und führt in minderversorgten Bereichen zur Expression proangiogenetischer Faktoren [8, 9]. Die Regulierung der Angiogenese erfolgt hauptsächlich über die Familie der vaskulären endothelialen Wachstumsfaktoren (VEGF, vascular endothelial growth factor). Diese umfasst insgesamt sechs Liganden: VEGF-A, -B, -C, -D und -E, den plazentaren Wachstumsfaktor (PIGF) sowie drei korrespondierende Rezeptoren: VEGFR-1, -2 und -3 [9]. Über einen Tyrosinkinase-gekoppelten Signalweg werden Proliferation, Differenzierung sowie Migration von Endothelzellen und somit die Neubildung des Gefäßsystems induziert [10, 11].
Die ZulassungsstudieDie randomisierte, placebokontrollierte, multinationale und multizentrische Phase-III-VELOUR-Studie (Aflibercept Versus Placebo in Combination FOLFIRI in the Treatment of Patients with Metastatic Colorectal Cancer after Failure of an Oxaliplatin Based Regimen) sollte die Wirksamkeit von Aflibercept als Zweit-Linien-Therapie bei Patienten mit metastasiertem kolorektalem Karzinom (mCRC) nachweisen, die vorher mit einem Oxaliplatin-haltigen Regime behandelt wurden. 1226 Patienten erhielten neben dem FOLFIRI-Regime zusätzlich Placebo (n = 612), bzw. Aflibercept (4 mg/kg KG alle zwei Wochen; n= 614) [12, 17, 18]. Der primäre Endpunkt der Studie war das Gesamtüberleben. Die sekundären Endpunkte umfassten progressionsfreies Überleben, Gesamtansprechrate und Sicherheit. Patienten mit zusätzlicher Aflibercept-Therapie zeigten ein verlängertes medianes Gesamtüberleben (13,5 versus 12,06 Monate), sowie eine erhöhte Ansprechrate (20% versus 11%) im Vergleich zur Kontrolle [17]. Außerdem war eine signifikante Verlängerung des progressionsfreien Überlebens von 4,67 Monaten auf 6,90 Monate zu beobachten. Unerwünschte Ereignisse, wie Diarrhoe, Fatigue, Stomatitiden, Infektionen, Hypertonie, abdominale Schmerzen, Neutropenie und Proteinurie waren in der mit Aflibercept behandelten Gruppe teilweise um ein Vielfaches erhöht [14]. 27% dieser Patienten brachen die Studie vorzeitig ab, in der Placebo-Gruppe lag die Abbruchrate bei 12% [17]. |
Angiogenese-Hemmstoffe
Zytotoxische Chemotherapeutika und Angiogenese-Inhibitoren zeigen unterschiedliche Wirkmechanismen und Toxizitätsprofile, sodass deren Kombination zu einer besseren Wirksamkeit ohne eine Erhöhung der Toxizität führen kann [12]. Prof. Dr. Stefan Kubicka, Chefarzt der medizinischen Klinik I im Klinikum am Steinenberg, erklärte, dass im Vergleich zu Chemotherapeutika bei Angiogenese-Hemmstoffen mit einer geringen Resistenzentwicklung zu rechnen sei. Zytotoxische Substanzen schädigen genetisch instabile Tumorzellen, wohingegen Angiogenese-Hemmstoffe auf gesunde Endothelzellen mit wesentlich geringerer Mutationsrate einwirken.
Die Hemmung von vaskulären endothelialen Wachstumsfaktoren führe nicht nur zur Antiangiogenese, sondern könne auch durch Normalisierung des Gefäßbettes die Diffusion von Chemotherapeutika zum Tumor erhöhen. Zudem halten Fachleute die Anwendung von Angiogenese-Hemmern über die Zeit der Chemo- oder Strahlentherapie hinaus für sinnvoll. Die Antiangiogenese-Therapie führt nicht zur Kumulation von unerwünschten Wirkungen, wie dies bei Chemotherapien der Fall ist, da die Angiogenese kein ständiger Prozess im Körper ist, sondern nur bei Vorgängen wie Wundheilung und Wachstum benötigt wird.
Bisher gibt es mehrere Optionen, mit denen die Gefäßneubildung gehemmt werden kann. Cetuximab (Erbitux®, Bristol-Myers Squibb & Merck KGaA), ein chimärer monoklonaler Antikörper, sowie Panitumumab (Vectibix®, Amgen), ein humaner monoklonaler Antikörper, sind gegen den Rezeptor des epidermalen Wachstumsfaktors (EGF, epidermal growth factor) gerichtet. Bevacizumab (Avastin®, Roche), ein humanisierter monoklonaler Antikörper, verhindert durch Bindung an VEGF-A die Wechselwirkung mit dessen Rezeptoren.
Die Gabe von Bevacizumab zu einer zytotoxischen Chemotherapie, die meistens aus dem FOLFOX- oder FOLFIRI- Regimen besteht, ist in vielen Leitlinien zur Erst-Linien-Therapie anerkannt [20]. Diese Kombination verlängert bei Patienten mit metastasiertem kolorektalen Karzinom das progressionsfreie Überleben (PFS, Progression Free Survival) um etwa ein Jahr sowie das Gesamtüberleben (OS, Overall Survival) auf etwa zwei Jahre [13, 14, 15, 16].
Eine weitere Möglichkeit, die Angiogense zu hemmen, bieten Tyrosinkinase-Inhibitoren. Regorafenib (Stivarga®, Bayer AG) wurde im September 2012 von der FDA zur Therapie des mCRC zugelassen. Aufgrund der hohen strukturellen Homologie der Tyrosinkinase-Rezeptoren greifen die meisten Tyrosinkinase-Inhibitoren oft nicht spezifisch an das gewünschte Target an [12]. Diese unspezifische Hemmung führe zu breiteren Wirkungen, erhöhe aber leider auch die Toxizität, so Prof. Dr. Ralf-Dieter Hofheinz, Leiter des Tagestherapiezentrums am Interdisziplinären Tumorzentrum Mannheim.
Aflibercept bei AMDAflibercept ist seit Dezember 2012 unter der Bezeichnung Eylea® (Bayer Pharma AG) als intravitreale Injektion zugelassen zur Behandlung der neovaskulären (feuchten) altersabhängigen Makuladegeneration (AMD). Die feuchte AMD zeichnet sich durch eine pathologische choroidale Neovaskularisation (CNV) aus. Treten Blut und Flüssigkeit aus den pathologischen choroidalen Gefäßen aus, kommt es zu einer Netzhautverdickung oder einem Netzhautödem, was zum Verlust der Sehschärfe führen kann. Aflibercept als löslicher Köderrezeptor für VEGF-A und PlGF hemmt die Aktivierung der VEGF-Rezeptoren und damit das pathologische Gefäßwachstum. Nach intravitrealer Injektion von Aflibercept verringerten sich die Netzhautdicke und die mittlere CNV-Läsionsgröße, das Sehvermögen blieb erhalten. |
Besonderheiten von Aflibercept
Aflibercept (Zaltrap®) ist ein rekombinantes Fusionsprotein, das aus der konstanten Region des humanen Immunglobulin IgG1 und der extrazellulären Domäne der humanen VEGFR-1 und -2 besteht und mit hoher Affinität VEGF-A und -B sowie den plazentaren Wachstumsfaktor (PIGF) bindet.
Da Bevacizumab ausschließlich VEGF-A inhibiert, kann durch Hochregulierung weiterer Wachstumsfaktoren die Hemmung teilweise kompensiert werden. Dieser Mechanismus ist bei Aflibercept nicht zu erwarten. Denn Aflibercept hemmt zusätzlich VEGF-B und PIGF, sodass die Kompensationsmöglichkeiten eingeschränkt sind. Aflibercept ist somit prinzipiell ein effektiverer VEGF-Inhibitor, als Bevacizumab. Mit dieser Dreifach-Blockade wird auch die Wirksamkeit von Aflibercept bei Patienten erklärt, die auf eine Bevacizumab-Therapie nicht mehr ansprechen.
Tipps für die PraxisPatienten mit einer Aflibercept-Therapie werden vermutlich meist von auf Onkologie spezialisierten Apotheken versorgt werden. Es lohnt sich besonders die Nebenwirkungen zusammen mit dem Patienten zu beobachten und bei Verdacht auf ernsthafte Probleme eine weitergehende Diagnose anzuraten. Bei den leichteren unerwünschten Wirkungen hingegen sollte der Patient zum Durchhalten der Therapie motiviert werden. |
DAZ-Interview
Aflibercept erfolgreich in der Zweit-Linien-Therapie
Mit dem rekombinanten Fusionsprotein Aflibercept steht eine neue Option für das kolorektale Karzinom zur Verfügung, die das Überleben der Patienten nach vorheriger Oxaliplatin-Behandlung statistisch signifikant verlängern kann. Wir sprachen mit Prof. Dr. med. Ralf-Dieter Hofheinz, leitender Arzt des TagesTherapieZentrums (TTZ) am Interdisziplinären Tumorzentrum Mannheim (ITM) Universitätsmedizin Mannheim, Universität Heidelberg, über die Vor- und Nachteile des neuen Antikörper.
DAZ: Warum wird Aflibercept gerade für diese Indikation eingesetzt?
Hofheinz: Aflibercept wurde auch in anderen randomisierten Studien untersucht. Jedoch ist die VELOUR-Studie mit Patienten mit metastasiertem kolorektalem Karzinom die erste positive Phase-III-Studie, sodass Aflibercept nun für die Zweit-Linien-Therapie beim Kolonkarzinom eingesetzt wird.
DAZ: Was sollte man bei der Anwendung von Aflibercept beachten?
Hofheinz: Aflibercept besitzt zwei Arten von Nebenwirkungen. Zum einen werden die durch die Chemotherapie bedingten Nebenwirkungen wie zum Beispiel Diarrhö, Mukositis und Stomatitis verstärkt. Zum anderen resultiert die spezifische Hemmung von VEGF, insbesondere in Blutdruckanstieg, Proteinurie, verzögerte Wundheilung, Blutungen sowie in sehr seltenen Fällen in arteriellen Thromboembolien. Blutungen sind relativ häufig, allerdings handelt es sich hierbei zumeist um leichte Schleimhautblutungen. Es sollten aber vier Wochen Abstand zwischen größeren Operationen und einer Therapie mit Aflibercept eingehalten werden. In der Regel wird die Anwendung von Aflibercept nicht durch kleinere Operationen behindert.
DAZ: Welche Vorteile sehen Sie bei Aflibercept im Vergleich zu Bevacizumab?
Hofheinz: Aflibercept besitzt theoretisch ein breiteres Wirkspektrum als Bevacizumab, da nicht nur vaskuläre endotheliale Wachstumsfaktoren (VEGF), sondern auch der plazentare Wachstumsfaktor (PIGF) blockiert wird und damit auch Wirksamkeit nach Vorbehandlung mit Bevacizumab besteht. Es gibt derzeit jedoch noch keine Vergleichsstudien zwischen Aflibercept und Bevacizumab. Daher kann man bisher nur Daten von Aflibercept und Bevacizumab aus getrennten Studien vergleichen. Die Ergebnisse der VELOUR-Studie deuten aber darauf hin, dass insbesondere Patienten, die von einer Tumorverkleinerung profitieren, einen Vorteil durch den Einsatz von Aflibercept erhalten, wohingegen Patienten mit weniger aggressiv verlaufenden Erkrankung durchaus mit Bevacizumab weiterbehandelt werden können.
DAZ: Wie beurteilen Sie die Chancen für Aflibercept in der Tumortherapie?
Hofheinz: Das theoretisch breitere Wirkspektrum und die Tatsache, dass Aflibercept zur Remission führt, lassen auf gute Marktchancen schließen. Zudem gibt es bisher sehr positive Erfahrungen nach der Zulassung von Zaltrap® in den USA. Die hauptsächliche Behandlungssituation wird zunächst in der Zweit-Linien-Therapie sein. Aflibercept stellt eine Bereicherung des Therapiespektrums dar und ermöglicht eine differenziertere ZweitLinien-Therapie.
DAZ: Bei Bevacizumab wird die marginale Lebenszeitverlängerung von wenigen Wochen kritisch gesehen. Dies scheint bei Aflibercept auch der Fall zu sein. Wie schätzen Sie ein verlängertes medianes Überleben von wenigen Wochen oder Monaten ein?
Hofheinz: Der Fortschritt von Aflibercept besteht in der gleichen Größenordnung wie bei den anderen molekulargezielten Substanzen. Im Mittel wird das Gesamtüberleben um sechs bis acht Wochen verlängert. Wir haben aber auch Patienten, die noch nach 20 bis 30 Monaten von einer Aflibercepttherapie profitieren. Leider gibt es noch keinen prädiktiven Marker für Angiogenesehemmstoffe. Daher kann noch nicht im Voraus gesagt werden, welche Patienten besonders von der Therapie mit Aflibercept profitieren werden.
DAZ: Es wird diskutiert, dass die Angiogenesehemmung das Wachstum aggressiver Tumorzellen fördern kann. Sehen Sie auch diese Gefahr?
Hofheinz: Es gibt durchaus präklinische Daten, die diese Hypothese nahelegen. Wenn man sich jedoch die klinischen Daten anschaut, kann diese Annahme nicht bestätigt werden. Wir haben bisher nicht den Eindruck, dass nach Beendigung einer Angiogenesetherapie deutliche Metastasierungstendenzen auftreten.
DAZ: Herr Professor Hofheinz, vielen Dank für das Interview!
Apothekerin My Hanh Nguyen

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.