
- DAZ.online
- DAZ / AZ
- DAZ 38/2009
- Die Halbwertsdauer – ...
Debatte
Die Halbwertsdauer – ein vergessener Parameter
In den meisten Lehrbüchern der Pharmakologie für Mediziner wird bislang der Begriff "Halbwertsdauer" bzw. "Half value duration" nicht beschrieben. Dagegen wird im (von Pharmazeuten primär für Pharmaziestudenten geschriebenen) "Lehrbuch der Klinischen Pharmazie" von U. Jaehde et al. (2003) die Halbwertsdauer anschaulich erklärt.
Halbwertsdauer ist keine Halbwertszeit!
Die Halbwertsdauer darf nicht mit der Eliminationshalbwertszeit verwechselt werden. Unter der Halbwertszeit versteht man den Zeitraum, in dem die Arzneistoffkonzentration im Blut bzw. Organismus um 50% abgenommen hat. Daraus folgt, dass nach etwa fünf Halbwertszeiten die Substanz nahezu vollständig eliminiert ist und entsprechend, dass eine Dosisänderung erst nach etwa fünf Halbwertszeiten den neuen Gleichgewichtszustand erreicht hat. Die Halbwertszeit ist abhängig vom Verteilungsvolumen und der Clearance und damit auch eine körpereigene Variable. Das heißt, die Halbwertszeit ist umso länger, je größer das Verteilungsvolumen und je kleiner die Clearance des Patienten ist. Die Halbwertszeit ist einer der wichtigsten pharmakokinetischen Parameter. Deshalb ist die Halbwertszeit zu Recht in der Roten Liste für jedes aufgeführte Präparat im blau eingefärbten "Verzeichnis chemischer Kurzbezeichnungen von Wirkstoffen" angegeben.
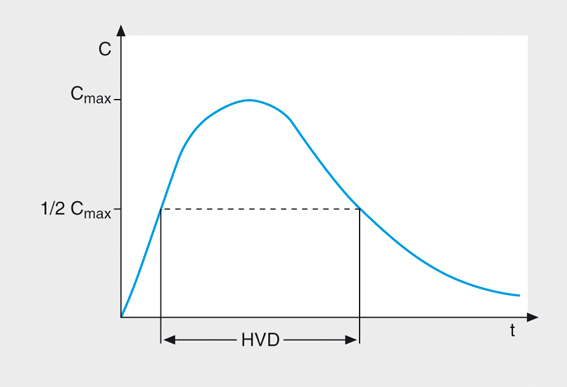
Dagegen ist die eher unbekannte Größe Halbwertsdauer ein Wert, der nur für die Beurteilung der Qualität einer Retardformulierung bedeutsam ist. Die wissenschaftlichen Mitarbeiter J. Meier, E. Nüesch und R. Schmidt der Pharmazeutischen For-schungs- und Entwicklungsabteilung von der Sandoz AG in Basel/Schweiz führten 1974 diesen Begriff ein [1]. Sie definierten die Halbwertsdauer (HWD) als den Zeitraum, in dem die Pharmakonkonzentration von peroral applizierten Retardpräparaten über der halbmaximalen Konzentration (≥ 50% Cmax) liegt (Abb. 1). Das bedeutet, die HWD gibt das Zeitfenster an, in dem im Blut mindestens die halbmaximale Konzentration des Wirkstoffs vorhanden ist. Um im deutschsprachigen Raum Verwechslungen mit der Halbwertszeit zu vermeiden, könnte die Halbwertsdauer auch als "Halbe Cmax -Dauer" (HCD) bezeichnet werden. Die HWD wird mittels sog. Single-dose-Studien (Einmalapplikation) bestimmt.
Zwar wurde in den achtziger Jahren von vorwiegend niederländischen Arbeitsgruppen versucht, höhere Plateauwerte wie etwa T80 (mindestens 80% der maximalen Konzentration) [2] oder die sog. Plateauzeit mit ≥ 75% Cmax einzuführen [3], doch fanden diese Vorschläge kaum Verbreitung.
Kinetische Parameter und Schmerztherapie
Prinzipiell kann für jedes Retardpräparat die HWD bestimmt werden. Die Erstbeschreiber hatten als Beispiel mit Dibenzepin ein retardiertes Antidepressivum gewählt. Bei zahlreichen Therapieregimen, wo ein vorzeitiges Absinken der Arzneistoff-Plasmakonzentration dem Patienten schaden kann (z. B. Depressionen, Infektionen, Anfallsleiden, Herz-Kreislauf-Erkrankungen oder chronische Schmerzen), sollte die Kenntnis der HWD obligat sein.
Beispiel retardierte Opioide
Am Beispiel der peroralen Therapie mit retardierten Opioiden bei Patienten mit chronischen Schmerzen soll die klinisch relevante Bedeutung verschiedener pharmakokinetischer Parameter im Folgenden detaillierter dargestellt werden.
Die Retardierung von Opioiden soll primär die analgetische Wirkdauer verlängern und dadurch die Einnahmefrequenz verringern und somit die Compliance verbessern. Zusätzlich soll die verzögerte Freisetzung durch Verringerung der Fluktuationen, etwa von hohen Plasmakonzentrationen, die Rate von unerwünschten Wirkungen senken.
Die Halbwertsdauer ist ein Kriterium für die Güte der betreffenden Retardformulierung hinsichtlich der Dauer der Wirkstoff-Freisetzung, nicht dagegen für das Ausmaß der Konzentrationsschwankungen im Plasma bei einer Dauertherapie, den sog. Fluktuationen.
PTF-Wert
Zur quantitativen Bestimmung dieser Fluktuationen dient üblicherweise der sog. PTF-Wert (Peak Trough Fluctuation), der möglichst niedrig sein sollte
PTF-Wert [%] = [(C max – C min ) x 100 / C Mittelwert ] .
Der PTF-Wert wird nach Erreichen des Steady-State-Zustandes eines Pharmakons mittels Multiple-dose-Studien bestimmt [4].
Erst stabile Opioidplasmaspiegel (d. h. möglichst geringe und insbesondere langsame Konzentrationsänderungen) erlauben eine wirksame Schmerztherapie – auch bei nicht Tumor-bedingten Schmerzen – ohne das Risiko einer iatrogen induzierten psy-chischen Abhängigkeit, sprich Opioidsucht. Denn anders als beim Junkie mit seinen Plasmaspitzen beim i.v. Heroin-Spritzen wird das dopaminerge Belohnungssystem (Sucht) durch einen relativ konstanten Opioidspiegel kaum aktiviert. Deshalb dominiert unter diesen Bedingungen die analgetische Wirkung der Opioide. Da die Maxime einer geringen Fluktuationsrate des Plasmaspiegels eine "Conditio sine qua non" für eine dauerhafte Opioidtherapie beim chronischen Schmerzpatienten darstellt, ist der PTF-Wert der "wichtigere" Parameter im Vergleich zur Halbwertsdauer. Wohl deshalb erfüllen alle zugelassenen retardierten Opioidpräparate mehr oder weniger zufriedenstellend dieses Axiom und vereinzelt machen die Hersteller sogar Angaben zum PTF-Wert in den Fach-Infos der Roten Liste (z. B. PTF-Wert: 119.9 ± 35.3% für Morphin-ratiopharm® retard und Morph® Sandoz).
Halbwertsdauer und End-of-dose-Schmerzen
Entsprechend dem "By-theclock"-Prinzip der WHO muss eine ausreichend lange Wirkung des retardierten Opioids zwischen den einzelnen Dosisgaben gewährleistet sein. Wenn aber die Zeitdauer des analgetisch wirksamen Plasmaspiegels wesentlich geringer als das vom Hersteller deklarierte Dosierungsintervall ist, kann es zu einer Art von Durchbruchschmerz, dem sog. End-of-dose-Schmerz kommen. Bei Tumorschmerzpatienten beträgt diese Form des vorzeitigen Verlustes der Opioidanalgesie etwa 30% der Durchbruchschmerzen [5]. Eine unzureichende Galenik kann an diesen End-of-dose-Schmerzen beteiligt sein.
Da die Halbwertsdauer einen Rückschluss darauf gestattet, ob zwischen den vorgesehenen Einnahmezeitpunkten ausreichende Wirkstoffspiegel gegeben sind, kann die Beachtung der HWD bereits bei der Auswahl der Präparate das Risiko dieser Schmerzform mindern.
Nach einer Untersuchung im Jahr 2008 liegt die Halbwertsdauer von mehreren Morphinpräparaten (30 mg) mit angeblicher 12-Stunden-Wirkdauer meist zwischen 5,5 bis 6,3 Stunden (Tab. 1). Nur Morphin-HCL Krewel® zeigte mit 8,3 Stunden eine ausreichende HWD [6].
| Tab 1. Halbwertsdauer von Opioid-Retardpräparaten mit 2-mal täglicher Einnahme. Die Bestimmung erfolgte meist händisch aus mittleren Plasmaspiegelverläufen. Die Angaben für Morphinpräparate beziehen sich in der Regel auf 30 mg-Darreichungsformen nach Nüchterneinnahme (Kapanol ® 50 mg). [K. Güttler: Opioide auf dem Prüfstand. Dtsch. Apothek. Zeitg. 148: 69–73; 2008] | |||
| Wirkstoff | Retardpräparat | Anbieter | Halbwerts- dauer (HWD) [h] |
| Morphin | Morphanton® Retard Tbl. | Juta Pharma | 5,5 |
| Morphin | M-beta® Tbl. | betapharm | 5,5 |
| Morphin | Morphin Hexal® Tbl. | Hexal | 5,5 |
| Morphin | Morphin AL retard Tbl. | Aliud Pharma | 5,5 |
| Morphin | Morphin-Puren® Tbl. | Actavis | 5,5 |
| Morphin | Morphin-ratiopharm® retard Tbl. | ratiopharm | 5,6 |
| Morphin | Morphinsulfat-GRY® Tbl. | Teva/Gry | 5,6 |
| Morphin | Capros® Kps. | Medac | 5,8 |
| Morphin | M-long® Kps. | Grünenthal | 5,8 |
| Morphin | MST® Retardtabletten | Mundipharma | 6,3 |
| Morphin | M-STADA® retard Tbl. | Stada-Arzneimittel | 6,3 |
| Morphin | Morphin-HCI Krewel® Tbl. | Krewel Meuselbach | 8,3 |
| Morphin | Kapanol® Kps. | GlaxoSmithKline | 13,0 |
| Oxycodon | Oxycodon-HCI-ratiopharm® | ratiopharm | 9,4 |
| Oxycodon | Oxygesic® | Mundipharma | 10,9 |
| Hydromorphon | Palladon® retard | Mundipharma | 6,9 |
Bei Opioidpräparaten mit angegebenen 24-stündigem Einnahmeintervall liegen für Morphin (60 mg; MST Continus® bzw. Capros® 1x tägl.) die Werte der Halbwertsdauer zwischen 7,4 bis 12,7 bzw. 8,8 Stunden. Deutlich länger dagegen ist die HWD bei Oros-Hydromorphon (Jurnista®). Durch die besondere Galenik der Oros-Technologie wird nahrungsunabhängig eine Halbwertsdauer von ca. 30 Stunden erreicht [7]. Das bedeutet, eine lange HWD ermöglicht ein längeres Dosierungsintervall.
In einer doppelblinden Cross-over-Studie mit zwei unterschiedlich retardierten Mor-phin-Präparaten für die zweimal bzw. einmal tägliche Einnahme (MS Contin® vs. MS Contin XL® ; Purdue Pharma, Kanada) an Tumorschmerzpatienten waren die Fluktuationen beim Zwölf-Stunden-Dosierungsintervall signifikant größer als bei einmal täglicher Gabe (179 ± 41,3% vs. 94 ± 28,8%), obwohl die Patienten die gleiche Morphin-Tagesgesamtdosis erhielten [8].
Daraus folgt, bei Retardpräparaten sind die Fluktuationen geringer, wenn bzw. obwohl Dosis und Dosierungsintervall größer sind. Dies steht im Gegensatz zum Fluktuationsverhalten der Plasmakonzentrationen von nicht retardierten Arzneimitteln. Denn da sind die Fluktuationen umso geringer, je kleiner Dosis und Intervall sind [9].
Aufgrund der direkten Korrelation von HWD und Dosierungsintervall ergibt sich, dass HWD und Fluktuationen invers korrelieren. Das heißt: je größer die HWD, umso geringer die Fluktuation. Diese Beziehung gilt über die Bedeutung des Dosierungsintervalls hinaus, denn bei einmal täglicher Einnahme hat Jurnista® (HWD: ca. 30 Std.) einen PTF-Wert von ca. 39% [10], aber bei ebenfalls einmal täglicher Einnahme hat zum Beispiel das retardierte Carbamazepinpräparat Carbaflux® mit einer HWD von ca. 60 Std. nur einen PTF-Wert von 0,7 ± 0,2%.
Ist eine lange HWD ein Intoxikationsrisiko?
Insbesondere bei Arzneimitteln, die eine HWD aufweisen, die länger als das vorgegebene Dosierungsintervall ist (z. B. Kapanol® , Jurnista®), stellt sich die Frage, inwieweit diese Diskrepanz zur Kumulation und letztlich Intoxikation führen kann.
Wie die meisten Arzneistoffe werden auch die Opioide proportional zu ihrer Plasmakonzentration eliminiert (sog. Kinetik Erster Ordnung). Das bedeutet, gemäß dem Massenwirkungsgesetz wird bei höheren Plasmakonzentrationen entsprechend mehr vom Arzneistoff eliminert. Weil außerdem im oberen Dosisbereich keine Sättigung der abbauenden Enzyme eintritt (Übergang in die sog. Kinetik Nullter Ordnung) wie etwa bei Phenytoin oder Acetylsalicylsäure, besteht im Rahmen von therapeutischen Dosierungen keine Intoxikationsgefahr bei HWD-Werten, die größer sind als das Applikationsintervall (z. B. Kapanol® , Jurnista®).
Vielmehr resultiert dann ein Plasmaspiegelverlauf, der dazu beiträgt, die Fluktuationen des Plasmaspiegels zu verringern (s. o.). Natürlich kann gegebenenfalls das Dosierungsintervall auch kostengünstig verlängert werden.
Absoluter Cmax-Wert: für HWD klinisch relevant?
Bei allen drei Parametern, die die Qualität der Retardgalenik charakterisieren wie PTF-Wert, HWD oder Tmax ist die maximale Plasmakonzentration (Cmax) eine mehr oder minder entscheidende Bezugsgröße. Obwohl für die HWD nicht die Abhängigkeit von der Höhe der Wirkstoffkonzentration wie etwa für die Wirkungsdauer besteht, die mit steigendem Cmax-Wert zunimmt, zeigt auch die HWD als relativer Wert eine gewisse Beziehung zum Plasmaspiegel. Der Einfluss der Dosis und damit der Höhe des Plasmaspiegels (Cmax) auf die HWD ist jedoch relativ gering, wie eine Auswertung aus Plasmaspiegel-Verlaufskurven des retardierten Hydromorphons (Oros-Galenik) zeigt. Für die drei Dosierungen von 8, 16 und 32 mg (entsprechend ca. 40 – 160 mg Morphin) waren die Werte der HWD: 33, 35 und 35 Stunden [11]. Das bedeutet, eine vierfache Dosissteigerung bewirkt nur eine Änderung der HWD von etwa 10%. Daraus folgt, dass die absolute Höhe der Wirkstoffkonzentration (Cmax) keinen klinisch relevanten Einfluss auf die HWD hat.
Insbesondere haben unterschiedlich hohe Cmax-Werte keine qualitativen Auswirkungen auf den Verlauf der Freisetzungskinetik aus der Retardformulierung und damit auf die HWD. Das heißt, eine hohe Opioiddosierung macht aus einer schlechten HWD keine gute und vice versa.
Unabhängig davon sollten HWD-Vergleiche zwischen verschiedenen Präparaten möglichst bei gleicher bzw. äquianalgetischer Dosierung erfolgen.
Tmax und Dose dumping
Bei retardierten Arzneimitteln ist die Zeit bis zum Erreichen der maximalen Plasmakonzentration (Tmax) zwar nicht immer genau bzw. einfach zu bestimmen, nichtsdestotrotz ist dieser Wert wichtig für die Einschätzung eines bislang unterschätzten Risikos bei der Anwendung von oralen Retardpräparaten, das sog. Dose-dumping-Phänomen. Unter Dose dumping wird die unkontrollierte Freisetzung größerer Wirkstoffmengen aus Retardpräparaten verstanden. Ursache sind die zu langen Verweilzeiten der Arzneiform im Magen, die zu plötzlich erhöhten Wirkstoffspiegeln führen können, wenn Tmax zu gering ist [12]. Die Magenentleerung wird durch alkoholische Getränke verzögert – insbesondere durch Rotwein (Faktor 5). Aber auch nicht-alkoholische Getränke wie Fruchtsäfte, hochkalorische Getränke oder die sog. Energy drinks bewirken eine signifikante Verlangsamung der Magenentleerung [13]. Oft wird übersehen, dass die Aufnahme von fester und insbesondere fetter Nahrung zu langen Magenentleerungszeiten führt, die zwischen zwei bis drei Stunden (z. B. Kartoffeln, Bananen), drei bis vier Stunden (z. B. Äpfel, Spinat, Rührei), vier bis fünf Stunden (z. B. Hülsenfrüchte, Wild) oder sogar sechs bis acht Stunden bei Gänsebraten oder Ölsardinen liegen können.
Bereits ein eher karges Frühstück (2 Scheiben Brot, 40 g Käse, 150 ml Orangensaft, 150 ml Milch, 20 g Cerealien) erhöht den Medianwert der Magenentleerungszeit vom Nüchternwert (23 Minuten) auf 3,6 Stunden [14]. Unter diesen Bedingungen können die Retardpräparate vorwiegend im nicht kontinuierlich mit Mageninhalt durchmischten Magenfundus zwischengelagert werden, um später gegebenenfalls nach Stunden (sog. lag-Zeit) in einer Bolusentleerung größere Mengen gelösten Wirkstoffs ins Duodenum zu entleeren. Das kann insbesondere bei hoch dosierten Opioidretardpräparaten zu hohen Plasmaspiegeln führen und bedeutet damit ein relevantes Gefährdungspotenzial für den Patienten wie etwa vermehrte Nebenwirkungen bis hin zur Atemdepression.
Für retardierte Opioide, die alle 24 Stunden eingenommen werden sollen, sind die Tmax-Werte beispielsweise für MST Continus®: 2,3 ± 1,1 Std., für Capros® 1 x tägl.: 5 Std. und für Jurnista®: 12 – 16 Std. [15]. Das macht verständlich, dass bisher unter der Oros-Galenik (Jurnista®) keine Fälle mit deutlichem Dose dumping beobachtet worden sind, im Gegensatz zu anderen Retardformen [12].
Da isotone, körperwarme Flüssigkeit schnell (300 ml in maximal 30 min.) aus dem Magen entleert wird, sollten vor allem hochdosierte Retardpräparate (speziell mit geringem Tmax-Wert) zur Vermeidung des Dose-dumping-Phänomens nicht zu den Mahlzeiten, sondern möglichst mit mindestens 200 ml Wasser ca. 30 Minuten vor der Mahlzeit eingenommen werden.
Praktische Bedeutung der Halbwertsdauer
Es muss ausdrücklich darauf hingewiesen werden, dass die Halbwertsdauer und der PTF-Wert rein rechnerische Größen darstellen, die Indikatoren für die Qualität der Retardierung bzw. optimalen Applikationsintervalle sind, die aber keine Aussage über die analgetische Wirksamkeit erlauben.
Andererseits ist die durch die Halbwertsdauer objektivierte unzureichende Retardierung vieler Opioide nicht nur ein Theoretikum, sondern hat klinische Relevanz. Denn viele Schmerztherapeuten verordnen wegen der unzureichenden analgeti-schen Wirkdauer die sog. 12-Stunden-Präparate prinzipiell im 8-Stunden-Intervall. Diese durch mangelhafte Galenik erforderliche Verordnungspraxis ist nicht nur Compliance-unfreundlich, sondern stellt einen erheblichen Kostenfaktor dar.
Kostenfaktor
Wenn die Tagestherapiekosten (TTK) aufgrund der im Fachinfo-Service (FS) angegebenen – aber in praxi oft nicht zutreffenden – Einnahmeintervalle berechnet werden, resultieren Kosten, die realiter falsch sind.
Stattdessen ergeben die sog. Halbwertsdauer-basierten Tagestherapiekosten eine zutreffendere Kostenberechnung:
TTK / HWD 24/τ x 24.
HWD24/τ ist die Anzahl der HWD in 24 Stunden gemäß vorgeschriebenem Dosierungsintervall(τ): also 3 HWD bei 8-stündiger bzw. 2 HWD bei 12-stündiger und 1 HWD bei einmal täglicher Einnahme. Außerdem gilt, wenn HWD > τ dann HWD = τ.
Halbwertsdauer-basierte Tagestherapiekosten sind die Kosten, die über 24 Stunden einen Opioid-Plasmaspiegel von mindestens einem halben Cmax-Wert garantieren.
Das bedeutet in praxi, wenn die Opioiddosierung so gewählt wird, dass die minimale analgetisch effektive Konzentration mindestens der halben Cmax -Konzentration entspricht, ist das Risiko von End-of-dose-Schmerzen nahezu ausgeschlossen.
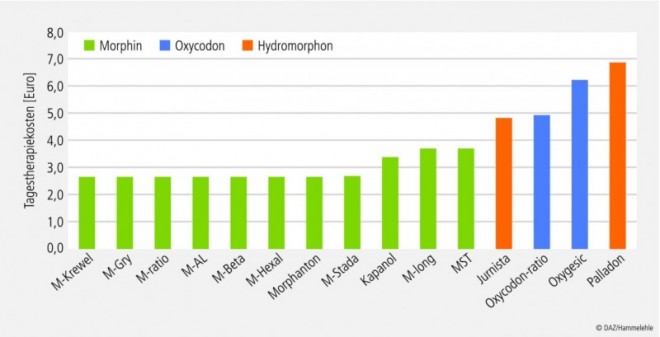
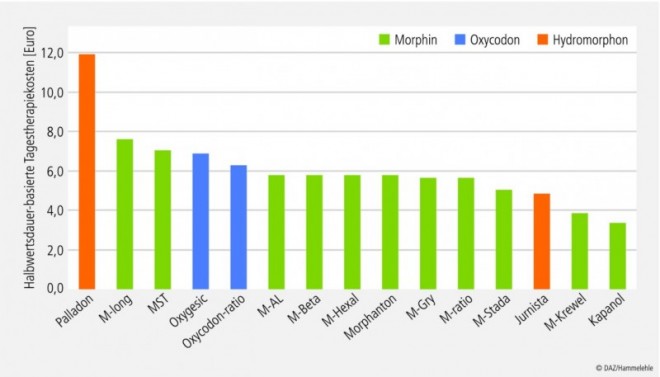
In Abbildung 2 sind die Tagestherapiekosten (Dosierungsintervalle gemäß Fachinfo-Service) von verschiedenen peroralen Retardpräparaten (Morphin, Oxycodon, Hydromorphon) in annähernd äquianalgetischer Dosierung dargestellt, in Abbildung 3 die entsprechenden Halbwertsdauer-basierten Tagestherapiekosten. Für die sog. DDD-Kosten, die allerdings keinen äquianalgetischen Vergleich gestatten, zeigen sich ähnliche kostenrelevante Unterschiede (Tab. 2).
| Tab. 2. DDD-Kosten und Halbwertsdauer (HWD)-basierte DDD-Kosten. Einzelheiten s. Text. [Schwabe U & Paffrath D (Hrsg.): Arzneiverordnungsreport 2008] | ||
| Präparat | DDD-Kosten | HWD-basierte DDD-Kosten |
| M-Krewel | 2.32 | 3.35 |
| M-beta | 2.52 | 5.50 |
| M-STADA | 2.59 | 4.93 |
| M-ratiopharm | 2.65 | 5.68 |
| M-AL | 2.76 | 6.02 |
| M-HEXAL | 2.77 | 6.04 |
| M-GRY | 2.96 | 6.34 |
| Kapanol | 3.32 | 3.32 |
| Jurnista | 6.19 | 6.19 |
| Oxycodon-ratio | 6.34 | 8.09 |
| Palladon | 7.42 | 12.90 |
| Oxygesic | 8.44 | 9.29 |
Austauschbarkeit der Arzneimittel
Außerdem ist die HWD ein wichtiger Parameter für die Austauschbarkeit retardierter Opioidpräparate. Nicht nur formale Gründe wie fehlende Aut-idem-Markierung, limitierendes Budget oder bestehende Industrie-KV-Rabattverträge, sondern auch medizinische Aspekte wie etwa die sog. Opioidrotation machen die Kenntnis der HWD für Apotheker und Arzt unverzichtbar (vgl. Tab. 1).
Wenn ohne Kenntnis bzw. Berücksichtigung der HWD ein Patient von einem Opioidpräparat mit langer HWD auf ein anderes Opioidpräparat mit relativ kurzer HWD umgestellt wird, dann ist das Risiko für diesen Patienten deutlich erhöht, End-of-dose-Schmerzen zu erleiden.
Natürlich ist es primär Aufgabe des behandelnden Arztes, diesen Durchbruchschmerz beim chronischen Schmerzpatienten zu erkennen und durch entsprechende Maßnahmen wie Verkürzung des Dosierungsintervalls bzw. Erhöhung der Dosis zu beheben. Allerdings bedeutet dies – außer den höheren Kosten – für den Patienten eine reduzierte Compliance bzw. eine höhere Rate unerwünschter Opioidwirkungen durch relativ zu hohe maximale Opioidplasmaspiegel.
Informationsdefizit bei Ärzten und Apothekern
Der eingängige Parameter Halbwertsdauer könnte gerade für einen pharmakokinetisch weniger Versierten ein hilfreiches Kriterium bei der Auswahl von Retardpräparaten sein. Doch die mangelhaften Angaben zur Beurteilung der Retardform-spezifischen Freisetzungskinetik im Fachinfo-Service erschweren dem Arzt unnötig eine suffiziente Schmerztherapie. Denn anders als etwa bei Koronarmitteln (z. B. ISDN Stada® retard) ist bisher bei keinem retardierten Opioidpräparat in den Fach-Infos die HWD angegeben, obwohl dies bereits 2001 angemahnt wurde [16] und heutzutage wegen des seit 2008 gültigen Rahmenvertrages zur Arzneimittelversorgung für den Arzt und Apotheker umso wichtiger wäre.
Ignoranz der Hersteller
Darüber hinaus sollten Galeniker von den pharmazeutischen Firmen, deren Präparate bisher eine eher suboptimale HWD aufweisen, weniger über die Sinnhaftigkeit der HWD diskutieren oder sie ignorieren und allein den PTF-Wert favorisieren, als insgesamt eine bessere Galenik ihrer Retardpräparate realisieren. Denn eine bestmögliche Schmerztherapie mit einem oralen retardierten Opioid kann nur gelingen, wenn die Galenik alle drei pharmakokinetischen Kriterien optimiert:
- Nicht nur einen kleinen PTF-Wert und damit geringere Plasmaspiegel-Fluktuationen, sondern auch
- eine hohe Halbwertsdauer, um dadurch das Risiko der sog. End-of-Dose-Schmerzen zu verringern und zusätzlich
- einen höheren Tmax-Wert, um das Dose-dumping-Phänomen zu vermeiden.
Kurz zusammengefasst
|
Literatur
[1] Meier J, Nüesch E, Schmidt R: Pharmacokinetic Criteria for the Evaluation of Retard Formulations. Eur J Clin Pharmacol 1974; 7: 429–432
[2] Jonkman JHG, Berg WChr, de Vries K et al.: Disposition and clinical pharmacokinetics of theophylline after administration of a new sustained release tablet. Eur J Clin Pharmacol 1981; 21:39 – 44
[3] Steinijans VW, Trautmann H, Johnson E, Beier W: Theophylline steady-state pharmacokinetics: recent concepts and their application in chronotherapy of reactive airway diseases. Chronobiol Int 1987; 4:331– 47;
[4] Mehnert W.:Therapeutische Äquivalenz. (S 59– 60) In: Jaehde U, Radziwill R, Mühlebach S, Schunack W (Hrsg): Lehrbuch der Klinischen Pharmazie. Wissenschaftl. Verlagsgesellschaft, Stuttgart, 2003
[5] Portenoy RK and Hagen NA: Breakthrough pain: definition, prevalence and characteristics. Pain 1990; 41:273 – 81
[6] Güttler K Interview durch Uhl D: Retardierte Opioide auf dem Prüfstand. Dtsch Apo Ztg 2008; 148 (1/2): 65 – 69
[7] Sathyan G, Xu E, Thipphawong J, Gupta SK: Pharmacokinetic profile of a 24-hour controlled-release OROS® formulation of hydromorphone in the presence and absence of food. BMC Clin Pharmacol 2007;7:2 [http://www.biomedcentral.com/1472-6904/7/2]
[8] Hagen NA, Thirlwell M, Eisenhoffer J et al.: Efficacy, safety, and steady-state pharmacokinetics of once-a-day controlled-release morphine (MS Contin XL®) in cancer pain. J Pain Symptom Manage 2005; 29:80 – 90
[9] Eichelbaum M, Schwab M: Arzneistoffkonzentration im Organismus in Abhängigkeit von der Zeit: Pharmakokinetik im engeren Sinn. (72-73) In: Aktories K, Förstermann U, Hofmann F, Starke K (Hrsg): Allgemeine und spezielle Pharmakologie und Toxikologie. Urban & Fischer, München, 2009
[10] Drover DR, Angst MS, Valle M et al: Input characteristics and bioavailability after administration of immediate and a new extended-release formulation of hydromorphone in healthy volunteers. Anesthesiology 2002; 97:827–36
[11] Gupta S and Sathyan G. Providing constant analgesia with OROS® hydromorphone. J Pain Symptom Manage 2007; 33:S19–S24
[12] Adam U, Aurich K, Weitschies W, Blume H: Retardierte Opioide: Dose dumping durch Alkohol? Dtsch Apo Ztg 2008;148:1824-32
[13] Franke A, Teyssen S, Harder H, Singer MV: Effect of ethanol and some alcoholic beverages on gastric emptying in humans. Scand J Gastroenterol; 2004; 39(7):638-44
[14] Weitschies W, Wedemeyer RS, Kosch O et al.: Impact of the intragastric location of extended release tablets on food interactions. J Control Release 2005;108(2-3),375-85
[15] Sathyan G, Xu E, Thipphawong J, Gupta SK: Pharmacokinetic investigation of dose proportionality with a 24-hour controlled-release formulation of hydromorphone. BMC Clin Pharmacol 2007; 7:3 [http://www.biomedcentral.com/1472-6904/7/3]
[16] Güttler K. Medikamentöse Schmerztherapie: Grundlagen und internistische Anwendungen. (S 121) In: Wörz R (Hrsg.): Differenzierte medikamentöse Schmerz-therapie. Urban & Fischer, München-Jena, 2001
Nota bene: Die Zahlenangaben zu den Tmax- und PTF-Werten sind soweit nicht anders angegeben den entsprechenden Fachinformationen der Herstellerfirmen (Rote Liste Service GmbH; Postfach 11 01 71, 10831 Berlin) entnommen.
Autor
Dr. Kuno Gütller,
Institut für Pharmakologie,
Uniklinik Köln,
Gleueler Str.24,
50931 Köln























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.