
- DAZ.online
- DAZ / AZ
- DAZ 31/2007
- Hepatozelluläres
Arzneimittel und Therapie
Hepatozelluläres Karzinom
Sorafenib wirkt auch gegen Leberzellkrebs
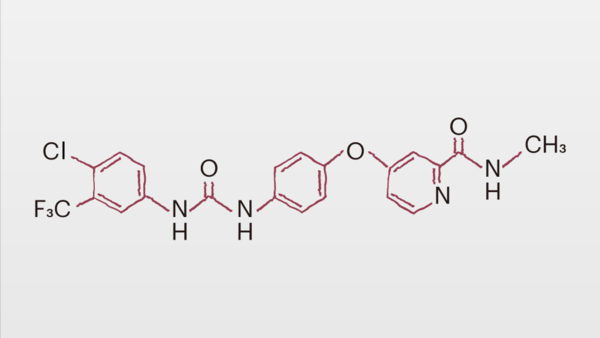
Die gezielte Ausrichtung einer medikamentösen Therapie auf bestimmte molekulare Defekte (targeted therapy) soll die Behandlung auch von Tumoren revolutionieren. Für dieses Prinzip steht der Multi-Kinasehemmer Sorafenib (Nexavar®), der in den Tumorzellen außer Kontrolle geratene Signalwege blockiert. Bereits seit Juli 2006 zur Therapie des Nierenzellkarzinoms zugelassen, hat Sorafenib jetzt auch günstige klinische Ergebnisse in der Phase-III-Studie gegen Leberzellkrebs geliefert. Die Zulassung für diese Indikation wird für Ende 2007 erwartet.
Entwickelt wurde Sorafenib ursprünglich als Raf-Kinase-Inhibitor. Bei rund 30% der Tumore ist der für die normale Zellteilung verantwortliche Ras/Raf-Kinase-Signalweg gestört: Das Signalprotein Ras schaltet sich dabei nach erfolgter Zellteilung nicht wieder ab. Die Folge ist ein überschießendes, unkontrolliertes Zellwachstum. "Für die Weiterleitung der Signale in den Zellkern wird Raf als weiteres Signalprotein benötigt", so Enghofer, "und genau dieses wird durch Sorafenib blockiert. Der Wachstumsstimulus kann nicht weitergegeben werden." Außerdem hemmt der Wirkstoff noch weitere Kinasen, so die Tyrosinkinasen des VEGF-Rezeptors (vascular endothelial growth factor) sowie des PDGF-Rezeptors beta (platelet derived growth factor). Sie sind maßgeblich an der Bildung neuer tumorversorgender Blutgefäße beteiligt.
Die Wirkung von Sorafenib gegen das hepatozelluläre Karzinom (HCC) wurde in der internationalen, randomisierten, doppelblinden, placebokontrollierten Phase-III-Studie SHARP (Sorafenib HCC Assessment Randomized Protocol Trial) getestet. 602 Patienten erhielten zweimal täglich 400 mg Sorafenib bzw. Placebo, Einschlusskriterien waren ein histologisch nachgewiesenes hepatozelluläres Karzinom mit mindestens einer radiologisch messbaren Läsion, ein guter Allgemeinzustand, das Fehlen einer systemischen Vorbehandlung und ein Child-Pugh-Score der Klasse A. Mit diesem Score kann eine Leberzirrhose in Stadien eingeteilt werden, es lässt sich gleichzeitig anhand dieser Stadien die Prognose des Patienten abschätzen. Ein Child-Pugh-Score der Klasse A entspricht einem noch nicht allzu sehr fortgeschrittenem Krankheitsstadium, wie es in Deutschland auf etwa drei von fünf Patienten zutrifft.
Die Ergebnisse der SHARP-Studie waren so überzeugend, dass sie im Februar 2007 vorzeitig beendet wurde, um nunmehr auch den Patienten der Placebo-Gruppe das Verum anzubieten. Denn der Multi-Kinasehemmer war in beiden primären Endpunkten dem Placebo hochsignifikant überlegen: Das Gesamtüberleben betrug in der Verum-Gruppe durchschnittlich 10,7 Monate vs. 7,9 Monate unter Placebo. Die Zeit bis zum symptomatischen Progress lag mit Sorafenib bei 24 Wochen (5,5 Monaten), mit Placebo dagegen bei nur 12,3 Wochen (2,8 Monaten). Die verlängerte Zeit bis zur Tumorprogression spricht zudem für eine bessere Lebensqualität der Patienten im Sorafenib-Studienarm. Die in der Studie beobachteten Nebenwirkungen von Sorafenib wurden als "akzeptabel" bezeichnet. Sie bestanden vor allem in Diarrhö, Hautreaktionen an Händen und Füßen sowie Gewichtsverlust.
Ein Wirkmechanismus – viele mögliche Indikationen
Neben dem Nieren- und Leberzellkarzinom soll Sorafenib auch gegen etliche weitere Krebserkrankungen eingesetzt werden. In klinischen Studien der Phase II bzw. III werden derzeit Wirksamkeit und Verträglichkeit von Sorafenib bei Mammakarzinom, kleinzelligem und nicht-kleinzelligem Bronchialkarzinom, Ovarialkarzinom und auch bei der akuten myeloischen Leukämie (AML), einer seltenen hämatologisch-onkologischen Erkrankung, untersucht. Hier gilt es vor allem fest zustellen, ob die von Sorafenib beeinflussten Kinasen bei diesen Tumorerkrankungen tatsächlich eine ähnlich große Rolle spielen wie beim Nierenzellkrebs und beim hepatozellulären Karzinom.
QuelleDr. Erich Enghofer, Leverkusen; Prof. Dr. med. Tim Greten, Hannover: "Innovativer Therapieansatz zur Lebensverlängerung beim Leberzellkarzinom", Frankfurt/Main, 22. Juni 2007, veranstaltet von der Bayer HealthCare AG, Leverkusen. Simone Reisdorf, freie Medizinjournalistin






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.