
- DAZ.online
- News
- Pharmazie
- MS-Patient stirbt an ...
Lemtrada bei Multipler Sklerose
MS-Patient stirbt an Thrombozytopenie nach Alemtuzumab-Gabe
Stuttgart - 20.11.2017, 15:00 Uhr

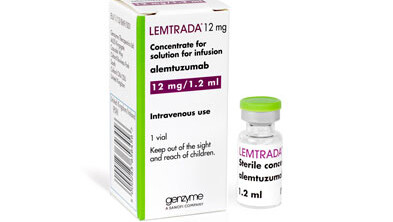
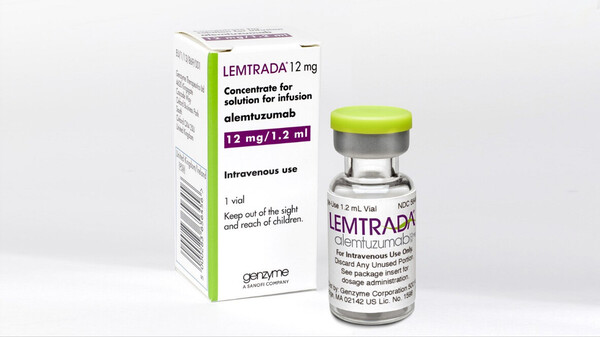
Lemtrada löste eine therapierefraktäre Thrombozytopenie aus, woran ein 34-jähriger Multiple-Sklerose-Patient verstarb. (Foto: Genzyme)
Alemtuzumab kann schwere Thrombozytopenien auslösen. Diese Nebenwirkung des bei remittierend-schubförmiger Multipler Sklerose eingesetzten CD52-Antikörpers ist bekannt. Neu ist, dass diese Idiopathische thrombozytopenische Purpura (ITP) nicht auf eine Behandlung anspricht. Die Arzneimittelkommission der Ärzteschaft informiert in einer Drug-Safety-Mail über den zweiten Thrombozytopenie-bedingten Todesfall unter Lemtrada®.
Patienten, die aufgrund Multipler Sklerose Alemtuzumab erhalten, entwickeln in 1 Prozent der Fälle schwere idiopathische thrombozytopenische Purpura, ITP. Diese bekannte Nebenwirkung tritt meist 14 bis 36 Monate nach der ersten Alemtuzumab-Infusion auf. Bereits in den Zulassungsstudien verstarb ein MS-Patient an ITP, da die Thrombozytopenie vermutlich zu spät erkannt wurde, um therapeutisch noch erfolgreich zu intervenieren und den Patienten zu retten. Aus diesem Grund müssen Ärzte bei einer Lemtrada®-Therapie die Blutwerte der MS-Patienten regelmäßig überprüfen, und zwar vor Start der ersten Lemtrada®-Infusion und bis 48 Monate nach der letzten Gabe von Alemtuzumab. Lemtrada® erhalten MS-Patienten in zwei Behandlungszyklen: Im ersten Jahr bekommen sie 12 mg Alemtuzumab an fünf aufeinanderfolgenden Tagen. Das zweite Behandlungsjahr umfasst nur noch drei Infusionen Alemtuzumab à 12 mg ebenfalls an aufeinanderfolgenden Tagen.
Alemtuzumab-Thrombozytopenie war therapieresistent
Die Arzneimittelkommission der Ärzteschaft (AkdÄ) meldet nun den Tod eines weiteren Patienten unter Alemtuzumab-Therapie. Allerdings erkannte man im aktuellen Fall des 34-jährigen MS-Patienten die Thrombozytopenie rechtzeitig, nur sprach der junge Mann auf keine Therapie an und verstarb letztendlich an einer Kleinhirnblutung.
Thrombozytopenien auch mild und selbstlimitierend
Eine Thrombozytopenie zeigt sich durch vermehrte Blutergüsse, punktförmige Einblutungen – Petechien, Schleimhautblutungen und bei Frauen durch eine verstärkte Menstruation. MS-Patienten mit einer Thrombozytopenie unter Alemtuzumab erhalten als Gegenmaßnahme in der Erstlinientherapie Glucocorticoide. Laboranalytisch macht sich die Thrombozytopenie durch eine verminderte Zahl an Blutplättchen bemerkbar. Liegen die Normwerte bei gesunden Menschen bei 150.000 bis 450.000 Thrombozyten pro µl Blut, spricht man bei Werten unter 80.000 von einer klinisch relevanten Thrombozytopenie, da ab diesen Werten relevante Blutungen zu befürchten sind.
Nicht jeder Fall einer beschriebenen Thrombozytopenie unter Alemtuzumab verläuft derart schwerwiegend bis tödlich. So beschreibt eine Fallserie 22 Patienten, die eine milde ITP unter Lemtrada® entwickelten. Die Thrombozyten erholten sich auch ohne therapeutische Maßnahmen innerhalb von zwei Monaten bei diesen Patienten.
Alemtuzumab in der Diskussion: Thrombozytopenie und Verschlechterung von MS
Nicht zum ersten Mal ist Alemtuzumab in der Diskussion aufgrund schwerer unerwünschter Arzneimittelwirkungen. Anfang dieses Jahres hat Lancet Neurology zwei Fallberichte veröffentlicht, in denen MS-Patienten neue MRT-Läsionen und eine Verschlechterung ihrer MS-Symptomatik unter Alemtuzumab zeigten. Was die Kliniker allerdings nicht aufklären konnten, war, ob die im MRT neu aufgetretenen Läsionen bei den Multiplen Sklerotikern als Fortschreiten der MS zu werten waren oder als weitere, von der Multiplen Sklerose unabhängige, Autoimmunprozesse.
Mehr zum Thema
Antikörper gegen Multiple Sklerose
Verschlechtert Alemtuzumab MS?
Die US-amerikanische Zulassungsbehörde hat dem Nebenwirkungsprofil von Lemtrada® Rechnung getragen; die FDA schränkt den Einsatz von Alemtuzumab auf MS-Patienten ein, die zuvor auf zwei oder mehrere Arzneimittel nicht ausreichend angesprochen haben. In Europa dürfen Neurologen Alemtuzumab freier anwenden: „Lemtrada® ist angezeigt zur Behandlung von erwachsenen Patienten mit schubförmig-remittierender Multipler Sklerose (RRMS) mit aktiver Erkrankung“.
Wie wirkt Alemtuzumab bei Multipler Sklerose?
Der exakte Wirkmechanismus des humanisierten CD52-Antikörpers bei MS ist nicht vollständig geklärt. Vor allem CD3-T-Lymphozyten und CD19-B-Lymphozyten exprimieren das Glykoprotein. Durch Bindung von Alemtuzumab an die CD52-positiven Lymphozyten lösen sie eine komplementvermittelte Zytolyse aus. Die Forschung weist „in Richtung immunmodulatorischer Wirkung“, schreibt die Fachinformation zu Lemtrada. Hierdurch kommt es wohl zu einer Senkung der zirkulierenden B- und T-Zellen und einer sich anschließenden Repopulation, was die Wahrscheinlichkeit eines erneuten Schubs bei Multipler Sklerose verringert.
Diese modulierende Eigenschaft auf das Immunsystem durch Lemtrada® wird auch der Nebenwirkung ITP zugrunde gelegt. Denn die Reaktion der Blutplättchen auf Alemtuzumab ist keine typische arzneimittelinduzierte Immunthrombozytopenie, bei der die Antikörper nur in Anwesenheit des Arzneimittels binden. In solchen Fällen bindet das Arzneimittel reversibel direkt an ein Glykoprotein auf der Oberfläche der Thrombozyten und führt so zu einer Konformationsänderung dieses gebundenen Oberflächenproteins. Diese Konformationsänderung schafft so ein neues Epitop, das die Auto-Antikörperbildung auslöst. Wohingegen die durch Alemtuzumab ausgelöste Bildung von Autoantikörpern gegen Thrombozyten durch eine Fehlregulation des Immunsystems bewirkt wird.
Kommerzielle Interessen in der Historie machten Mabcampath® zu Lemtrada®
Alemtuzumab sorgte bereits früher für Aufsehen. Der CD52-Antikörper war seit 2001 als Mabcampath® für Patienten mit chronisch lymphatischer Leukämie vom B-Zell-Typ (B-CLL) zugelassen. Nachdem der Hersteller Genzyme jedoch feststellte, dass Alemtuzumab auch bei Multipler Sklerose Wirksamkeit zeigt, hat Genzyme die Zulassung von Mabcampath® bei Leukämie zugunsten der Zulassung des Antikörpers bei MS zurückgegeben. Seit 2013 steht Alemtuzumab in Lemtrada® Patienten mit remittierend schubförmiger MS als therapeutische Option zur Verfügung.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.