

Remagen - 07.07.2020, 14:00 Uhr
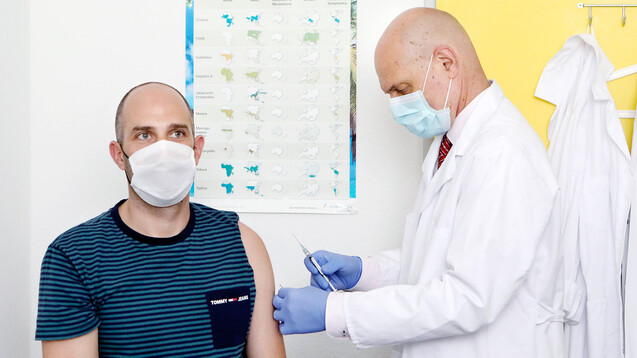
Die Impfstoff-Forschung gegen SARS-CoV-2 schreitet voran. Hier ist Prof. Dr. Peter Kremsner (Institut für Tropenmedizin Tübingen) zu sehen, wie er einen Probanden mit dem Impfstoff von Curevac in der 1. Phase der klinischen Studie impft. (c / Foto: imago images / ULMER Pressebildagentur)
Mittlerweile werden weltweit 19 Impfstoffkandidaten gegen das neuartige Coronavirus am Menschen getestet. Als erster konnte AZD1222 aus Oxford die klinische Phase 3 erklimmen. Ihm folgt nun CoronaVac von Sinovac LS. Soeben hat die brasilianische Arzneimittelbehörde Anvisa die Genehmigung zum Beginn der Studie erteilt. Die Rekrutierung der fast 9.000 Teilnehmer aus Kreisen der Gesundheitsberufe soll in diesem Monat losgehen.
Nach der aktuellen „Draft landscape of COVID-19 candidate vaccines“ der WHO vom 6. Juli 2020 hat die Zahl der COVID-19-Impfstoffkandidaten, die in der klinischen Erprobung angekommen sind, weiter zugenommen. Mittlerweile sind es 19 Kandidaten, davon zehn in den Phasen 3, 2 und 1/2. Neun weitere haben es immerhin schon bis in die Phase 1 geschafft, darunter auch die mRNA-Vakzine von Curevac (NCT04449276). Darüber hinaus befindet sich ein schier unüberschaubares Feld von 130 weiteren Kandidaten in der präklinischen Phase.

Der erste COVID-19-Impfstoffkandidat in der klinischen Phase 3 war „ChAdOx1” vom Jenner Institute der Oxford Universität (seit der Partnerschaft mit AstraZeneca „AZD1222“). Bereits 8.000 Freiwillige sollen für die Studie rekrutiert worden sein, die in Großbritannien, Südafrika und neuerdings auch in Brasilien läuft. Ende Juni hatte die Universität Oxford über den Start der Studie, der ersten in Phase 3 zu einer COVID-19-Vakzine in Lateinamerika, informiert. Die Studienzentren befinden sich in Sao Paulo, Rio de Janeiro und im Nordosten von Brasilien.
Nun bekommen die Briten vor Ort einen Mitstreiter beziehungsweise „Konkurrenz“. Am 3. Juli 2020 hat die brasilianische Regulierungsbehörde Anvisa der Firma Sinovac LS, einer Tochtergesellschaft von Sinovac in Brasilien, eine Genehmigung für eine Phase 3-Studie mit dem inaktivierten COVID-19-Impfstoff CoronaVac erteilt (NCT04456595). Die Studie wird von dem brasilianischen Instituto Butantan gesponsert. Die Agentur hat den Antrag im Rekordtempo von nur zwei Wochen bearbeitet. Die Studie soll fast 9.000 Angehörige der Gesundheitsberufe rekrutieren, die in COVID-19-Einrichtungen an zwölf klinischen Standorten in mehreren brasilianischen Bundesstaaten arbeiten. Die Aufnahme der Teilnehmer soll in diesem Monat beginnen, sobald die Voten der Ethikkommissionen für jeden Standort eingeholt sind. Der Impfplan umfasst zwei intramuskuläre Injektionen im Abstand von 14 Tagen. Zur Bewertung der Sicherheit und Immunogenität werden die erwachsenen Teilnehmer in zwei Gruppen eingeteilt (18 bis 59 Jahre und über 60 Jahre). Alle werden über zwölf Monate nachbeobachtet. Vorläufige Zwischenergebnisse hinsichtlich der Wirksamkeit sollen bei Erreichen einer Zielanzahl von 150 Fällen präsentiert werden können. Als Studienende wird September 2021 angegeben.
Die Tabelle trägt die Kernfakten zu den am weitesten fortgeschrittenen COVID-19-Impfstoffprojekten zusammen.
| Bezeichnung des Impfstoffs | Impfstofftyp | Entwickler / Funding | Aktueller Stand der klinischen Erprobung Codes in Studienregistern (clinicaltrials.gov, chin Studienregister, EudraCT) |
| AZD1222 | Adenovirus-Vektor-Impfstoff
| University of Oxford / AstraZeneca / BARDA | Phase 3 Phase 2b/3 Phase 1/2 |
| CoronaVac | Inaktiviertes Virus, plus Adjuvans | Sinovac / Instituto Butantan | Phase 3 (not yet recruiting) |
| Ad5-nCoV | Adenovirus-Vektor-Impfstoff | CanSino Biological Inc. / Beijing Institute of Biotechnology | Phase 2 Phase 1 |
| mRNA-1273 | mRNA-Impfstoff
| Moderna / NIAID/BARDA | Phase 2 Phase 1 |
| INO-4800 | DNA-Plasmid-Impfstoff
| Inovio Pharmaceuticals | Phase 1/2 NCT04447781 NCT04336410 |
| Unbenannt | DNA-Plasmid-Impfstoff
| Cadila Healthcare Limited
| Phase 1/2 CTRI/2020/07/026352 (not yet recruiting) |
| Unbenannt | Inaktiviertes Virus | Wuhan Institute of Biological Products / Sinopharm | Phase 1/2 ChiCTR2000031809 |
| Unbenannt | Inaktiviertes Virus | Beijing Institute of Biological Products / Sinopharm | Phase 1/2 hiCTR2000032459 |
| NVX-CoV2373 | Protein-Untereinheit, plus Adjuvans Matrix M | Novavax | Phase 1/2 NCT04368988 |
| BNT162 | mRNA-Impfstoff | BioNTech / Fosun Pharma / Pfizer | Phase 1/2 2020-001038-36 NCT04368728 |
0 Kommentare
Das Kommentieren ist aktuell nicht möglich.